| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《物质的量》试题预测(2017年最新版)(二)
参考答案:D 本题解析:铜和硝酸反应,随着浓度的减少,硝酸的还原产物的价态越低,铜和浓硝酸反应生成NO2,而与稀硝酸反应时则生成NO,故生成的气体有NO2和NO,则n(NO2)+n(NO)= 本题难度:一般 2、选择题 设NA为阿伏加德罗常数的值。下列说法中错误的是 ( ) |
参考答案:B
本题解析:略
本题难度:一般
3、选择题 溶质相同、质量分数为a%和b%的两份溶液质量分别为mg、ng,将两份溶液混合并蒸发去xg水,所得溶液的物质的量浓度为c mol/L。关于求溶质的摩尔质量,下列说法正确的是(?)
A.只要知道蒸发后所得溶液的密度(ρ),就能求出溶质的摩尔质量
B.只要知道混合前两份溶液的物质的量浓度(c),就能求出溶质的摩尔质量
C.只要知道蒸发前混合液的体积(V),就能求出溶质的摩尔质量
D.以上说法都不正确。
参考答案:
D
本题解析:
混合液中的溶质如果是易挥发或分解的,就无法求出溶质的摩尔质量。
本题难度:一般
4、选择题 等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是(?)
A.2 mol・L-1 H2SO4溶液
B.18 mol・L-1 H2SO4溶液
C.6 mol・L-1 KOH溶液
D.3 mol・L-1 HNO3溶液
参考答案:A
本题解析:18 mol・L-1H2SO4溶液是浓硫酸,Al遇浓硫酸发生钝化、Mg与浓硫酸生成二氧化硫,不产生氢气,B错误;3 mol・L-1HNO3溶液是稀硝酸,Mg、Al与稀硝酸产生NO,D错误;Mg能与稀硫酸产生H2、与KOH溶液不反应,Al与稀硫酸和KOH溶液都产生H2,且均有2Al~3H2,所以产生H2最多的是A。
点评:Al与过量盐酸、稀硫酸或强碱溶液都产生H2,且均有2Al~3H2。
本题难度:一般
5、计算题 一定量的Mg、Al的混合物中加入足量盐酸,产生标准状况下的气体5.6升,再在此溶液中加入过量NaOH溶液,最终得到沉淀5.8克,求:
(1)Mg、Al的物质的量各为多少?
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积。
参考答案:依题意得镁的物质的量: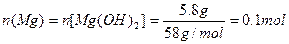
设铝的物质的量为Y,则有 ?
?
解得Y = 0.1mol
将混合物投入足量氢氧化钠溶液中得到氢气的体积: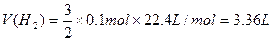
本题解析:略
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《影响盐类水.. | |