��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���л�ѧ�����ȷ���ǣ�?��
A��˫��ˮʹ����KMnO4��Һ�ĺ�ɫ��ȥ��3H2O2+2MnO4-+6H+===2Mn2++4O2��+6H2O
B��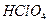 �ĵ��뷽��ʽ��
�ĵ��뷽��ʽ��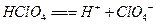
C���������������Һ���������ĵ缫����ʽΪ��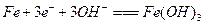
D����ʾ�к��ȵ��Ȼ�ѧ����ʽ��2NaOH(aq)+H2SO4(aq) ===Na2SO4(aq)+2H2O(l)
�ο��𰸣�B
�����������
�����Ѷȣ���
2��ѡ���� ����ȷ��ʾ���л�ѧ��Ӧ�����ӷ���ʽ����
A������������Һ��ϡ����ķ�Ӧ OH-��H+�� H2O
B����������ϡ���ᷴӦ CaO + 2H+= Ca2+ + H2O
C����Ƭ������������Һ�� Fe + Ag+= Fe2+ + Ag
D��̼�������ϡ������ CO32+��2H+��CO2?��H2O
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
3��ѡ���� ���з�Ӧ�����ӷ���ʽ����ȷ����?��?��
A��Na2O2����ˮ��2Na2O2+2H2O=4Na+��4OH��+O2��
B�������ռ����Ca(HCO3)2��Һ��Ca2++2HCO3��+2OH��=CaCO3 ��+2H2O+CO32��
C��������Ͷ��ˮ�У�2Na+2H2O=2Na++2OH��+H2��
D������������Һ���չ���CO2�� CO2��2OH��=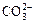 ��H2O
��H2O
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
4��ѡ���� ���з�Ӧ�����ӷ���ʽ��д����ȷ���ǣ�������
A�����͵�̼������Һ��ͨ������HCl���壺Na++CO32-+H+=NaHCO3��
B����AgNO3��Һ�еμӹ�����ˮ��Ag++2NH3?H2O=[Ag��NH3��2]++2H2O
C������������Һ��ͨ��������SO2���壺2ClO-+SO2+H2O=SO32-+2HClO
D��4mol?L-1��NaAlO2��Һ��7mol?L-1������������ϣ�4AlO2-+7H++H2O=3A1��OH��3��+Al3+
�ο��𰸣�A�����͵�̼������Һ��ͨ������HCl���壬̼���ƺ��Ȼ��ⷴӦ����̼�����ƺ��Ȼ��ƣ�����̼�����Ƶ��ܽ���С��̼���ƣ��������ɵ�̼�����ƻ��������壬���ӷ���ʽΪNa++CO32-+H+=NaHCO3������A��ȷ��
B����AgNO3��Һ�еμӹ�����ˮ�����ɵ��������������ڹ�����ˮ���������������ӷ���ʽΪAg++2NH3?H2O=[Ag��NH3��2]++2H2O����B��ȷ��
C������������Һ��ͨ��������SO2���壬�������Ѷ�����������Ϊ���ᣬ��������ԭΪ�����ӣ���C����
D��4mol?L-1��NaAlO2��Һ��7mol?L-1������������ϣ�4molAlO2-��7molH+��Ӧ��
?AlO2-+H++H2O=A1��OH��3����
4mol?4mol? 4mol
A1��OH��3+3H+=Al3++3H2O��
?1mol? 3mol? 1mol
�������ӷ���ʽΪ��4AlO2-+7H++H2O=3A1��OH��3��+Al3+
��D��ȷ��
��ѡC��
���������
�����Ѷȣ�һ��
5������� �����ʵ��Ļ�ѧ������գ�
��1��Na2CO3ˮ������ӷ���ʽ��______��
��2��H2S���뷽��ʽ��______��
��3��AlCl3ˮ������ӷ���ʽ��______��
��4����25�桢101kPa�£�lg������ȫȼ������CO2��Һ̬ˮʱ����55.6kJ������д����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ��______��
��5����������ȼ�ϵ�ص������缫����ʽ
������______��������______��
��6��д��NaHCO3��Һ�е�����Ũ�ȹ�ϵ
c��H+��+c��Na+��=______��
c��Na+��=______��
�ο��𰸣���1��̼����ˮ��Һ��ˮ�⣬̼��������Ƕ�Ԫ���������ӷֲ�ˮ�⣬ˮ������ӷ���ʽΪ��CO32-+H2O?OH-+HCO3-���ʴ�Ϊ��CO32-+H2O?OH-+HCO3-��
��2��������������ʣ���ˮ��Һ�д��ڵ���ƽ�⣬��Ԫ����ֲ����룬����ķ���ʽΪ��H2S?H++HS-���ʴ�Ϊ��H2S?H++HS-��
��3���Ȼ���ˮ��Һ��������ˮ�����������������Ȼ��⣬�ʴ�Ϊ��Al3++3H2O?Al��OH��3��+3H+��
��4��lg������ȫȼ������CO2��Һ̬ˮʱ����55.6kJ������16g����ȼ�շ���889.6KJ�������Ȼ�ѧ����ʽ��д������ע�ۼ�״̬�Ͷ�Ӧ�ʱ�д���Ȼ�ѧ����ʽΪ��
CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-889.6 kJ/mol��
�ʴ�Ϊ��CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-889.6kJ/mol��
��5������ȼ�ϵ��ԭ�������������ڸ���ʧ���ӷ���������Ӧ��������Һ������ˮ�������缫��ӦΪ��2H2-4e-+4OH-=4H2O�������õ������������������ӣ������缫��ӦΪ��O2+4e-+2H2O=4OH-��
�ʴ�Ϊ��2H2-4e-+4OH-=4H2O��O2+4e-+2H2O=4OH-��
��6��̼��������Һ�д��ڵ���غ�Ϊ��c��Na+��+c��H+��=c��OH-��+2c��CO32-��+c��HCO3-���������غ�����Ԫ�غ�̼Ԫ�ص��غ㣬���ݻ�ѧʽ��֪��Ԫ�غ�̼Ԫ����ͬ��̼Ԫ�صĴ�����ʽ��̼���������ˮ��͵��뷢���ı䣬�õ������غ�Ϊc��Na+��=c��HCO3-��+c��CO32-��+c��H2CO3����
�ʴ�Ϊ��c��OH-��+2c��CO32-��+c��HCO3-����c��HCO3-��+c��CO32-��+c��H2CO3����
���������
�����Ѷȣ�һ��