微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案
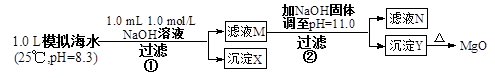
模拟海水中的
离子浓度(mol/L)
| Na+
| Mg2+
| Ca2+
| Cl―
| 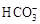
|
0.439
| 0.050
| 0.011
| 0.560
| 0.001
|
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;
实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;
Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12。
下列说法正确的是(?)
A.沉淀物X为CaCO3
B.滤液M中存在Mg2+,不存在Ca2+
C.滤液N中存在Mg2+、Ca2+?
D.步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
参考答案:A
本题解析:步骤①发生Ca2++OH-+ HCO3-="==" CaCO3↓+H2O;步骤②:Ksp[Mg(OH)2]=c(Mg2+)×(10-3)2=5.6×10-12,c(Mg2+)=5.6×10-6。Q[Ca(OH)2]=c(Ca2+)×(10-3)2=10-8<Ksp,无Ca(OH)2析出。A选项正确,生成0001 mol CaCO3。B选项错误,剩余c(Ca2+)=0.001 mol/L。C选项错误,c(Mg2+)=5.6×10-6<10-5,无剩余,D选项错误,生成0.05 mol Mg(OH)2,余0.005 mol OH-,Q[Ca(OH)2]=0.01×0.0052=2.5×10-7<Ksp,无Ca(OH)2析出。
本题难度:一般
2、选择题 下列叙述正确的是? ( )
A.一般认为沉淀离子浓度小于10-4 mol/L时,则认为已经沉淀完全
B.反应AgCl+NaBr=AgBr+NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水
C.Al(OH)3(s) Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3
Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3 Al3++3OH-表示水解平衡
Al3++3OH-表示水解平衡
D.只有反应速率很高的化学反应才能应用于工业生产
参考答案:B
本题解析:沉淀离子浓度小于10-5 mol/L时,则认为已沉淀完全,A项错误。Al (OH)3 Al3++3OH-表示Al(OH)3的电离平衡,C项错误;化学反应能否应用于工业生产与反应速率无必然联系。
Al3++3OH-表示Al(OH)3的电离平衡,C项错误;化学反应能否应用于工业生产与反应速率无必然联系。
本题难度:一般
3、填空题 (12分)实验室用氧化锌矿粉(主要含ZnO、FeCO3、CuO等)制备碱式碳酸锌[Zn2(OH)2CO3],并将其用于合成氨工艺脱硫研究。
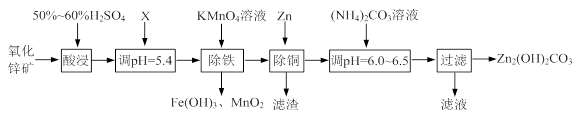
(1)“酸浸”时保持H2SO4过量的目的是 。
(2)已知:Mn2+开始沉淀的pH=8.1。
①写出加入KMnO4溶液除铁的离子方程式: 。
②流程中调节pH=5.4所加试剂X为 (填化学式);试剂X、KMnO4溶液加入顺序能否互换?请判断并说明理由 。
(3)上述流程中的“滤液”可以用作化肥,该滤液的主要成分为 (填化学式)。
(4)合成氨原料气脱硫原理如图,碱式碳酸锌吸收硫化氢的化学方程式为 。

参考答案:(1)提高矿石的浸出率(或防止Zn2+、Fe2+、Cu2+等金属离子水解)(答1点即给分)
(2)①3Fe2+ + MnO4-+7H2O=3Fe(OH)3↓ + MnO2 ↓+5H+(不配平扣1分)
②ZnO(或答碱式碳酸锌、碳酸锌、氢氧化锌、氨水等均给分)
不能,(1分)强酸性条件下KMnO4被还原成Mn2+,在除去Mn2+时,会使Zn2+同时沉淀(1分)
(3)(NH4)2SO4(多答碳酸氢铵等视而不见)
(4)Zn2(OH)2CO3 + 2H2S=2ZnS↓+CO2↑+3H2O(不配平扣1分)
本题解析:(1)“酸浸”时,硫酸与ZnO、FeCO3、CuO反应,生成硫酸盐等,溶液中存在金属阳离子,均会发生水解反应,所以酸浸时硫酸过量的目的是提高矿石的浸出率,防止Zn2+、Fe2+、Cu2+等金属离子水解;
(2)①由流程图可知,加入高锰酸钾除铁时,Fe元素以氢氧化铁的形式除去,同时生成二氧化锰,所以加入KMnO4溶液除铁的离子方程式是3Fe2+ + MnO4-+7H2O=3Fe(OH)3↓ + MnO2 ↓+5H+;
②最终的产物是碱式碳酸锌流程中调节pH=5.4所加试剂X既能除去过量的硫酸调节溶液的pH又不能引入新的杂质,所以X只能是ZnO或碱式碳酸锌、碳酸锌、氢氧化锌等;
试剂X与高锰酸钾不能互换,因为在酸性条件下,高锰酸根离子被还原为锰离子,而锰离子沉淀时的pH=8.1>5.4,此时Zn2+也会沉淀,所以不能互换;
(3)由流程图可知,除铜后的溶液中的溶质为硫酸锌,加入碳酸铵后,主要得到碱式碳酸锌和硫酸铵,硫酸铵可做化肥,所以滤液中的溶质是(NH4)2SO4;
(4)碱式碳酸锌吸收硫化氢后得到ZnS沉淀,同时又二氧化碳、水生成,过滤后可达到除硫的目的,所以碱式碳酸锌吸收硫化氢的化学方程式为Zn2(OH)2CO3 + 2H2S=2ZnS↓+CO2↑+3H2O。
考点:考查对工业流程的分析,物质性质的判断
本题难度:困难
4、选择题 下列说法中正确的是
[? ]
A.物质的溶解性为难溶,则该物质不溶于水
B.不溶于水的物质溶解度为0
C.某离子被沉淀完全是指该离子在溶液中的浓度为0
D.绝对不溶解的物质是不存在的
参考答案:D
本题解析:
本题难度:一般
5、选择题 一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=cm(An+)×cn(Bm-),称为难溶电解质的离子积.在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀.已知有关物质的颜色和溶度积如下:
| 物质 | AgCl | AgI | Ag2S
颜色
白
黄
黑
KSP(25℃)
1.8×10-10
1.5×10-16
1.8×10-50
|
下列叙述不正确的是( )
A.25℃时,饱和AgCl、AgI、Ag2S溶液中所含Ag+的浓度相同
B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生
C.溶度积小的沉淀可以转化为溶度积更小的沉淀
D.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2?溶液中的溶度积相同
参考答案:A.饱和AgCl、AgI、Ag2S溶液中Ag+的浓度分别为:
本题解析:
本题难度:简单