|
高考化学必考知识点《难溶电解质的溶解平衡》高频试题强化练习(2017年最新版)(八)
2017-08-06 09:15:44
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是( )
A.向饱和食盐水中加入少量的浓盐酸,看不到明显的现象
B.将硫酸铜溶液与碳酸钠溶液混合,得到的沉淀是以Cu(OH)2为主,说明了在相同条件下Cu(OH)2的溶解度比CuCO3的更小
C.在0.01 mol・L-1 NaCl溶液中加入少量的AgNO3溶液,有白色沉淀生成,接着向上述溶液中加入足量的浓氨水,白色沉淀不会溶解
D.CaCO3溶液的导电能力很弱,是因为CaCO3是弱电解质,存在如下电离平衡:CaCO3 Ca2++ CO32- Ca2++ CO32-
|
参考答案:B
本题解析:A项有NaCl晶体析出,A错误;C中AgCl(s) Ag+(aq)+Cl-(aq),加入浓氨水后生成[Ag(NH3)2]+,沉淀溶解平衡右移,白色沉淀会溶解,C错误;选项D中,溶液的导电性只与离子浓度和离子所带电荷有关,CaCO3溶液的导电能力很弱是因为CaCO3溶解度很小,但CaCO3是强电解质,D错误。 Ag+(aq)+Cl-(aq),加入浓氨水后生成[Ag(NH3)2]+,沉淀溶解平衡右移,白色沉淀会溶解,C错误;选项D中,溶液的导电性只与离子浓度和离子所带电荷有关,CaCO3溶液的导电能力很弱是因为CaCO3溶解度很小,但CaCO3是强电解质,D错误。
考点:难溶电解质的溶解平衡
本题难度:一般
2、选择题 将适量AgBr固体溶在水中,溶液中存在AgBr(s)  Ag+(aq)+Br-(aq)。则下列说法正确的是( ) Ag+(aq)+Br-(aq)。则下列说法正确的是( )
A.向此体系中滴加足量浓NaCl溶液,发现沉淀转化为白色,说明Ksp(AgCl)<Ksp(AgBr)
B.向此体系中加入少量AgBr固体,平衡正向移动,当再次平衡时c(Ag+)、c(Br-)增大
C.此体系中一定存在c(Ag+)=c(Br-)=[Ksp(AgBr)]1/2
D.某溶液中c(Ag+)・c(Br-)=Ksp(AgBr),说明此时c(Ag+)=c(Br-)
参考答案:C
本题解析:A项,转化成白色沉淀,不能说明Ksp(AgCl)<Ksp(AgBr),错误;B项,平衡不移动,且c(Ag+)、c(Br-)不变化;C项,根据Ksp(AgBr)=c(Ag+)・c(Br-)判断,正确;D项,当c(Ag+)・c(Br-)=Ksp(AgBr),说明此时正好形成AgBr的饱和溶液,错误。
本题难度:一般
3、填空题 在一定温度下,向AgI的饱和溶液中:(填“增大”、“减小”或“不变”)
(1)若加入AgNO3固体,c(I-)______.
(2)若加入更多的AgI固体,则c(Ag+)______.
(3)若加入固体AgBr,c(I-)______.
参考答案:在一定温度下,向AgI的饱和溶液中存在沉淀溶解平衡,AgI(s)?Ag+(aq)+I-(aq),平衡状态下存在溶度积常数,Ksp=C(Ag+)?C(I-);
(1)若加入AgNO3固体,会增加银离子浓度,沉淀溶解平衡AgI(s)?Ag+(aq)+I-(aq),左移,c(I-)减小,故答案为:减小;
(2)若加入更多的AgI固体,沉淀溶解平衡AgI(s)?Ag+(aq)+I-(aq),不变,则c(Ag+)不变,故答案为:不变;
(3)若加入固体AgBr,AgBr的溶解性大于AgI,所以平衡状态下AgBr溶液中的银离子浓度大于AgI溶液中的银离子浓度,所以碘化银沉淀溶解平衡左移,c(I-)减小,故答案为:减小;
本题解析:
本题难度:一般
4、选择题 下列说法中,正确的是
A.某离子被沉淀完全是指该离子在溶液中的浓度变为0
B.某物质的溶解性为难溶,则该物质的溶解度为0
C.一般来说,溶解度小的难溶物容易转化为溶解度大的难溶物
D.沉淀的生成、溶解和转化其实质都是沉淀发生了溶解平衡的移动
参考答案:D
本题解析:A、该离子在溶液中的浓度变为10-5mol/L可以认为离子被沉淀完全,错误;B、物质的不溶是相对的,错误;C、一般来说,溶解度大的难溶物容易转化为溶解度小的难溶物,错误;D、正确。
本题难度:一般
5、填空题 (12分)弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。根据要求回答问题
(1)生活中明矾常作净水剂,其净水的原理是 (用离子方程式表示)。
(2)常温下,取0.2 mol・L-1 HCl溶液与0.2 mol・L-1 MOH溶液等体积混合,测得混合溶液后的pH=5。写出MOH的电离方程式: 。
(3)0.1mol/L的NaHA溶液中,已知有关粒子浓度由大到小的顺序为:
c(Na+)>c(HA―)>c(H2A)>c(A2-)
①该溶液中c(H+) c(OH-)(填“>”、“<”或“=”)。
②作出上述判断的依据是 (用文字解释)。
(4)含Cr2O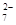 的废水毒性较大,某工厂废水中含5.0×10-3 mol・L-1的Cr2O 的废水毒性较大,某工厂废水中含5.0×10-3 mol・L-1的Cr2O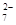 。为了使废水的排放达标,进行如下处理: 。为了使废水的排放达标,进行如下处理:
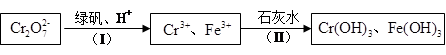
①绿矾化学式为FeSO4・7H2O。反应(I)的离子方程式为 。
②若处理后的废水中c(Cr3+)=3.0×10-6 mol・L-1,则废水中c(Fe3+)=" _________" mol・L-1。(Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH) 3]=6.0×10-31)
参考答案:(1)Al3+ + 3H2O  Al(OH)3 + 3H+(2分,写“=”和“↓”不得分) (2)MOH Al(OH)3 + 3H+(2分,写“=”和“↓”不得分) (2)MOH M+ + OH-(2分,写“=”不得分) (3)①< (2分,写“小于”不给分) ②NaHA溶液显碱性,说明HA-水解程度大于电离程度(2分)(4)①Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O(2分) ②2×10-13(2分) M+ + OH-(2分,写“=”不得分) (3)①< (2分,写“小于”不给分) ②NaHA溶液显碱性,说明HA-水解程度大于电离程度(2分)(4)①Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O(2分) ②2×10-13(2分)
本题解析:(1)生活中明矾常作净水剂,是因为明矾溶于水生成的 Al3+发生水解生成可Al(OH)3胶体能吸附水中的杂质,离子方程式为:Al3+ + 3H2O  Al(OH)3 + 3H+。(2)0.2 mol・L-1 HCl溶液与0.2 mol・L-1 MOH溶液等体积混合,测得混合溶液后的pH=5,说明MOH是弱碱,电离方程式为:MOH Al(OH)3 + 3H+。(2)0.2 mol・L-1 HCl溶液与0.2 mol・L-1 MOH溶液等体积混合,测得混合溶液后的pH=5,说明MOH是弱碱,电离方程式为:MOH M+ + OH-。(3)c(H2A)>c(A2-)说明HA―的水解程度大于电离程度,HA―水解溶液显碱性,则c(H+)<c(OH-)。(4)①Cr2O72-有强氧化性,Fe2+有还原性,发生氧化还原反应,离子方程式为:Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O。②Ksp[Cr(OH) 3]=c(Cr3+)×c3(OH-)=3.0×10-6×c3(OH-)=6.0×10-31,得c3(OH-)=2.0×10-25,Ksp[Fe(OH)3]= c(Fe3+) ×c3(OH-)=4.0×10-38, M+ + OH-。(3)c(H2A)>c(A2-)说明HA―的水解程度大于电离程度,HA―水解溶液显碱性,则c(H+)<c(OH-)。(4)①Cr2O72-有强氧化性,Fe2+有还原性,发生氧化还原反应,离子方程式为:Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O。②Ksp[Cr(OH) 3]=c(Cr3+)×c3(OH-)=3.0×10-6×c3(OH-)=6.0×10-31,得c3(OH-)=2.0×10-25,Ksp[Fe(OH)3]= c(Fe3+) ×c3(OH-)=4.0×10-38,
c(Fe3+) ×2.0×10-25=4.0×10-38,c(Fe3+)=2×10-13mol・L-1
考点:盐类的水解及其应用、溶度积的计算、离子方程式的书写。
本题难度:困难
|