微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:

请回答下列问题:
(1)步骤②中发生反应的离子方程式为 。
(2)步骤④中调节pH=6.0~6.5的目的是 。
(3)对MgSO4・7H2O晶体直接加热 (填“能”或“不能”)得到无水MgSO4固体。
(4)步骤⑤的操作为 。
(5)长时间加热MgCO3悬浊液后生成Mg(OH)2,该反应的化学方程式为
(6)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH
| < 8.0
| 8.0 ~ 9.6
| > 9.6
|
颜色
| 黄色
| 绿色
| 蓝色
|
25℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为 [25℃时,Mg(OH)2的溶度积Ksp=5.6×10-12]。
(7)药品A是中和胃酸的常用药物,其有效成分是铝和镁的碱式碳酸盐。现进行如下实验确定其化学式:
实验一:取该碱式碳酸盐3.01g充分灼烧至恒重,测得固体质量减少了1.30g;
实验二:另取该碱式碳酸盐3.01g使其溶于足量的盐酸中,产生CO2的体积为112mL(标准状况);
实验三:向实验二的溶液中加入足量的NaOH溶液得到1.74g白色沉淀。
该药品的化学式为 。
参考答案:(每空2分,共14分)
(1)2NH4+MgO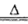 Mg2++2NH3↑+H2O
Mg2++2NH3↑+H2O
(2)抑制Mg2+水解,以便得到较纯的产品
(3)能
(4)蒸发浓缩、冷却结晶
(5)MgCO3+H2O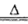 Mg(OH)2+CO2↑
Mg(OH)2+CO2↑
(6)蓝色
(7)Al2Mg6(OH)16CO3・4H2O
本题解析:(1)根据流程图可知,硫酸铵与MgO加热产生的气体可与硫酸反应有生成硫酸铵,所以该气体为氨气,所以MgO与铵根离子水解生成的氢离子反应,促进铵根离子的水解,家入围生成氨气,则硫酸铵与MgO在加热条件下反应生成氨气和镁离子、水,离子方程式是2NH4+MgO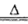 Mg2++2NH3↑+H2O;
Mg2++2NH3↑+H2O;
(2)得到的溶液为硫酸镁溶液,因为镁离子水解,生成氢氧化镁和硫酸,所以调节溶液的pHpH=6.0~6.5的目的是抑制Mg2+水解,以便得到较纯的产品;
(3)虽然镁离子水解生成氢氧化镁和硫酸,但硫酸是高沸点酸,不易挥发,则水解不会进行彻底,所以加热硫酸镁晶体能得到无水MgSO4固体;
(4)从溶液中得到晶体的操作为蒸发浓缩、冷却结晶,过滤,所以步骤⑤的操作为蒸发浓缩、冷却结晶;
(5)长时间加热MgCO3悬浊液后生成Mg(OH)2,同时有二氧化碳生成,化学方程式是MgCO3+H2O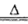 Mg(OH)2+CO2↑;
Mg(OH)2+CO2↑;
(6)25℃时,Mg(OH)2的溶度积Ksp=5.6×10-12,设氢氧化镁的饱和溶液中氢氧根离子的浓度为x,则5.6×10-12=0.5x×x2,x近似为10-4mol/L,氢氧化镁的饱和溶液的pH近似等于10,所以25℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为蓝色;
(7)根据实验一可知该碱式碳酸盐3.01g充分灼烧至恒重,生成水和二氧化碳的总质量是1.30g,根据实验二可知,生成的二氧化碳的物质的量是0.112L/22.4L/mol=0.005mol,其质量是0.005mol×44g/mol=0.22g,则水的质量是1.30g-0.22g=1.08g,则水的物质的量是1.08g/18g/mol=0.06mol;根据实验三可知,生成的氢氧化镁的质量是1.74g/mol,则3.01g固体中MgO的物质的量是1.74g/58g/mol=0.03mol,所以氧化铝的质量是(3.01-1.30-0.03mol×40g/mol)g=0.51g,所以Al2O3的物质的量是0.51g/102g/mol=0.005mol,则该药品中Al2O3:MgO:H2O:CO2=0.005:0.03:0.06:0.005=1:6:12:1,所以该药品的化学式是Al2Mg6(OH)16CO3・4H2O。
考点:考查对流程图的分析,基本操作的判断,物质化学式的计算
本题难度:困难
2、填空题 在室温下,下列五种溶液①0.1mol/LNH4Cl ②0.1mol/LCH3COONH4 ③ 0.1mol/ L NH4HSO4 ④0.1mol/LNH3・H2O和0.1mol/LNH4Cl的混合溶液 ⑤0.1mol/LNH
0.1mol/ L NH4HSO4 ④0.1mol/LNH3・H2O和0.1mol/LNH4Cl的混合溶液 ⑤0.1mol/LNH 3・H2O
3・H2O
(1)溶液①呈___性(填“酸”“碱”或“中”)其原因是____________________________(用离子方程式表示)
(2 )比较溶液②、③中C(NH4+)的大小关系是____________________(填>,<或=)
)比较溶液②、③中C(NH4+)的大小关系是____________________(填>,<或=)
(3)在溶液④中,_____________离子的浓度为0.1mol/L
NH3・H2O和_________离子的物质的量浓度之和为0.2mol/L
(4) 室温下测得溶液②的PH=7,则说明CH3COO-的水解程度_______(填>,<或=")" NH4+的水解程度,C(CH3COO-)_________C(NH4+)(填>,<或=)
参考答案:1)酸 , NH4++H2O N
N H3・H2O+H+ ,N
H3・H2O+H+ ,N H4+和水电离出来
H4+和水电离出来 的结合成NH3
的结合成NH3 ・H
・H 2O,促进水
2O,促进水 的电离,平衡时使C(H+)
的电离,平衡时使C(H+) >C(OH-),所以溶液呈酸性。(2)②<③ (3)Cl- , NH4+ (4) =" " ,
>C(OH-),所以溶液呈酸性。(2)②<③ (3)Cl- , NH4+ (4) =" " , =
=
本题解析:略
本题难度:困难
3、填空题 (16分)氮元素的化合物应用十分广泛。请回答:
(1)火箭燃料液态偏二甲肼(C2H8N2)是用液态N2O4作氧化剂,二者反应放出大量的热,生成无毒、无污染的气体和水。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,则该反应的热化学方程式为 。
(2)298 K时,在2L固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g)ΔH=-a kJ・mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
N2O4(g)ΔH=-a kJ・mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
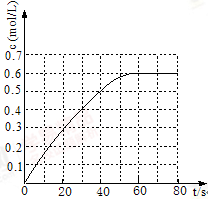
①298k时,该反应的平衡常数为 L ・mol-1(精确到0.01)。
②下列情况不是处于平衡状态的是 :
A.混合气体的密度保持不变; B.混合气体的颜色不再变化; C.气压恒定时。
③若反应在398K进行,某时刻测得n(NO2)="0.6" mol n(N2O4)=1.2mol,则此时V(正) V(逆)(填“>”、“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol・L-1NH4HSO4溶液中滴加0.1 mol・L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
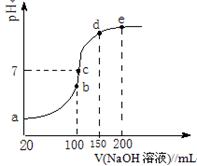
试分析图中a、b、c、d、e五个点,
①b点时,溶液中发生水解反应的离子是______;
②在c点,溶液中各离子浓度由大到小的排列顺序是 。
参考答案:(16分)(1)C2H8N2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(l) ΔH=-2550 kJ/mol(3分)
(2)(7分)①6.67 (3分) ②A(2分) ③< (2分)
(3)(6分)①NH4+(3分) ②c(Na+)>c(SO)>c(NH)>c(OH-)=c(H+)(3分)
本题解析:(1)根据题意可得热化学方程式:C2H8N2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(l) ΔH=-2550 kJ/mol;①根据图像和题意可知,在298k时,该反应达到平衡时,c(N2O4)="0.6mol/L," c(NO2)=0.3mol/L,所以该反应的平衡常数为K= L /mol; ②A.由于反应是在恒容的密闭容器内减小的,所以在任何时刻都存在混合气体的密度保持不变,一般不能判断反应达到平衡状态,错误; B.由于容器的容积不变,若混合气体的颜色不再变化,说明物质的浓度不变,反应达到平衡状态,正确; C.该反应的气体体积减小的反应,若未达到平衡状态,则气体的压强就会发生变化,因此气压恒定时,则反应处于平衡状态,正确。故选项是A;③若反应在298K进行,某时刻测得n(NO2)="0.6" mol n(N2O4)=1.2mol,则由于物质的浓度不变,但是该反应的正反应是放热反应,根据平衡移动原理:升高温度,平衡向吸热反应方向移动,即平衡逆向移动所以V(正)<V(逆);(3)①NH4HSO4是强酸弱碱盐,弱碱阳离子NH4+水解消耗水电离产生的OH-,使溶液显酸性,而且NH4HSO4是强酸的酸式盐,电离也产生H+,使溶液显酸性。b点时,溶液中发生水解反应的离子是NH4+;②在c点时溶液呈中性,c(OH-)=c(H+),n(Na+)=0.015mol;n(SO)=0.01mol,由于NH4+会发生水解反应而消耗,所以n(NH4+)< 0.01mol,因为溶液的体积是相同的,所以微粒的物质的量越多,离子浓度就越大,因此c(Na+)> c(SO)>c(NH),在溶液中水电离程度很小,所以c(OH-)、c(H+)都很小,远小于盐电离产生的离子浓度,因此溶液中各离子浓度由大到小的排列顺序是c(Na+)>c(SO)>c(NH)>c(OH-)=c(H+)。
L /mol; ②A.由于反应是在恒容的密闭容器内减小的,所以在任何时刻都存在混合气体的密度保持不变,一般不能判断反应达到平衡状态,错误; B.由于容器的容积不变,若混合气体的颜色不再变化,说明物质的浓度不变,反应达到平衡状态,正确; C.该反应的气体体积减小的反应,若未达到平衡状态,则气体的压强就会发生变化,因此气压恒定时,则反应处于平衡状态,正确。故选项是A;③若反应在298K进行,某时刻测得n(NO2)="0.6" mol n(N2O4)=1.2mol,则由于物质的浓度不变,但是该反应的正反应是放热反应,根据平衡移动原理:升高温度,平衡向吸热反应方向移动,即平衡逆向移动所以V(正)<V(逆);(3)①NH4HSO4是强酸弱碱盐,弱碱阳离子NH4+水解消耗水电离产生的OH-,使溶液显酸性,而且NH4HSO4是强酸的酸式盐,电离也产生H+,使溶液显酸性。b点时,溶液中发生水解反应的离子是NH4+;②在c点时溶液呈中性,c(OH-)=c(H+),n(Na+)=0.015mol;n(SO)=0.01mol,由于NH4+会发生水解反应而消耗,所以n(NH4+)< 0.01mol,因为溶液的体积是相同的,所以微粒的物质的量越多,离子浓度就越大,因此c(Na+)> c(SO)>c(NH),在溶液中水电离程度很小,所以c(OH-)、c(H+)都很小,远小于盐电离产生的离子浓度,因此溶液中各离子浓度由大到小的排列顺序是c(Na+)>c(SO)>c(NH)>c(OH-)=c(H+)。
考点:考查热化学方程式的书写、化学平衡状态的判断、化学平衡常数的计算、温度对化学平衡移动的影响、盐的水解、溶液中离子浓度的大小比较的知识。
本题难度:一般
4、选择题 下列叙述错误的是
A.在加热搅拌条件下加入MgO,可除去MgCl2溶液中的Fe3+
B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍
C.常温下,CH3COONa和CH3COOH的混合溶液中(pH=7):c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
D.常温下,Cd(OH)2和Co(OH)2的混合悬浊液中,c(Cd2+)是c(Co2+)的3.5倍。已知:KSP(Cd(OH)2)=7.2×10-15, KSP(Co(OH)2)=1.8×10-15