微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 工业上常用铁质容器盛装冷浓酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移人硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是______________________。
(2)另称取铁钉6.0g放入15.0ml.浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中的Fe2+,应先用__________(选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性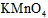 溶液
溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应: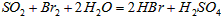
?然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中SO2的体积分数为
____________。
[探究二] 分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。

(3)装置B中试剂的作用是_____________。
(4)认为气体Y中还含有Q的理由是_____________(用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于_____________(选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验现象应是_____________。
(7)若要测定限定体积气体Y中H2的含量(标准状况下约有28ml H2),除可用测量H2体积的方法外,可否选用质量称量的方法?做出判断并说明理由___________________________。
参考答案:(1)铁钉表面被钝化
(2)①d;②66.7%
(3)检验SO2是否除尽
(4)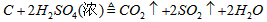
(5)c
(6)D中固体由黑变红和E中固体由白变蓝
(7)否,用托盘天平无法称量D或E的差量(或:可,用分析天平称量D或E的差量)
本题解析:
本题难度:困难
2、选择题 下列实验目的可以达到的是
A.电解熔融氯化镁制取金属镁
B.醋酸钠结晶水合物与碱石灰共热制取甲烷。
C.浓硫酸与溴化钠共热制取溴化氢
D.饱和碳酸钠溶液除去二氧化碳中的氯化氢
参考答案:A
本题解析:略
本题难度:一般
3、实验题 ?(16分)某化学研究小组为证明CO具有还原性,首先查阅相关资料,获取下列信息:
①? ;
;
②CO和H2都可在加热条件下与CuO反应;
③CO有剧毒,在空气 中可以燃烧。
中可以燃烧。
根据以上信息和有关知识,他们设计了如图所示的实验装置。
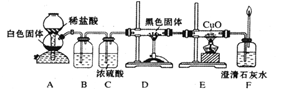
试回答下列问题:
(1)装置A中反应的离子方程式是______________?。
(2)装置B.中最适宜的试剂是_______;必须用装 置C吸收气体中水蒸气的理由是_
置C吸收气体中水蒸气的理由是_ ______。
______。
(3)按照如图装置进行实验时,首先应进行的操作是检查气密性,并要排净整套装置中的空气,则排净装置中空气的必要性是______ ?
(4)?根据该实验中的_______现象,可证明CO具有还原性,有关反应的化学方程式为______________。
(5)?若要根据装置F中石灰水变浑浊的现象确认CO具有还原性,则应在上图装置_______与_______之间连接右图中的_______装置(填序号)。
参考答案:(16分)(1) CaCO3 + 2H+ = Ca2+ +H2O + CO2?↑(2分)
(2)饱和碳酸氢钠溶液(2分)?防止水蒸气与碳反应生成的氢气对实验现象产生干扰(2分)
(3)防止空气中的氧气对实验现象及结果产生干扰(2分)
(4)E装置中黑色CuO变成红色(2分)?CuO+CO?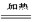 Cu+CO2(2分)
Cu+CO2(2分)
(5)D E (2分)?④(2分)
本题解析:略
本题难度:一般
4、选择题 限用下列一种试剂鉴别氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,这种试剂是( )
A.KSCN
B.HCl
C.BaCl2
D.NaOH
参考答案:取五种溶液分别滴加NaOH溶液时,产生白色沉淀的是氯化镁;先产生沉淀,后沉淀溶解的是氯化铝;产生红褐色沉淀的是氯化铁;产生白色沉淀,后又变灰绿色,最后变成红褐色的是氯化亚铁;无现象的是氯化钠,而加入KSCN只能检验氯化铁,加入盐酸和氯化钡不能检验任何物质,
故选D.
本题解析:
本题难度:一般
5、实验题 过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,请填写下列空白:
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250mL?(填仪器名称)中,加水衡释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
??MnO4-+??H2O2+??H+=?Mn2++??H2O+□
(3)滴定时,将高锰酸钾标准溶液注入?(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是?。
(4)重 复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为?。
复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为?。
(5)下列操作能使测定结果偏高的是?
A.滴定前滴定管尖嘴中有气泡,滴定后气泡消失。
B.读取高锰酸钾标准溶液的刻度时,滴定前平视,滴定后俯视。
C.滴定前,在用蒸馏水洗涤滴定管后,未用高锰酸钾标准液润洗。
D.滴定过程中,锥形瓶中部分溶液溅出
参考答案:

本题解析:略
本题难度:一般