��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ԭ��صķ�Ӧԭ���ǣ�������
A���������
B��������ԭ��Ӧ
C�����ϼ�����
D����ѧ��ת��Ϊ����
�ο��𰸣�ԭ��ؿɽ���ѧ��ת��Ϊ���ܣ���Ӧԭ��Ϊ������ԭ��Ӧ������ʱ����������������Ӧ������������ԭ��Ӧ��
��ѡB��
���������
�����Ѷȣ���
2��ѡ���� ���й���ͭ-п-ϡ���ṹ�ɵ�ԭ��ص��й��������������
[? ]
A��п��������п����������Ӧ
B��ͭ��������ͭ����ʧȥ���Ӷ��ܵ�����
C������������ԭ��Ӧ����������������Ӧ
D�����·���������һ��Ϊ����������������һ��Ϊ����
�ο��𰸣�C
���������
�����Ѷȣ���
3������� Ǧ�����ǵ��͵Ŀɳ��͵�أ���������������Ƕ��Բ��ϣ�����ܷ�ӦʽΪ��
Pb��PbO2��4H����2SO42��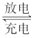 2PbSO4��2H2O ��ش���������(�������⡢����������ԭ)��
2PbSO4��2H2O ��ش���������(�������⡢����������ԭ)��
(1)�ŵ�ʱ�������ĵ缫��Ӧʽ��________________�����Һ��H2SO4��Ũ�Ƚ���________�������·ͨ��1?mol����ʱ�������ϸ��������������________g.
(2)����ȫ�ŵ�ľ�PbO2��Pbʱ��������ͼ���ӣ����һ��ʱ�������A�缫������________��B�缫������________����ʱǦ���ص��������ļ��Խ�________��
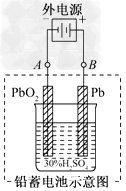
�ο��𰸣�(1)PbO2��2e����4H����SO42��===PbSO4��2H2O��С��48
(2)Pb��PbO2���Ի�
���������
�����Ѷȣ�һ��
4��ѡ���� ������������ս����������ʡ������ѧ��ͬ���Ƴɹ�������DZ������þ����������ȼ�ϵ��ϵͳ���乤��ԭ����ͼ��ʾ������˵���д������?
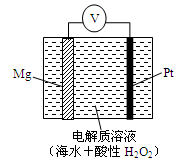
A����صĸ�����ӦΪ��Mg �C 2e��= Mg2��
B����ص����������Ļ�ԭ������ˮ
C����ع���ʱ��H�����ƶ�
D����ع���һ��ʱ�����Һ��pH����
�ο��𰸣�C
���������A����ȼ�ϵ���У�þ��������������þʧ���ӷ���������Ӧ���缫��ӦʽΪ��Mg-2e-=Mg2+����ȷ��B������������������˫��ˮ�õ��ӷ�����ԭ��Ӧ������ˮ����ȷ��C��ԭ��طŵ�ʱ���������Һ���������������ƶ��������������������ƶ�������D��ԭ���������˫��ˮ�õ��ӽ��H+����ˮ����Һ��������Ũ�Ƚ��ͣ�������Һ��pH������ȷ����ѡC��
�����Ѷȣ�һ��
5������� ��12�֣���Ⱦ�����Чȥ������Դ�ij�������ǻ�ѧ�츣�������Ҫ�о����⡣ij�о�С���������̿���Ҫ�ɷ�ΪMnO2��������������������ͭ�����Ƚ�����������������ͨ���������̼��ѳ�ȼúβ���е�SO2�����Ƶõ�ز���MnO2����Ӧ������ʡ�ԣ���
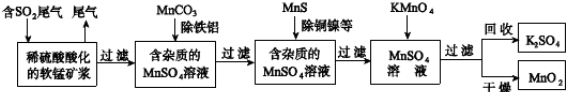
��ش��������⣺
��1��������������ʵ���� ��ѡ��������ĸ��ţ���
A����������ۺ����� B����ɫ��Ⱦ�ļ��� C������ļ���
��2�����˲����õ��IJ��������У� ��
��3����MnCO3�ܳ�ȥ��Һ��Al3+��Fe3+����ԭ���� ��
��4��д��KMnO4��Һ���뵽MnSO4��Һ���Ʊ�MnO2�����ӷ�Ӧ����ʽ�� ���ö��Ե缫���MnSO4��ҺҲ���Ƶ�MnO2���������ĵ缫��Ӧʽ�� ��
��5��MnO2�Ǽ���п�̵�صĵ缫���ϣ���ط�Ӧ����ʽΪ��2MnO2+Zn+H2O====2MnOOH+Zn(OH)2,д���õ�طŵ�ʱ�������ĵ缫��Ӧʽ�� ��
�ο��𰸣���1��A��C��2���ձ���©����������
��3��������Һ�е��ᣬ�ٽ�Al3+��Fe3+ˮ�����������������
��4��3Mn2++2 MnO4- +2H2O ====5MnO2+4H+ Mn2++2H2O-2e-====MnO2+4H+
��5��MnO2+H2O+e-====MnOOH+OH-
�����������1����ɫ��Ⱦ��Ҫ�����ϵ��ѽ���������γɵģ�SO2���γ����꣬�������ʵ���˷�������ۺ����ã�ͬʱҲ�����������γɣ�����ѡAC����2������̼������������Һ�е��ᣬ������Һ�����ԣ��Ӷ��ٽ�Al3����Fe3��ˮ���������������������3����֪���Ȼ�ѧ����ʽ��Mn(s)��O2(g)��MnO2(s) ��H����520kJ/mol����S(s)��O2(g)��SO2(g) ��H����297kJ/mol����Mn(s)��S(s)��2O2(g)��MnSO4(s) ��H����1065kJ/mol������ݸ�˹���ɿ�֪�ۣ����٣��ۣ����õ�SO2��MnO2��Ӧ������ˮMnSO4���Ȼ�ѧ����ʽMnO2(s)��SO2(g) =MnSO4(s) ��H=-248kJ/mol����4������������ʧȥ���ӷ���������Ӧ�����ö��Ե缫���MnSO4��Һ���Ƶ�MnO2����������������ӷŵ磬�������缫��Ӧʽ��Mn2����2H2O��2e����MnO2��4H������5��ԭ����и���ʧȥ���ӣ������õ����ӣ���˼���п�̵�طŵ�ʱ�������Ƕ������̵õ����ӣ���缫��Ӧʽ��MnO2��H2O��e����MnO(OH)��OH������6��ʵ�ʲμӷ�Ӧ��SO2�����ʵ�����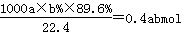 �����ݷ���ʽMnO2(s)��SO2(g) =MnSO4(s)��֪��������þ�����ʵ�����0.4abmol���������ɶ���������c kg������ݷ���ʽ3MnSO4��2KMnO4��2H2O=5MnO2��K2SO4��2H2SO4��֪��������������̵����ʵ�����
�����ݷ���ʽMnO2(s)��SO2(g) =MnSO4(s)��֪��������þ�����ʵ�����0.4abmol���������ɶ���������c kg������ݷ���ʽ3MnSO4��2KMnO4��2H2O=5MnO2��K2SO4��2H2SO4��֪��������������̵����ʵ�����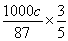 mol�����ȥ��������ͭ����������ʱ�����������Ԫ�ص����ʵ�����
mol�����ȥ��������ͭ����������ʱ�����������Ԫ�ص����ʵ�����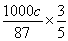 mol��0.4abmol���൱�ڶ������̵������ǣ�
mol��0.4abmol���൱�ڶ������̵������ǣ�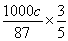 mol��0.4abmol����87g/mol����600c��34.8ab��g��
mol��0.4abmol����87g/mol����600c��34.8ab��g��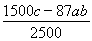 kg
kg
���㣺���������Ʊ��������̵��й��ж������
�����Ѷȣ�����