��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� �ڽ���ijʵ��̽�������У�һЩѧ�����ֵ�������ͭƬ�ֱ�������������������Ũ�����ϡ���ᷴӦ��������Һǰ��Ϊ��ɫ������Ϊ��ɫ��
�����������ѧ���ǽ��������ۺ������������ֹ۵㣺
һ����Ϊ���������Cu2+Ũ�ȵIJ�������ġ���ͬ�����ֿ�����??(�ͬ�⡱��ͬ�⡱)��ԭ����?��
��һ����Ϊ���ʡ���ɫ����Cu2+��NO2��ϵĽ����������Ƴ�һ��ʵ�鷽��֤��֮������Ƶ�ʵ�鷽����??
��֪0.3mol Cu��������ϡ���ᷴӦ����ԭ��HNO3�����ʵ�����?mol��
�ο��𰸣���ͬ�⣨1�֣�?Ũ���ᡢϡ�����������Cuȫ��ת��ΪCu2+������ͬ�������Һ��Cu2+Ũ����ͬ����Һ��ɫӦ����ͬ��2�֣�
��ˮϡ�Ϳ��ܷ�����ɫ��Ϊ��ɫ��2�֣����������𰸾��ɣ�
0.2mol��2�֣�
�������������Һ����ɫ����ɫ���ӵ�Ũ������������Cu2+Ũ����ͬ����ɫӦ����ͬ���ʴ�Ϊ����ͬ�⣻ Ũ���ᡢϡ�����������Cuȫ��ת��ΪCu2+������ͬ�������Һ��Cu2+Ũ����ͬ����Һ��ɫӦ����ͬ��
���ȥNO2����ɫ��������������Cu2+��NO2��ϵĽ�����ʴ�Ϊ����ˮϡ�Ϳ��ܷ�����ɫ��Ϊ��ɫ��
Cu��������ϡ���ᷴӦ��3Cu+8HNO3===3Cu(NO3)2+2NO��+4H2O�����������ʽ�����ǿ���֪����2mol���ᱻ��ԭ��NO���μӷ�Ӧ�������뱻��ԭ����������ʵ���֮����4��1����0.3molCu��0.8molHNO3��ȫ��Ӧ�������������ʵ���Ϊ0.8mol����ԭ��HNO3���ʵ�����0.2mol��
������������Ҫ������ͭ������ķ�Ӧ�����������龰��������ѧ֪ʶ��������⣬������ѧ�������������������������Ŀ�Ѷ��еȡ�
�����Ѷȣ�һ��
2��ʵ���� (9��)������ʵ��С���ͬѧ̽��һ����̼������������������Ƶķ�Ӧ����ش��������⣺
(1)��һС��ͬѧ�����ͼװ�ý���ʵ�顣ͨ��SO2���壬���������ľ�������Թ�C�У�ľ����ȼ��

��ͬѧ��ΪNa2O2��SO2��Ӧ������Na2SO3��O2����Ӧ�Ļ�ѧ����ʽΪ___________________________��
��ͬѧ��ΪNa2O����SO2��Ӧ��������Na2SO3��O2�⣬����Na2SO4���ɡ�Ϊ�����Ƿ���Na2SO4���ɣ���ͬѧ��������·�����

����Ϊ��ͬѧ�ķ����Ƿ����____________(���ǡ���)�����Ҫ˵���������ɣ�
��__________________________________________________________________________
��__________________________________________________________________________.
(2)�ڶ�С��ͬѧ������ͼ�е��й�װ��(�̶�װ�ü�������ȥ)��֤CO�����ܷ���Na2O2��Ӧ����֪��H2C2O4  ?CO2��+CO��+H2O
?CO2��+CO��+H2O
(�Ҷ���)?

��CO�ܹ���Na2O2������Ӧ����Ԥ�ⷴӦ����Ϊ______________________����֤�ò����ѡ����Լ���___________________________________________________��
����ʵ����ѡ������װ�ýӿ�����˳��Ϊ_________________________.
�ο��𰸣���1�� ����1�֣�
����1�֣�
��ϡHNO3����BaSO3����ΪBaSO4��1�֣�
������Ӧ��Ĺ�����Na2O2����������ˮ��ɰ�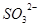 ����Ϊ
����Ϊ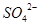 ��1�֣�
��1�֣�
��2��Na2CO3��1�֣���ϡ ����ϡHC1���ͳ���ʯ��ˮ��1�֣���a b c f��2�֣�
����ϡHC1���ͳ���ʯ��ˮ��1�֣���a b c f��2�֣�
���������(1)����CO2��������Ƶķ�Ӧ����ʽ��д����ֱ����ƽ��
��2�������Ǽ���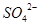 �Ĵ��ڣ��÷������Բ�������
�Ĵ��ڣ��÷������Բ�������
��ԭ��Һ�м�ʹû��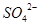 ����
����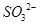 �������Ȼ�����Һ�γɵ�BaSO3�ɱ�ϡHNO3����ΪBaSO4
�������Ȼ�����Һ�γɵ�BaSO3�ɱ�ϡHNO3����ΪBaSO4
������Ӧ��Ĺ�����Na2O2����������ˮ��ɰ�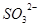 ����Ϊ
����Ϊ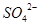 ������Ҳ���Եõ�ͬ��������
������Ҳ���Եõ�ͬ��������
��ȷ�ļ�������ǣ��ȼ���������ᣬ�ټ����Ȼ�����Һ������а�ɫ�������ɣ����֤����Na2SO4����
(2)CO��Na2O2������Na2O2+CO=Na2CO3
Na2CO3����̼���Σ����������䷴Ӧ����CO2����ͨ�����ʯ��ˮ�У����Ƿ��л��dz��֣�
����H2C2O4  ?CO2��+CO��+H2O��������CO�к���CO2����Ӧ���ü�Һ����CO2����װ�ýӿڵ�����˳��Ϊ��a b c f
?CO2��+CO��+H2O��������CO�к���CO2����Ӧ���ü�Һ����CO2����װ�ýӿڵ�����˳��Ϊ��a b c f
�����Ѷȣ�һ��
3��ʵ���� �� NH4Cl��������ʵ�飬���жϷ�����������˵��ԭ��
(1) �ò�����պȡ���� NH4Cl��Һ��pH��ֽ�Ӵ�ʱ����ֽ��ʾ����ɫ�����ɫ����ȣ��ɷ��� NH4Cl��Һ��pH ?7(�<������=����>��������?�ԣ���ᡱ��������С�������ԭ��������ӷ���ʽ��ʾΪ?��
(2)��NH4Cl��Һ�м���þ�ۣ��ɹ۲쵽���������ɣ�����Ҫ�ɷ�Ϊ?��
(3) 25��ʱ����0.1mol/L�İ�ˮ�м��������Ȼ�粒��壬�������ܽ�����ҺpH��С����Ҫԭ���ǣ�����ţ�?��
A����ˮ���Ȼ�立�����ѧ��Ӧ? B���Ȼ����Һˮ�������ԣ�������c(H+)
C���Ȼ������ˮ���������������ӣ������˰�ˮ�ĵ��룬ʹc(OH�D)��С
�ο��𰸣���1����?��? NH4++H2O NH3��H2O+H+
NH3��H2O+H+
��1��H2?��3��C
�����������1��NH4Cl��ǿ�������Σ�NH4��ˮ�������ԣ�����ʽΪNH4++H2O NH3��H2O+H+��
NH3��H2O+H+��
��2���Ȼ�������ԣ������ܺ�þ��Ӧ����������
��3����ˮ�д��ڵ���ƽ��NH3��H2O NH4����OH�������������Ȼ�粒��壬����NH4��Ũ�ȣ����ư�ˮ�ĵ��룬���Լ��Խ��ͣ�pH��С����ѡC��
NH4����OH�������������Ȼ�粒��壬����NH4��Ũ�ȣ����ư�ˮ�ĵ��룬���Լ��Խ��ͣ�pH��С����ѡC��
�����Ѷȣ�һ��
4��ʵ���� ��18�֣���ѧ̽�������ȷ��������̽������о������Ŀ�ѧ�ԣ��о����̵ļƻ��ԡ��о�Ŀ����ȷ�ԡ�
��һ��ѧ�����ף�Ӧ����ͼװ�ã�A����ʾ��ķ����о����������ʣ������������Ҫ�ɷ������������п�����ˮ����������ش��������⣺

��1�������о�(ʵ��)����ҪĿ����?
��2��Ũ�����������?�����о�Ŀ��ֱ����ص�ʵ��������? ________________? _?��
��3������е�װ��Ӧѡ��??���B����C��������ʢ�ŵ��Լ�
Ϊ??�����Լ����ƣ���ʹ�ø�װ�õ�Ŀ����?����װ���ڷ�����Ӧ�Ļ�ѧ����ʽΪ??��
������ѧ�����ң����ʵ��̽����������������Ĥ�����ʣ�����Ƭ��������Ĥ��Ͷ��Ũ�Ȼ�ͭ��Һ�У�������ܿ����һ�㺣��״����ɫ���ʡ�����ͬ������ƬͶ��ͬŨ�ȵ�����ͭ��Һ�У��ڶ�ʱ������Ƭ�����Ա仯���ش��������⣺
��1����Ƭ������ֵİ���ɫ���ʵĹ����з��������ӷ�Ӧ����ʽ��?��
��2��ͬѧ���ң���Ϊ�������Ȼ�ͭ��Һ��Ѹ�ٷ�Ӧ������ͬŨ�ȵ�����ͭ��Һ�ڶ�ʱ���ڲ���Ӧ��ԭ���ǡ����������ƻ����������污Ĥ,����������Ӳ��ܡ������������ʵ�鷽��������֤�����������˼·������пո�
[ʵ�鷽��] ������ͭ��Һ�м�����Ƭ�������������ټ���?�����Լ����ƣ�������Ӧ���Լӿ��ˣ�˵�������ƶ���ȷ��
�ο��𰸣���18�֣���һ��
��1���Ƚϸ���������ͳ�ʪ��������Ư���ԣ����о�������Ư����ʵ��Ⱥ����𰸾��ɣ���2�֣�
��2�����������е�ˮ���������ɫ��������ɫ��ʪ�����ɫ������ɫ�������𰸾��ɣ�
������2�֣���4�֣�
��3��B?��NaOH��Һ����ֹ�ж���Cl2��Ⱦ������2NaOH + Cl2 ="=" NaCl + NaClO+ H2O ������2�֣���8�֣�
��������1��2Al+3Cu2+��3Cu+2Al3+;��2�֣�
��2���Ȼ��ƣ������������2�֣�
���������ͨ��ʵ�������̽�����о���Ӧԭ�������ʵ�����
(һ)��1������ˮ��������������ͨ��Ũ���ᣬ�õ��������������������ֱ�����ʪ�����ɫ�����Ӵ����������ǶԱ�ʵ�飬�Ƚϸ���ġ���ʪ��������Ư���Բ���
��2��Ũ�������������е�ˮ����Ȼ���¸������ɫ�����ޱ仯������ʪ�����ɫ���������ɴ����ᣬ���յ�������ɫ
��3�����������ж�������ֱ���ŷŵ������У���Cװ���Ǹ��ܷ�װ�ã�����ȷ����Ӧѡ��Bװ�ã������ɱ���Һ����2NaOH + Cl2 ="=" NaCl + NaClO+ H2O
��������1����ɫ���ʱ��������û�����ͭ���ʣ�2Al+3Cu2+��3Cu+2Al3+
��2��ʵ����������Һ���ʵIJ������ν���������ӵIJ�ͬ�������˷�Ӧ����IJ�ͬ���ʿ�������ͭ��Һ�м�����Ƭ��������������ټ��뺬����������Һ���ɣ�Ϊ�˲��ı���Һ������ԣ���ü����Ȼ�����Һ���ٹ۲�����
�����Ѷȣ�һ��
5��ʵ���� (12��) �ס��ҡ���������λͬѧ��̽������Һ���̪���õ�ʵ��ʱ��������һ��������������������Һ�����̪��Һ����Һ����˺�ɫ�����ǹ���һ�����ɫ����ʧ�ˡ�
[����]
�ף������Ƿ�̪������ɵģ�
�ң�����������������Һ������еĶ�����̼��Ӧ��Ե�ʣ�
���������Ƿ�̪������е�������Ӧ��ʹ��ɫ��ʧ��
��������������������ҺŨ�ȴ�С�йء�
[���۷���]
��1����ͬѧ������Լ��IJ��룬���������λͬѧ�ķ���λͬѧ�������ǣ�?
?��
��2����ͬѧ��Ϊ��ͬѧ�IJ���Ҳ����ȷ������������?
?��
[ʵ�����]
��3��Ϊ֤ʵ��ͬѧ�IJ��룬����������ʵ�飬������±���
ʵ�鲽��
| �����һ�����Ŀ��
|
1�������Ƶ�����������Һ����??
| ?
|
2���ڼ��Ⱥ����Һ�е����̪�������Ϸ���һЩֲ����?
| ?
|
��4��ͨ������ʵ�飬��λͬѧ�۲쵽�������ǣ���Һ�ȱ�ɺ�ɫ������һ�����ɫ��Ȼ��ʧ����˷�̪��ɫ��ȥ�������ء�����ͬѧ�IJ�����ȷ����������ʵ��֤����
ʵ�鷽��
| ���ܹ۲쵽������ͽ���
|
����һ���ֱ����Ʋ�ͬ���ʵ���Ũ�ȵ�����������Һ��Ȼ����μ����η�̪��Һ��
| ���ʵ���Ũ�ȴ����Һ�з�̪��ɫ��ʧ
֤��?
|
����������ԭ��ɫ��ʧ����Һ�м�?
(���Լ�����)
| ��ɫ���³��֣���˵����ɫ��ʧ�������������ʵ���Ũ�ȴ�С�й�
�ο��𰸣�������̪���ʣ��տ�ʼ��Һ�Ͳ�����ɫ�ˡ�
������������Һ������еĶ�����̼��Ӧ����̼���ƺ�ˮ��̼����ˮ��Һ�Լ��ԣ���ɫ������ʧ��
�Ǣٳ�ȥ��Һ������?������ֲ����������
�Ȣٺ�ɫ��ʧ���������Ƶ����ʵ���Ũ�ȴ�С�й�?��ˮ
���������������ʵ��̽��Ϊ��ģ�����ѧ���ķ�������ͽ���������������1����̪������ɫ�������̪���ʣ���ʼ����ʱ�Ͳ��ܱ�ɺ�ɫ���ʼ�˵������ȷ����2�����������������̼��Ӧ������̼������Һ��̼������Һ�ʼ��ԣ���ʹ��̪��Һ��죬���ҵ�˵��Ҳ����ȷ����3����ͬѧ�Ȱ��������Ƽ��ȣ���Ϊ���ž���Һ���ܽ���������ټ�ֲ������Ϊ��ʹ��Һ�������������ֹ����������Ӧ����4���ڶ�ͬѧ�IJ����У�����ڲ�ͬŨ�ȵ�����������Һ�У����ʵ���Ũ�ȴ����Һ���̪�ĺ�ɫ��ʧ����֤����ɫ��ʧ���������Ƶ����ʵ���Ũ�ȴ�С�йأ������ɫ��ʧ����Һ�м�����ˮ����ɫ���֣���֤�����������ȷ�ġ�
�����Ѷȣ���
|