��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��1�������ٷɻ���ƽ�������ʱ��β���е�NO���ƻ������㣮��ѧ�������о����ô�������β���е�NO��COת���CO2��N2����ѧ����ʽ���£�2NO+2CO?

2CO2+N2
�о���������ʹ�õ���������ʱ����������ȱ���������ѧ��Ӧ���ʣ�Ϊ�˷ֱ���֤�¶ȡ������ȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ��У�
| ʵ���� | T/�� | NO��ʼŨ��
mol?L-1 | CO��ʼŨ��
mol?L-1 | �����ıȱ����
�O?g-1
��
280
1.2��10-3
5.8��10-3
82
��
?
?
?
124
��
350
?
?
124
|
�����ڱ���������ʣ���ʵ���������ݣ�
�����ʵ����Ŀ����______��
��2����ҵβ���е��������ﳣ���ð������շ���ԭ����NH3��NOx��Ӧ�����������ʣ�ijͬѧ��������װ�úͲ���ģ�ҵ�ϵ��������ﴦ�����̣��ṩ��װ�ã�

����һ��NH3����ȡ
�����ṩ��װ�����ܿ��١������ȡNH3��װ���ǣ�______����װ����ţ���
��������Cװ����ȡ����������ʵ��������ͬ����������±���| ?�Լ������� | ?�����Լ���g�� | NH3�����ml��?
|
| ?a | ?12.0gCa��OH��2�������� | ?10.8gNH4Cl | ?2688
|
| ?b | ?10.8g��NH4��2SO4 | ?2728
|
| ?c | ?12.0gNaOH�������� | ?10.8gNH4Cl | ?3136
|
| ?d | ?10.8g��NH4��2SO4 | ?3118
|
| ?e | ?12.0gCaO�������� | ?10.8gNH4Cl | ?3506
|
| ?f | ?10.8g��NH4��2SO4 | ?3584
|
�����������ݣ�ʵ������NH3������ߵ���______������ţ���
�������ģ��β���Ĵ�����

ѡ����������װ�ã�������˳�����ӳ�ģ��β������װ�ã�
��A�з�Ӧ�����ӷ���ʽ��______��
��Dװ�������У�ʹ�����Ͼ��ȡ����������ٶȣ�����һ�������ǣ�______��
��Dװ���е�Һ��ɻ���______������ţ���
a��CuSO4��Һ?b��H2O?c��CCl4?d��ŨH2SO4
��ͬѧ����Ƶ�ģ��β������ʵ�黹���ڵ�����ȱ���ǣ�______��
�ο��𰸣���1���ٸ�ʵ������֤�¶ȡ������ȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ����Ԣ���ֻ�ı�������������ֻ�ı��¶ȣ���������?
����Ӧ���������Ϊ��
��280������1.2��10-3��������5.80��10-3��������
��1.2��10-3����?��5.80��10-3����������?
�ڢ�ֻ�ı��¶ȣ�����Ŀ����̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죮
�ʴ�Ϊ��̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죮
��2������һ��NH3����ȡ
���Ʊ������ɲ��ý���NH4Cl��Ca��OH��2��Ũ��ˮ���ȵķ����Ʊ��������ܿ��١������ȡNH3��װ�ÿ��ü���Ũ��ˮ���Ʊ�����Hװ�ã��ʴ�Ϊ��H��
����ΪNH4Cl�����ֽ⣬���ɵIJ���NH3��HCl�����½�ϳ�NH4Cl������NaOH��Ca��OH��2����Ӧ�������ˮ�϶࣬���յ�NH3�϶࣬�ɱ������ݿ��Կ�����f��NH3������ߣ�
�ʴ�Ϊ��f����ΪNH4Cl�����ֽ⣬���ɵIJ���NH3��HCl�����½�ϳ�NH4Cl������NaOH��Ca��OH��2����Ӧ�������ˮ�϶࣬���յ�NH3�϶ࣻ
�������ģ��β���Ĵ���
��ϡ�������ǿ�����ԣ���ͭ����������ԭ��Ӧ��������ͭ��NO�ȣ���Ӧ�����ӷ���ʽΪ3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O��
�ʴ�Ϊ��3Cu+8H++2NO3-�T3Cu2++2NO��+4H 2O��
��Dװ��ʹ�����Ͼ��ȡ����������ٶȣ����⣬���������ڱ��Ͱ�ˮ���ɷ�ֹ������
�ʴ�Ϊ����ֹ�����ܽ⣨���ֹ��������
�ݰ�������������ͭ��Һ��ˮ�Լ������У��ɲ�������������Ϊ���Է��ӣ������ڷǼ����ܼ�������CCl4���汥�Ͱ�ˮ��
�ʴ�Ϊ��c��
��ȱ��β������װ�ã�������NO����Ⱦ�������ʴ�Ϊ��δ��Ӧ��NO������������Ⱦ������
���������
�����Ѷȣ�һ��
2��ʵ���� ��ش�����ʵ��������ȡ������й����⡣
����ͼ����KMnO4��Ũ���ᷴӦ��ȡ���������ļ���װ�á�װ��B��C��D�����÷ֱ��ǣ�
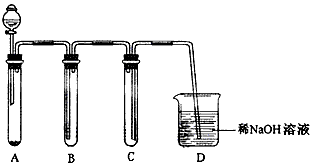
B_________________________��C _______________________��D____________________��
����ʵ��������ȡ������NO���塣
����ͼ����������ɸ�ʵ��ļ���װ����__________������ţ���
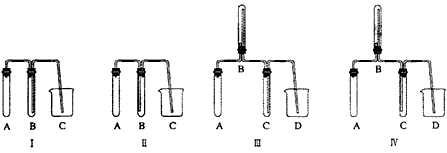
�ڸ�����ѡ��װ������±�������Ҫ�Ŀ��Բ��

�ۼ�����Ӧ�۲쵽������_______________________��
�ο��𰸣��ų�ȥCl2�л��е���������HCl������Һ���ռ����������ն��������
�Ƣ٢�� ��A���Թ��������ݲ�����ͭƬ���٣���Һ�������Թ��ϲ��к���ɫ�����壬һ��ʱ���B��Һ���ų�������ռ�����ɫ���塣
��A���Թ��������ݲ�����ͭƬ���٣���Һ�������Թ��ϲ��к���ɫ�����壬һ��ʱ���B��Һ���ų�������ռ�����ɫ���塣
���������
�����Ѷȣ�һ��
3��ʵ���� ijͬѧ������װ���Ʊ�������Cl2�����ʡ�
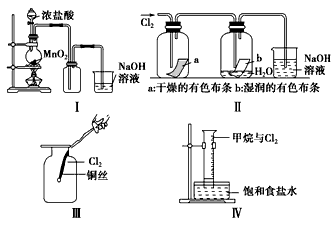
(1)��ͼԲ����ƿ�з�Ӧ�Ļ�ѧ����ʽΪ________________��
(2)��ͼ����ɫ����A____(�a����b��)����ͼ�ձ��з�����Ӧ�����ӷ���ʽ��________________��
(3)��ͭ˿������˿������ʵ�飬���Ҳ�ܵ�ȼ������Ϊ��˿Ҳ�ܵ�ȼ��������A______(��ѡ����ĸ)��
A��Fe��Cu���ǽ���Ԫ�� B��Fe���۵��Cu�� C��Fe���ܶȱ�CuС D��Fe�Ľ����Ա�Cuǿ
(4)����װ�÷����ڹ����ĵط�(�չ�û��ֱ������)��һ����۲쵽��Ͳ��������״Һ�����ɣ�����ʳ��ˮ��������������������Ͳ�ڻ���ɫ������ɫ��dz����Ͳ��Һ�������ȡ�
����״Һ�εijɷֿ�����(д����ʽ) _____________��
��ˮ���ñ���ʳ��ˮ������ˮ��ԭ����__________________��
�۱���ʳ��ˮ��������������������ԭ����__________________��
(5)��������Һ�����ͼʵ�����ձ��У�����Һ�����ԣ����Ҳ��Cl2���ɣ���ԭ����(�����ӷ�Ӧ����ʽ��ʾ)__________________��
�ο��𰸣�(1)MnO2��4HCl MnCl2��Cl2����2H2O��
MnCl2��Cl2����2H2O��
(2)b��Cl2��2OH-===Cl-��ClO-��H2O��
(3)D��
(4)��CH2Cl2��CHCl3��CCl4���ڽ���Cl2��ˮ�е��ܽ�ȣ�����Cl2��ˮ�ķ�Ӧ���۷�Ӧ����HCl���ɣ�ʹ��Һ�е�Cl-Ũ������ʹNaCl���ܽ�ƽ��������NaCl����ķ����ƶ�
(5)Cl-��ClO-��2H+==Cl2����H2O
���������
�����Ѷȣ�һ��
4��ѡ���� ��ͼ����ȡ���ռ�ij�����ʵ��װ�ã���װ�ÿ�����
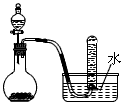
[? ]
A��Ũ������ͭ��Ӧ��ȡ�������� ?
B��?����������������̷�Ӧ��ȡ���� ?
C��?Ũ��ˮ����ʯ�ҷ�Ӧ��ȡ���� ?
D��?Ũ����Ͷ������̷�Ӧ��ȡ����
�ο��𰸣�B
���������
�����Ѷȣ���
5��ʵ���� ͼ�е�ʵ��װ�ÿ�������ȡ��Ȳ������գ�

(1)ͼ�У�A�ܵ�������______________����ȡ��Ȳ�Ļ�ѧ����ʽ��________________________________________________________________________��
(2)��Ȳͨ��KMnO4������Һ�й۲쵽��������_________________________________________________________________________����Ȳ������________��Ӧ��
(3)��Ȳͨ�����CCl4��Һ�й۲쵽��������________________________________________________________________________����Ȳ������________��Ӧ��
(4)Ϊ�˰�ȫ����ȼ��ȲǰӦ________����Ȳȼ��ʱ��ʵ��������________________________________________________________________________��
�ο��𰸣�(1)����ˮ��߶��Կ��Ʒ�Ӧ�ķ�����ֹͣ��CaC2+2H2O��Ca(OH)2+C2H2��
(2)KMnO4��Һ��ɫ������
(3)Br2��CCl4��Һ��ɫ���ӳ�
(4)������Ȳ�Ĵ��ȣ���������������Ũ�ҵĺ���
���������
�����Ѷȣ�һ��