��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� С����ʵ��ʱ��С��մ��һЩKMnO4��Ƥ���ϵĺڰߺܾò�������������ò����ϡ��Һϴ�����Ͽ��Ը�ԭ�������ӷ���ʽΪ��MnO4-+H2C2O4+H+��CO2��+Mn2++����δ��ƽ�������ڴ˷�Ӧ��������ȷ���ǣ�������
A���÷�Ӧ����������H2C2O4
B��1molMnO4-�ڷ�Ӧ��ʧȥ5mol����
C���÷�Ӧ�ҿ��ڵIJ�����OH-
D����ƽ�÷�Ӧ��H+�ļ�������6
�ο��𰸣�A�����ϼ۽��͵�Ԫ������Ԫ�أ����ڷ�Ӧ��KMnO4������������A����
B����Ԫ�ػ��ϼ۴�+7�۽��͵�+2�ۣ�Ԫ�صõ����ӣ����ϼ۽�����=�õ����ӵ���Ŀ=5����1molMnO4-�ڷ�Ӧ�еõ�5mol���ӣ���B����
C�����ݵ����غ㣬�÷�Ӧ����Ԫ�ػ��ϼ۽���5�ۣ���̼Ԫ�ػ��ϼ۹�����2�ۣ����Է�Ӧת�Ƶ�����Ϊ10�����Կ��Եõ���2MnO4-+5H2C2O4+H+��10CO2��+2Mn2++�������ݵ���غ㡢ԭ���غ㣬���ԡ���Ϊ8H2O��H+�ļ�������6����C����
D������ԭ���غ㡢�����غ�͵���غ�����ƽ���ӷ���ʽΪ��2MnO4-+5H2C2O4+6H+�T10CO2��+2Mn2++8H2O��H+�ļ�������6����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
2���ƶ��� ��16�֣��Ի�����Ϊԭ��������������������к�Fe2O3��SiO2��Al2O3��MgO�ȣ����������Ʊ����죨Fe2O3���Ĺ������£�

��1�����ܹ�����Fe2O3��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ ��
������A����Ҫ�ɷݵĻ�ѧʽΪ ��
��2����ԭ�����м���FeS2��Ŀ���ǽ���Һ�е�Fe3 +��ԭΪFe2 +��������������ΪH2SO4������ɸ÷�Ӧ�����ӷ���ʽ��FeS2 + 14Fe3 + + H2O="=" 15Fe2 + + SO42- + ��
��3�����������У�O2��NaOH��Fe2+��Ӧ�����ӷ���ʽΪ ��
��4��Ϊ��ȷ�����������������������Ҫ������Һ��pH�ķ�Χ�� ���������ӳ�����pH���±�������ҺB���Ի��յ������У�д��ѧʽ�� ��
������
| Fe(OH)3
| Al(OH)3
| Fe(OH)2
| Mg(OH)2
|
��ʼ����pH
| 2.7
| 3.8
| 7.6
| 9.4
|
��ȫ����pH
| 3.2
| 5.2
| 9.7
| 12.4
|
�ο��𰸣���16�֣�
��1����5�֣�Fe2O3 + 3H2SO4 ="=" Fe2(SO4) 3+ 3H2O��2�֡���ѧʽ1�֡���ƽ1�֣�
SiO2��2�֡���дFeS2���۷֣���д������ѧʽ0�֣�
��2����3�֣�8 2 16H+���ڿ�1�֣�
��3����4�֣�4Fe2 + + O2 + 2H2O + 8OH��= 4Fe(OH)3�� ����ѧʽ��2�֡���ƽ2�֡���
Fe2++2OH-=Fe(OH)2����2�֣���4Fe(OH)2+O2+2H2O=4Fe(OH)3��2�֣�
������������д���ڸ�����ʽ��ѧʽ��1�֡���ƽ1�֣�
��4����5�֣�3.2~3.8����֮�������ֵ��2�֣� Na2SO4��Al2(SO4)3��MgSO4��3�֣���дH2SO4���۷֣���д����0�֣�
�����������1����������ϡ���ᷴӦ������������ˮ����ѧ����ʽΪFe2O3 + 3H2SO4 ="=" Fe2(SO4) 3+ 3H2O����������ֻ�ж������費��ϡ���ᷴӦ�����ԡ�����A����Ҫ�ɷݵĻ�ѧʽΪSiO2��
��2��FeS2�е�SԪ�صĻ��ϼ���-1�ۣ���������Fe�Ļ��ϼ���+2�ۣ�S�Ļ��ϼ���+6�ۣ���������14�ۣ���Fe3+�Ļ��ϼ۽���1�ۣ������������ϼ�������ȣ�����Fe3+��ϵ����14����SO42-��ϵ����2���ٸ���Ԫ���غ�͵���غ��ж��������л��������ӣ���ϵ��Ϊ16����ˮ��ϵ����8��
��3��O2��NaOH��Fe2+��Ӧ���������������������ӷ���ʽΪ4Fe2 + + O2 + 2H2O + 8OH��= 4Fe(OH)3����
��4�����ݱ�������ʹ��������ȫ���������������Ӳ��ܳ�����������Һ��pH�ķ�Χ�ǣ�3.2~3.8����ҺB�������������ӵ������Σ���Na2SO4��Al2(SO4)3��MgSO4��
���㣺����Թ������̵ķ��������ʵ��жϣ���ѧ����ʽ����ƽ
�����Ѷȣ�����
3��ʵ���� ��12�֣�ijѧ��Ϊ̽������CO2�ķ�Ӧ����������װ�ý���ʵ�顣����֪PdCl2�ܱ�CO��ԭ�õ���ɫ��Pd�����ɹ�ѡ���ҩƷ�У�CaCO3����״����Na2CO3����ĩ�������ᡢϡ���ᡢ�ơ�
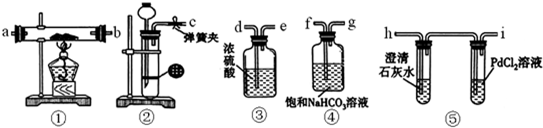
��1���뽫��ͼ��װ�������������ڡ� �� ���١� ������װ����ţ�
��2��д��װ�â��з�Ӧ�����ӷ���ʽ�� ��
��3�����װ�������Բ�װ��ҩƷ���۲쵽 ����ʱ�ٵ�ȼ�ƾ��ƣ�װ�âܵ������� ��
��4����֪CO�ڳ�ʪ�����пɽ�PdCl2��ԭΪ��ɫ��ĩ״���٣�Pd����д���÷�Ӧ�Ļ�ѧ����ʽ ��
��5��ʵ�������CO2������װ�â�PdCl2��Һ�й۲쵽�к�ɫ������װ�â��з�Ӧ�����ɷ�ֻ��һ�֣���������м���ϡ���������ʹ����ʯ��ˮ����ǵ����塣�ݴ�����д��Na��CO2��Ӧ�Ļ�ѧ����ʽ�� ��
�ο��𰸣���1���ܢۢ�(2��) ��2��CaCO3��2H+��Ca2+��CO2����H2O
��3��װ�â��г���ʯ��ˮ����ǣ����ջӷ�������HCl
��4��PdCl2��CO��H2O��Pd��CO2��2HCl
��5��2Na+2CO2
���������
�����Ѷȣ�����
4��ѡ���� M2O7X-��S2-��������Һ�з�Ӧ���£�M2O7X��+3S2��+14H+��2M3++3S��+7H2O����M2O7X����M�Ļ��ϼ���
A��+2
B��+3
C��+4
D��+6
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
5��ѡ���� ���в������ڸ��ϲ��ϵ���
A���Ͻ�
B��������
C�������մ���
D�����½ṹ�մ�
�ο��𰸣�B��C
����������Ͻ��������ֻ��������ϵĽ�����ǽ����ں϶��ɵľ��н������Ե����ʣ������ڸ��ϲ��ϡ����½ṹ�մɶ��ǵ�һ���ϣ��絪����ṹ�մɵȡ��������Dz�����ά�ͺϳ���֬�γɵĸ��ϲ��ϡ������մ���������ά����̼��ά�����մ��γɵĸ��ϲ���
�����Ѷȣ���