| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点归纳《原电池原理》答题技巧(2017年最新版)(一)
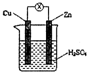 3、选择题 下列关于原电池的叙述中正确的是( ) 4、填空题 氨气在科研、生产中有广泛应用。 5、选择题 有关下图的说法不正确的是 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《物质的量》.. | |