微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
[? ]
A.工业盐酸因溶解了氯气而呈现黄色
B.1mol Cu能与含有2mol H2SO4的浓硫酸恰好完全反应,生成1molSO2
C.铁件镀铜,溶液为硫酸铜溶液,电镀过程中溶液的浓度保持不变粗铜精炼过程中,溶液也为硫酸铜溶液,溶液的浓度也保持不变
D.浓度均为0.1mol/L的苯酚钠溶液和CH3COONa溶液中:阴离子的总浓度前者小于后者
参考答案:D
本题解析:
本题难度:一般
2、推断题 非金属单质a及其化合物在一定条件下可发生如图所示的变化,五种物质中都含有同一种元素。

(1)若a常温下是一种固体,则a是___________,c是___________。 e→c的化学方程式为______________________。
(2)若a常温下是一种气体,则a是___________,d是___________。 e→c的离子方程式为______________________。 b→c的化学方程式为______________________。
参考答案:(1)a:S;c:SO2;e→c:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(2)a:N2;d:NO2;e→c:3Cu+8H++2NO3-==3Cu2++2NO↑+4H2O;b→c:4NH3+5O2 4NO+
4NO+
6H2O
本题解析:
本题难度:一般
3、选择题 在稀硫酸中加入铜粉,铜粉不溶解,再加入下列固体粉末:①FeCl2;②Fe2O3;③Zn;④KNO3,铜粉可溶解的是?
[? ]
A.①②?
B.②④?
C.②③?
D.①④
参考答案:B
本题解析:
本题难度:一般
4、选择题 为证明铁的金属活动性比铜强,某同学设计了如下4个方案,其中能证明铁的金属活动性比铜强的方案是
[? ]
方案
?现象或产物
A.
将铁片置于CuSO4溶液中
铁片上有亮红色物质析出
B.?
将铁丝和铜丝分别在氯气中燃烧
产物分别为FeCl3和CuCl2
C.
将铁片和铜片分别放入热浓硫酸中
分别为Fe2(SO4)3和CuSO4
D.
将铜片置于FeCl3溶液中?
铜片逐渐溶解
参考答案:A
本题解析:
本题难度:一般
5、填空题 废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。
(1)写出工业上制备印刷电路板反应原理的离子方程式:____________________。
(2)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是_______(填字母)。
A.热裂解形成燃油 B.露天焚烧 C.作为有机复合建筑材料的原料 D.直接填埋
(3)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。写出在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的离子方程式:___________________
(4)控制其他条件相同,印刷电路板的金属粉末用10% H2O2和3.0mol/L H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
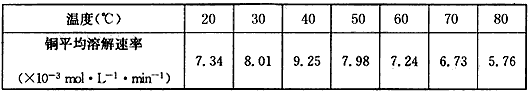
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是__________
(5)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀。制备CuCl的离子方程式是________________。
参考答案:(1)2Fe3++Cu=2Fe2++Cu2+
(2)BD
(3)Cu+H2O2+2H+=Cu2++2H2O
(4)H2O2分解速率加快
(5)2Cu2++SO32-+2Cl-+H2O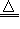 2CuCl↓+SO42-+2H+
2CuCl↓+SO42-+2H+
本题解析:
本题难度:一般