微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关短周期元素的叙述中,肯定正确的是
A.原子最外层电子只有1个或2个的元素是金属元素
B.16号元素原子的最 外层电子数是4号元素
外层电子数是4号元素 原子最外层电子数的四倍
原子最外层电子数的四倍

C.11号元素与17号元素能形成XY2型化合物
D.136C表示的碳原子核内有6个质子、7个中子
参考答案:D
本题解析:略
本题难度:一般
2、选择题 短周期元素aA2+、bB+、cC3-、dD-都具有相同电子层结构,则下列叙述正确的是(? )
A.原子半径A>B>D>C
B.原子序数D>C>B>A
C.离子半径C>D>B>A
D.单质还原性A>B>D>C
参考答案:
本题解析:A选项,aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则离子核外电子数相同,即a-2=b-1=c+3=d-1,原子序数A>B>D>C,A、B处于同一周期,C、D处于同一周期,且A、B处于C、D所在周期的相邻下一周期,同周期,原子序数越大原子半径越小,所以原子半径B>A,C>D,电子层越大原子半径越大,所以原子半径B>A>C>D,故A错误;B选项,aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则离子核外电子数相同,即a-2=b-1=c+3=d-1,原子序数A>B>D>C,故B错误;C选项,电子层结构相同,核电荷数越大,离子半径越小,核电荷数A>B>D>C,所以离子半径C3->D->B+>A2+,故C正确;D选项,A、B处于同一周期,A、B形成阳离子,则A、B为金属,原子序数A>B,单质还原性B>A,C、D处于同一周期,C、D形成阴离子,则C、D为非金属,原子序数D>C,单质氧化性D>C,故D错误。
本题难度:一般
3、选择题 右表是元素周期表的一部分。X、Y、Z、W均为短周期元素,X、W的质子数之和为23。下列说法正确的是?(?)
?
A.原子半径:W>Y
B.氢化物的稳定性:Y<Z
C.最高价氧化物对应水化物的酸性:W>Z
D.Z的氧化物不能溶于Y的氢化物的水溶液
参考答案:C
本题解析:略
本题难度:一般
4、选择题 下列分子结构中,原子的最外电子都能满足8电子稳定结构的是(?)
A.XeF2
B.CO2
C.PCl5
D.HClO
参考答案:B
本题解析:在分子形成的过程中,原子都有趋向最外层电子层为8(或2)电子的“稳定结构”(稀有气体原子的结构)。离子化合物形成时,活泼的金属原子失去最外层的少数电子,形成稳定阳离子结构;活泼的非金属原子获得电子,最外层补足到8电子,形成稳定的阴离子结构。共价化合物形成时,原子间相互吸引对方的电子,组成共用电子对,形成8电子稳定结构。常见的稳定结构多为8电子结构,但也存在非电子结构的稳定状态。如对氢原子来说,最外层有2个电子,就达到稳定结构。
选项C的磷原子,最外层有5个电子,分别和5个氯原子结合,形成5个共用电子对,磷原子最外层形成10个电子结构。选项D中的次氯酸,含氧酸的结构是:+1价的氯原子和-1价的氢氧根原子团结合,也就是氧原子分别和氢原子、氯原子结合,氧原子达到8电子稳定结构,而氢原子仅能达到2电子的稳定结构。在选项A中,稀有气体氙原子的结构已是稳定结构,当它和氟原子结合时,最外层电子数必然超过8个。本题的正确选项只能是B,CO2的结构中,碳原子分别和两个氧原子形成碳氧双键,每个原子的最外层为8电子稳定结构。
本题难度:简单
5、填空题 有A,B,C,D,E五种短周期元素,A与B可形成BA型化合物,且A元素是非金属性最强的元素.金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8个;C元素有三种同位素C1,C2,C3,自然界里含最多的是C1,C3的质量数是C1的3倍,C2的原子的质量数是C1的2倍.D的气态氢化物的水溶液呈碱性,而其最高价氧化物的水化物为强酸,E元素原子的最外层电子数比次外层电子数多4个,E离子的核外电子数比质子数多2个.
(1)写出元素名称:A.?B.?C.?D?.?E.?.
(2)写出C1,C2, C3粒子的符号:?,?,?
(3)写出E离子的结构示意图?E的氢化物的分子式?.
(4)写出A的单质与B的单质反应的化学方程式?;
(5)写出A的单质和B的单质分别与水反应的化学方程式?,?,将二者反应后生成的溶液混合,发生反应的离子方程式为?
(6)A与C形成的化合物中含化学键类型是?.用电子式表示该化合物的形成过程??.
参考答案:(每空各1分,共16分) (1)氟;钠;氢;氮;氧? (2) 1 1H,2 1H(D),3 1H(T)
(3)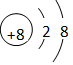 ; H2O (4)2Na+F2=2NaF
; H2O (4)2Na+F2=2NaF
(5)2F2+2H2O=4HF+O2↑;Na+2H2O=2NaOH+H2↑; OH-+HF=F-+H2O?
(6)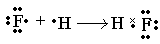 ?共价键
?共价键
本题解析:A元素是非金属性最强的元素,则A是F元素。金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8个,所以根据化学式BA可知,B是第IA元素,所以B是Na。C元素有三种同位素C1,C2,C3,自然界里含最多的是C1,C3的质量数是C1的3倍,C2的原子的质量数是C1的2倍,由此可知,C是氢元素。D的气态氢化物的水溶液呈碱性,氨气溶于水显碱性,所以D是氮元素。E元素原子的最外层电子数比次外层电子数多4个,E离子的核外电子数比质子数多2个,这说明E是非金属元素氧元素。
点评:该题是中等难度的试题,试题综合性强,贴近高考。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
本题难度:一般