��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ѧ��ѧ��Ҫ������ѧר�������������������йػ�ѧ������ȷ���ǣ�������
A��CO2�ĵ���ʽ��
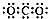
B��������Ϊ37����ԭ�ӣ�
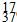
Cl
C��NH4Cl�ĵ���ʽ��
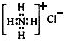
D��ԭ�Ӻ�����10�����ӵ���ԭ�ӣ�

�ο��𰸣�D
���������
�����Ѷȣ���
2������� �춬����(�ṹ��ͼ)��«���к����ḻ��������������������Ĺ�Ч��
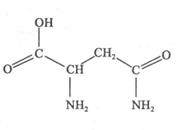
��1���춬��������Ԫ���У�??(��Ԫ������)Ԫ�ػ�̬ԭ�Ӻ���δ�ɶԵ�������࣬�춬������̼ԭ�ӵ��ӻ����������?�֡�
��2��H2S��H2Se�IJ����Աȼ�����
��ѧʽ
| ������nm
| ����
| �е㣯��
|
H2S
| 1.34
| 92.3o
| һ60.75
|
H2Se
| 1.47
| 91.0o
| һ41.50
|
?
��H2Se�ľ�������Ϊ?�����еĹ��ۼ�����Ϊ?��
��H2S�ļ��Ǵ���H2Se��ԭ�����Ϊ?��
��3����֪��(Mo)λ�ڵ�������VIB�壬�⡢�����̵IJ��ֵ��������±���ʾ
���
| I5��kJ��mol-1
| I6��kJ��mol-1
| I7��kJ��mol-1
| I8��kJ��mol-1
|
A
| 6990
| 9220
| 11500
| 18770
|
B
| 6702
| 8745
| 15455
| 17820
|
C
| 5257
| 6641
| 12125
| 13860
|
?
A��??(��Ԫ�ط���)��B�ļ۵����Ų�ʽΪ ?��
�ο��𰸣���1������1�֣�? 2 ��1�֣�
��2���ٷ��Ӿ��壨2�֣� ���Լ���2�֣�
�� ����S�ĵ縺��ǿ��Se���γɵĹ��õ��ӶԳ������Ǵ�2�֣�
��3��Mn��2�֣� 3d54s1��2�֣�
�����������1���춬��������̼���⡢����������Ԫ�أ���̬ԭ�Ӻ���δ�ɶԵ���������Ϊ��Ԫ�ء�
��2����H2Se�ڳ���ʱΪ�ɷǽ���Ԫ���γɵ���̬�⻯�Ϊ���Ӿ��壻H��SeΪ��ͬԪ�أ��γɵĹ��ۼ�Ϊ���Լ���
��S��SeΪͬ����Ԫ�أ�Sλ�ڵ������ڡ�Seλ�ڵ������ڣ�S�ĵ縺��ǿ��Se���γɵĹ��õ��ӶԳ���������H2S�ļ��Ǵ���H2Se��
��3��Aԭ�� I5��I6�� I7�� I8��������Aԭ��ʧȥ��8�����Ӷ��Ǽ۵��ӣ�����AΪMnԪ�أ�B��Cԭ��I7��I6���˺ܶ࣬˵��B��Cԭ�ӵļ۵���Ϊ6��������������B����C��˵��BΪ�������ڵ�Cr��CΪ��(Mo)λ�ڵ������ڣ�Cr�ļ۵����Ų�ʽΪ��3d54s1
�����Ѷȣ�һ��
3������� ̼���⡢����������ȷǽ���Ԫ�����������������ϢϢ��ء��ش��������⡣
(1)д����ԭ�ӵĵ����Ų�ʽ________��C��Si��N�ĵ縺���ɴ�С��˳����________��
(2)������ˮ��Һ�д��ڵ������________�֡�
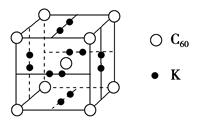
(3)��ѧ�Ұ�C60��K������һ��������һ�ָ���ϩ��صĻ�����������ڵ���ʱ��һ�ֳ����壬�侧����ͼ��ʾ����������Kԭ�Ӻ�C60���ӵĸ�����Ϊ________��
(4)��C60��ѧ���ֺϳ���Si60��N60����������������۵�Si60>N60>C60�����ƻ���������Ҫ������N60>C60>Si60����ԭ����________________________��
�ο��𰸣�(1)1s22s22p63s23p2��N>C>Si
(2)4��(3)3��1
(4)�ṹ���Ƶķ��Ӿ������Է�������Խ���Ӽ�������(�»���)Խǿ���ۻ����������Խ�࣬���۵㣺Si60>N60>C60�����ƻ�������Ͽ���ѧ����Ԫ�ص縺��Խǿ���γɵĻ�ѧ��Խ�ȶ����ϼ�ʱ��������Խ�࣬���ƻ�������Ҫ��������С˳��ΪN60>C60>Si60
���������(2)HF��H2O�����γ������H��F��H��F��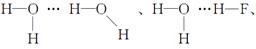 H��O��H��F��H�����֡�
H��O��H��F��H�����֡�
(3)K���ھ������棺12��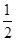 ��6��C60���ھ�����������ģ�8��
��6��C60���ھ�����������ģ�8��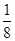 ��1��2����Kԭ�Ӻ�C60���ӵĸ�����Ϊ��6��2��3��1��
��1��2����Kԭ�Ӻ�C60���ӵĸ�����Ϊ��6��2��3��1��
(4)�۵�����Ӽ���������С�йأ����ƻ����������ƻ������ڵĹ��ۼ���
�����Ѷȣ�һ��
4������� ����ѧ��ѡ��3�����ʽṹ�����ʡ���15�֣�
��������Ԫ�أ�����A��B��C��D��EΪ����������Ԫ�أ�F��GΪ��������Ԫ�أ����ǵ�ԭ����������������������������Ϣ���ش����⡣
AԪ�صĺ���������͵��Ӳ�����ȣ�Ҳ��ԭ�Ӱ뾶��С��Ԫ��
|
BԪ��ԭ�ӵĺ���p��������s��������1
|
Cԭ�ӵĵ�һ�����ĵ����ֱܷ���:
I1=738kJ/mol? I2 =" 1451" kJ/mol? I3 = 7733kJ/mol? I4 = 10540kJ/mol
|
Dԭ�Ӻ�������p���ȫ�������
|
EԪ�ص������������������IJ�Ϊ4
|
F��ǰ�������е縺����С��Ԫ��
|
G�����ڱ��ĵ�����
|
?
��1����֪BA5Ϊ���ӻ����д�������ʽ?
��2��B��̬ԭ����������ߵĵ��ӣ���������ڿռ���?������ԭ�ӹ����?��
��3��ijͬѧ����������Ϣ���ƶ�C��̬ԭ�ӵĺ�������Ų�Ϊ��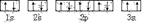
��ͬѧ�����ĵ����Ų�ͼΥ����?
��4��Gλ��?��?�����۵����Ų�ʽΪ??
��5��DE3 ����ԭ�ӵ��ӻ���ʽΪ?���ü۲���ӶԻ��������Ʋ���ռ乹��Ϊ?
��6������FԪ�صķ�����??������ԭ�ӽṹ��֪ʶ���Ͳ����������ԭ����?
?
��7��FԪ�صľ�������ͼ��ʾ������þ������ܶ�Ϊa g/cm3�������ӵ�����ΪNA��
Fԭ�ӵ�Ħ������ΪM����Fԭ�ӵİ뾶Ϊ??cm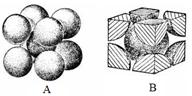
�ο��𰸣���1�� ?��2�֣�?��2��? 3?��1�֣����Ĵ��Σ�1�֣�
?��2�֣�?��2��? 3?��1�֣����Ĵ��Σ�1�֣�
��3������������ԭ����1�֣�?��4��?�ڢ�B��1�֣� d ��1�֣���3d54s2��1�֣�
��5�� sp3��1�֣��������Σ�1�֣���6����ɫ��Ӧ��1�֣���?����̬ԭ�ӵĵ��������������ӻ�ԾǨ���ϸ��ܼ�����ɼ���̬ԭ�ӡ����Ӵӽϸ������ļ���̬ԾǨ���ϵ������ļ���̬������̬ʱ�����Թ����ʽ�ͷ�������?��2�֣�?
��7��?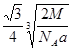 ?��2�֣�
?��2�֣�
�������������Ԫ�ص����ʡ�ԭ�Ӻ�������Ų����ɼ�Ԫ�������ڱ��е�λ�ÿ����жϣ�A��H��B��N��C��Mg��D��P��E��Cl��F��K��G��Mn��
��1�����ӻ�������һ���������Ӽ������Ըû���������MH4����H���γɵ����Ӽ�������ʽΪ ��
��
��2��Nԭ�Ӻ������������ߵ���p���ӣ��ڿռ���3������ԭ�ӹ���ʷĴ��Ρ�
��3��1��ԭ�ӹ��������ɵĵ�����2���������������෴�����������ԭ����3s����еĵ�������������ͬ��Υ��������ԭ����
��4��Mn���ڵ������ڵڢ�B��Mnԭ���������ĵ��� 91EXAm.org��d����ģ�����Mn����d�����̵�ԭ�Ӻ�����25�����ӣ����Ծ���25���˶�����
��5��PCl3������ԭ�ӵŵ��Ӷ�����1/2��5��3��
+
�����Ѷȣ�һ��
5��ѡ���� ����˵������ȷ���ǣ�?��
A��NO2��SO2��BF3����������ԭ�ӵ��������Ӷ�������8e���ȶ��ṹ
B��P4��CH4����������������Ҽ��Ƕ�Ϊ109o28�@
C��CsCl��������ÿ��Cs+��������������Cl-����8��
D��ԭ�Ӿ�����۷е�һ���Ƚ�������ĸ�
�ο��𰸣�C
������������ۻ�������Ԫ�ػ��ϼ۵ľ���ֵ������������֮������8�����Ԫ��ԭ�ӵ��������Ӿ�������8�����ȶ��ṹ������A��N��S��B�������㣬A����ȷ�����ļ�����60��ģ�B����ȷ��ԭ�Ӿ�����۷е㲻һ���Ƚ�������ĸߣ������ٵ��۷е�ͺܸߣ�D����ȷ�����Դ�ѡC��
�����Ѷȣ�һ��