��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����dz��ȵ�λ��1������1��10-��m������g�����ﵽ����ʱ����������g���ʣ����罫����ͭ�Ƴɡ�����ͭ��ʱ���зdz�ǿg��ѧ���ԣ��ڿ����п���ȼ�գ����жԡ�����ͭ��g�й�������ȷg�ǣ�������
A�������¡�����ͭ����ͭƬ�Ľ�����ǿ����Ӧʱ��Ӧ���ʿ�
B�������¡�����ͭ����ͭƬ����ʧ���ӣ���Ӧʱ��Ӧ���ʿ�
C�������¡�����ͭ����ͭƬ�Ļ�ԭ��ǿ
D��������ͭ��������ϸС����ѧ��Ӧʱ�Ӵ�������Է�Ӧ���ʿ�
�ο��𰸣�������ͭ����ͭƬ����ͭԪ����ɣ���ѧ����һ�������ǡ�����ͭ���ı�����ϴ��������ֽӴ�����Ӧ���ʽϴ��ڿ����п���ȼ�գ�
��ѡD��
���������
�����Ѷȣ���
2��ѡ���� ������ʾ���淴Ӧ��2A��g����B��g��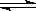 2C��g����H<0 ����ȷͼ������ͼ�е�( )
2C��g����H<0 ����ȷͼ������ͼ�е�( )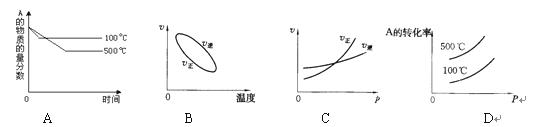
�ο��𰸣�C
����������¶�Խ�ߣ���Ӧ����Խ�죬�ﵽƽ���ʱ��Խ�٣�A��B����ȷ���÷�Ӧ�������С�ġ����ȵĿ��淴Ӧ��������ѹǿ��ƽ��������Ӧ������У�C��ȷ�������¶ȣ�ƽ�����淴Ӧ������У���Ӧ���ת���ʽ��ͣ�D����ȷ����ѡC��
���㣺������������Է�Ӧ���ʺ�ƽ��״̬��Ӱ��
�������ڷ����й�ͼ��ʱӦ��ע�⣺һ���ͣ�t ͼ��� c��t ͼ��1.�ͣ�t ͼ�������淴Ӧ�����������(Ũ�ȡ��¶ȡ�ѹǿ������)�Է�Ӧ���ʺ�ƽ���ƶ���Ӱ�졣 ����ƽ��ͼ�� 1.���ֹյ��ͼ�������ݡ��ȹ���ƽ������ת���ʣ�ʱ��ͼ������ʵİٷֺ�����ʱ��ͼ���У��ȳ��ֹյ�������ȴﵽƽ��(�����¶ȸ�ѹǿ���ʹ�ú��ʵĴ�����)��
�����Ѷȣ�����
3��ѡ���� ����100mL1mol/L��������������Ƭ��Ӧ����ȡ���д�ʩ��ʹ��Ӧ���ʼӿ���H2�IJ���������ǣ��������¶ȣ��ڸ���100mL18mol/L����۸���100mL2mol/L��������������۴�����Ƭ���ݵ�������CuSO4��Һ��������
A���٢ۢ�
B���٢ܢ�
C���ڢۢ�
D���٢ڢ�
�ο��𰸣��������¶ȣ�ʹ��Ӧ���ʼӿ���H2�IJ������䣬����ȷ��
�ڸ���100mL18mol/L���ᣬ����������ԭ��Ӧ�������������ʴ���
�۸���100mL2mol/L���ᣬ����������ԭ��Ӧ�������������ʴ���
�����������۴�����Ƭ������Ӵ������ʹ��Ӧ���ʼӿ���H2�IJ������䣬����ȷ��
�ݵ�������CuSO4��Һ������ԭ��أ�ʹ��Ӧ���ʼӿ���H2�IJ������䣬����ȷ��
��ѡB��
���������
�����Ѷȣ�һ��
4��ѡ���� ���ڷ�Ӧ2SO2��g��+O2��g��?2SO3��g��������������Ӧ���ʵĴ�ʩ�ǣ�������
A�����������ݻ�
B����ȥ����SO3
C��ͨ�����O2
D��������ϵ�¶�
�ο��𰸣�A�����������ݻ�����С����ϵ��ѹǿ��ѹǿ��С������Ӧ���ʼ�С����A����
B����ȥ������������Ӧ���Ũ�Ȳ��䣬�������Ũ�ȼ�С����ѧƽ��������Ӧ�����ƶ�����������Ӧ���ʼ�С����B����
C��ͨ���������������Ӧ���Ũ�ȣ�����������Ӧ���ʣ���C��ȷ��
D��������ϵ���¶ȣ����淴Ӧ���ʶ���С����D����
��ѡC��
���������
�����Ѷȣ�һ��
5��ѡ���� ��þ��Ͷ�뵽ʢ������ij������������H2�����ʿ���ͼ��ʾ�������������У��������Ũ�ȣ���þ���ı����������Һ���¶ȣ���Cl ��Ũ�ȡ�Ӱ�췴Ӧ���ʵ�������?
��Ũ�ȡ�Ӱ�췴Ӧ���ʵ�������?
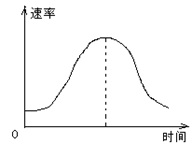 ?
?
A���٢�
B���ۢ�
C���٢ڢ�
D���ڢ�
�ο��𰸣�C
���������ͼ�����������ķ�Ӧ������������С�������ķ�ӦΪMg+2H+�TMg2++H2������ʼ��ӦʱŨ��������ŷ�Ӧ�Ľ��У�Ũ����С��������������������أ���Ӧ����Ӧ��С������ʼ�η�Ӧ����������˵���¶ȶԷ�Ӧ������Ӱ�죬��÷�ӦΪ���ȷ�Ӧ������ʹ�¶����ߣ���Ӧ���ʼӿ죬�ʢ���ȷ����1���ŷ�Ӧ�Ľ��У���Ӧ���ʿ�ʼ���ͣ��������ڷ�Ӧ������Һ�������ӵ�Ũ�Ƚ��ͣ��Ӷ����·�Ӧ���ʽ��ͣ��������ӵ�Ũ�ȶԷ�Ӧ������Ӱ�죬������ȷ���ɷ�Ӧ��֪Mg�μӷ�Ӧ����ʼ�Ӵ������Ӧ���ʿ죬���淴Ӧ�Ľ��У��Ӵ������С����Ӧ���ʼ�С���ʢ���ȷ����Cl�����μӷ�Ӧ��Cl����Ũ��������С����Ӱ�컯ѧ��Ӧ���ʣ��Ҹ÷�Ӧ��Cl-��Ũ�Ȳ��䣬�ʢܴ���Ӱ�췴Ӧ���ʵ�����Ϊ�٢ڢۣ���ѡC��
�����������Ǹ߿��еij������㣬�����е��Ѷȵ����⣬���ض�ѧ�����������ɺ��ܽ��������������������ȷ��Ӧԭ����ͼ���еķ�Ӧ���ʱ仯��Ӱ�췴Ӧ���ʵij��������ǽ����Ĺؼ���
�����Ѷȣ���