微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4==Na2SO4+SO2↑+S↓+H2O,下列各组实验中最先出现浑浊的是
[? ]
反应温度/℃ Na2S2O3溶液V/mL c/(mol/L-1)? 稀H2SO4V/mL c/(mol/L) H2OV/mL
A. 25 5 0.1 10 0.1 5
B. 25 5 0.2 5 0.2 10
C. 35 5 0.1 10 0.1 5
D. 35 5 0.2 5 0.2 10
参考答案:D
本题解析:
本题难度:一般
2、选择题 下述实验不能达到预期实验目的是( )
A.将2.5gCuSO4?5H2O溶解在97.5g水中 目的是配制质量分数为1.6%的CuSO4溶液
B.向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 目的是说明一种沉淀能转化为另一种更难溶的沉淀
C.室温下,用pH试纸测定浓度为0.1mol?L-1NaClO溶液和0.1mol?L-1CH3COONa溶液的pH 目的是比较HClO和CH3COOH的酸性强弱
D.室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 目的是研究浓度对反应速率的影响
参考答案:A.2.5gCuSO4?5H2O中CuSO4的质量为2.5g×160250=1.6g,溶液的质量为2.5g+97.5g=100g,则配制质量分数为1.6%的CuSO4溶液,故A正确;
B.因硫化银比氯化银更难溶,则向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液,会得到黑色沉淀,说明一种沉淀能转化为另一种更难溶的沉淀,故B正确;
C.pH试纸不能测出NaClO溶液的pH,能使试纸褪色,则不能用pH试纸测定浓度为0.1mol?L-1NaClO溶液和0.1mol?L-1CH3COONa溶液的pH来比较HClO和CH3COOH的酸性强弱,故C错误;
D.固定其他因素不变,则稀硫酸的浓度不同,反应的反应速率不同,故D正确;
故选C.
本题解析:
本题难度:简单
3、填空题 (8分)为了研究MnO2与双氧水(H2O2)的反应速率,某学生加少许的MnO2粉末于 50 mL密度为1.1g?cm-3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如下图所示。请依图回答下列问题:
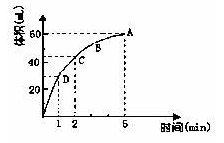
(1)实验时放出气体的总体积为 ___ ;
(2)放出一半气体所需要的时间为 ___ ;
(3)ABCD四点化学反应速率的由快到慢顺序为 ____ _______ ;
(4)在5min后,收集到的气体体积不再增加,原因是 。
参考答案:(8分) (1)60mL ; (2)1min ; (3) D>C>B>A ;(每空2分)
(4)此时双氧水已经完全分解;(2分)
本题解析:(1)根据图像可知,当气体的体积达到60ml时,就不再发生变化,所以实验时放出气体的总体积是60ml。
(2)当反应中生成3ml气体时,所用的时间是1min。
(3)反应速率越大,反映在曲线上,斜率就越大,所以ABCD四点化学反应速率的由快到慢顺序为D>C>B>A。
(4)5min后,收集到的气体体积不再增加,这说明反应物双氧水已经完全分解,不再产生氧气。
本题难度:一般
4、选择题 在反应C(s)+CO2(g)=2CO(g)中,能使反应速率加快的是
①增大压强 ②升高温度 ③将C粉碎 ④通CO2气体 ⑤加入足量木炭粉
A.①②③
B.①②④
C.①②③④
D.全部