微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 工业上用含80% FeS2的硫铁矿制取硫代硫酸钠,涉及到的化学反应如下(杂质不与O2、盐酸反应):
4FeS2+11O2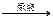 2Fe2O3+8SO2?①
2Fe2O3+8SO2?①
FeS2+2HCl→ FeCl2+H2S↑+S↓?②
2H2S+SO2→ 3S+2H2O?③
2NaOH+SO2→Na2SO3+H2O?④
Na2SO3+S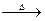 Na2S2O3?⑤
Na2S2O3?⑤
通过分析上述反应,进行计算:
(1)若在某密闭容器中加入150 g上述硫铁矿,并通入10 mol含氧气体积分数为0.4的富氧空气,按反应①充分反应后得到的气体中SO2的体积分数为__________(计算结果保留3位小数)。
(2)若以上各步反应的转化率均为100%,则150 g上述硫铁矿理论上最多可制得Na2S2O3___ g。
(3)若NaOH溶液吸收SO2的吸收率为90%,其它反应的转化率均为100%,则150 g上述硫铁矿最多可制得Na2S2O3多少g(写出计算过程,计算结果保留1位小数)?
(4)若反应②、④的转化率为90%,其它反应的转化率均为100%,要制得Na2S2O3最多,则原料中FeS2在反应①和②中的理论质量配比为多少(写出计算过程,计算结果保留3位小数)?
参考答案:(10分)
(1)0.216(2分)。(2)158 g(2分)。(3)149.7 g(3分)。(4)1.475(3分)
本题解析:略
本题难度:简单
2、选择题 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是

A.洗气瓶中没有看到明显现象
B.气体X是纯净物
C.洗气瓶中产生的沉淀是碳酸钡
D.Z导管口有红棕色气体出现
参考答案:D
本题解析:C+2H2SO4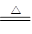 CO2↑+2SO2↑+2H2O 即:X为CO2和SO2混合气体;
CO2↑+2SO2↑+2H2O 即:X为CO2和SO2混合气体;
Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O 即Y为NO2
按题意,将三气体通入氯化钡溶液后:
NO2+SO2=NO+SO3? SO3+H2O=H2SO4? H2SO4+BaCl2=BaSO4↓+2HCl
可知:反应后的溶液呈强酸性,得到不溶于酸的BaSO4沉淀,但不能得到可溶于酸的BaSO3、BaCO3;同时CO2在强酸性溶液中不能存在,和NO一起逸出,而NO在瓶口可被氧化为NO2,而呈现红棕色
本题难度:一般
3、选择题 下列物质在一定条件下不能与SO2反应的是
A.Na2CO3溶液
B.Na2SO3溶液
C.CaCl2溶液
D.空气
参考答案:C
本题解析:略
本题难度:一般
4、选择题 下列有关二氧化硫的说法中,正确的是
A.检验SO2气体中是否混有CO2的方法是通入澄清石灰水中
B.SO2气体具有漂白性,能使品红溶液、紫色石蕊试液褪色
C.在含BaCl2的氨水中通入少量SO2气体会有白色沉淀生成
D.因为SO2气体具有还原性,所以在实验室不能用浓硫酸干燥SO2
参考答案:C
本题解析:考查SO2的性质
A:两者均可与澄清石灰水生成浑浊,不正确
B:使紫色石蕊试液褪色是由于该气体为酸性气体,溶于水生成亚硫酸的缘故,不正确
C:SO2+2NH3・H2O=2NH4++SO32-? SO32-+Ba2+=BaSO3↓,正确
D:由于两物质中硫的化合价相邻,不会发生氧化还原反应,故能用浓硫酸干燥SO2
答案为C
本题难度:一般
5、选择题 设计实验证明亚硫酸既有氧化性又有还原性,必选试剂是 (? )
A.盐酸、浓硫酸、氯化钡溶液
B.溴水、硫化钠溶液、稀硫酸
C.硝酸、硫化氢、氢氧化钠溶液
D.氧气、氯化钡溶液、水
参考答案:B
本题解析:略
本题难度:简单