微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在容积相同的不同密闭容器中内,分别充入同量的N2和H2,在不同温度下,任其发生反应: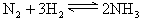 ,并分别在t0秒时测定其中NH3的体积分数[x(NH3)],绘成如图的曲线。
,并分别在t0秒时测定其中NH3的体积分数[x(NH3)],绘成如图的曲线。
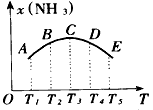
(1)A、B、C、D、E五点中,尚未达到化学平衡状态的点是_____________。
(2)此可逆反应的正反应是____热反应。
(3)AC段曲线是增函数,CE段曲线是减函数,试从化学反应速率和化学平衡角度说明理由。 _____________________________________
参考答案:
(1)A、B
(2)放热
(3)因为反应开始时,正反应速率大于逆反应速率,生成NH3的速度比消耗NH3速度要大,故NH3的体积分数[x(NH3)]不断增加,AC段曲线是增函数;而当达到平衡以后,温度升高.平衡逆向移动,故NH3的体积分数[x(NH3)不断减少,CE段曲线是减函数。
本题解析:
本题难度:一般
2、选择题 在体积可变的密闭容器中,反应mA(g)+nB(s)?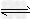 pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低.下列说法中,正确的是
pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低.下列说法中,正确的是
[? ]
A.(m+n)必定小于p?
B.(m+n)必定大于p
C.m必定小于p?
D.m必定大于p
参考答案:C
本题解析:
本题难度:一般
3、选择题 已知下列两个气态物质之间的反应:
C2H2(g)+H2(g)→C2H4(g)①
2CH4(g)→C2H4(g)+2H2(g)②
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:(Q1、Q2、Q3均为正值)
C(s)+2H2(g)===CH4(g) ΔH=-Q1Ⅰ
C(s)+1/2H2(g)===1/2C2H2(g) ΔH=-Q2Ⅱ
C(s)+H2(g)===1/2C2H4(g) ΔH=-Q3Ⅲ
Q值大小比较正确的是
[? ]
A.Q1>Q3>Q2?
B.Q1>Q2>Q3
C.Q2>Q1>Q3?
D.Q3>Q1>Q2
参考答案:A
本题解析:
本题难度:一般
4、填空题 在某2 L的密闭容器中加入0.1 mol碘单质和足量钨(W),在943 K时,发生反应W(s)+I2(g) 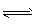 WI2(g),当I2的转化率为20%时,达化学平衡状态。
WI2(g),当I2的转化率为20%时,达化学平衡状态。
(1)反应从开始至平衡状态过程中用时20 s,其平均反应速率v(WI2)为________。
(2)943 K时,该反应的平衡常数K=________。
(3)若起始时,加入的碘为0.2 mol(其他条件不变)达平衡时容器中气体的体积比 V(I2)∶V(WI2)=________。
(4)在上述(1)平衡状态下,同时增加I2(g)和WI2(g)各0.02 mol(其他条件不变),化学平衡向________(填“正反应”或“逆反应”)方向移动,判断的依据是_____________。
参考答案:(1)5×10-4 mol・L-1・s-1
(2)0.25
(3)4∶1
(4)逆反应 ;Qc=0.4>K=0.25
本题解析:
本题难度:一般
5、选择题 下列各表述与示意图一致的是
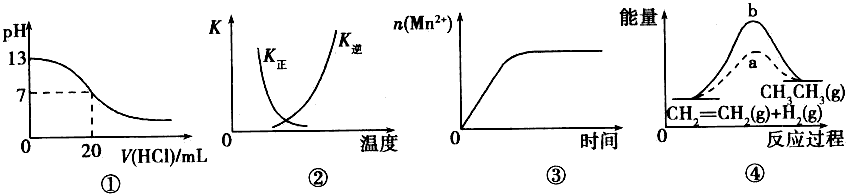
[? ]
A.图①表示25℃时,用0.1 moI・L-1盐酸滴定20 mL0.l mol・L-1NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应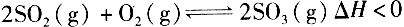 正、逆反应的平衡常数K随温度的变化
正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.0l moI・L-1 KMnO4酸性溶液与过量的0.l moI・L-1H2C2O4 溶液混合时,n(Mn2+)随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g) △H<0使用和未使用催化剂时,反应过程中的能量变化
参考答案:B
本题解析:
本题难度:一般