微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 如右图所示,两烧瓶中充入NO2气体,存在如下平衡:2NO2(g)?N2O4(g)△H<0;烧杯甲中盛放100mL?6mol?L-1的HCl溶液,烧杯乙中盛放100mL冷水,现向烧杯甲的溶液中放入25g?NaOH固体,同时向烧杯乙中放入25g?NH4NO3固体,搅拌使之溶解.
(1)A瓶中气体颜色______;简述理由______.
(2)B瓶中气体颜色______;简述理由______.
2、填空题 工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:
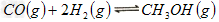
(1)判断反应达到平衡状态的依据是(填字母序号,下同)__________。
A.?生成 的速率与消耗CO的速率相等
的速率与消耗CO的速率相等
B.?混合气体的密度不变
C.?混合气体的相对平均分子质量不变
D.? 的浓度都不再发生变化
的浓度都不再发生变化
E.?气体的压强不再改变
(2)下表所列数据是反应在不同温度下的化学平衡常数(K)。

①由表中数据判断该反应的△H__________0(填“>”、“=”或“<”);
②某温度下,将 充入2L的密闭容器中,充分反应后,达到平衡时测得
充入2L的密闭容器中,充分反应后,达到平衡时测得
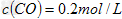 ,则CO的转化率为__________,此时的温度为__________。
,则CO的转化率为__________,此时的温度为__________。
(3)要提高CO的转化率,可以采取的措施是__________。
a.?升温 b.?加入催化剂 c.?增加CO的浓度 d.?恒容下加入? 使压强变大
e.?恒容下加入惰性气体使压强变大 f.?分离出甲醇
(4)在250℃时,某时刻测得该温度下的密闭容器中各物质的物质的量浓度见下表
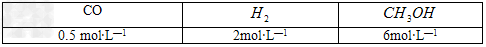
此时反应的正、逆反应速率的关系是:v(正)_________v(逆)(填“大于”“小于”或“等于”)。
(5)如图1所示,甲为恒容密闭容器,乙为恒压密闭容器。在甲、乙两容器中分别充入等物质的量的H2和CO,使甲、乙两容器初始容积相等。在相同温度下发生上述反应,并维持反应过程中温度不变。已知甲容器中CO的转化率随时间变化的图像如图2所示,请在图2中画出乙容器中CO的转化率随时间变化的图像。

3、选择题 在盛有足量A的体积可变的密闭容器中通入B,发生反应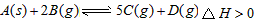 在一定温度、压强下达到平衡。平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法中正确的是
在一定温度、压强下达到平衡。平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法中正确的是
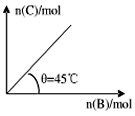
[? ]
A.平衡时B的转化率为60%
B.若再通入B,正逆反应速率均增大
C.在容器中加入少量A,则B的转化率增大
D.若保持压强一定,当温度升高时,图中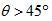
4、填空题 运用化学反应原理可以更好的分析化学反应的本质 。
(1)下列四组物质反应,其中与其它三组有本质不同的是_______。
A.Na2O2 + H2O
B.F2 + H2O
C.Cl2 + H2O
D.NO2 + H2O
(2)在 25℃下,向浓度均为 0.1mol・L-1 的NaCl和KBr混合溶液中逐滴加入硝酸银溶液,先生成_______沉淀 ( 填化学式 );当两种沉淀共存时溶液中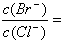 __________。(已知 25℃时 Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10)?
__________。(已知 25℃时 Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10)?
(3) 汽车尾气净化中的一个反应如下:2NO(g)+2CO(g) N2(g)+2CO2(g) 该反应混合体系中NO 的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
N2(g)+2CO2(g) 该反应混合体系中NO 的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
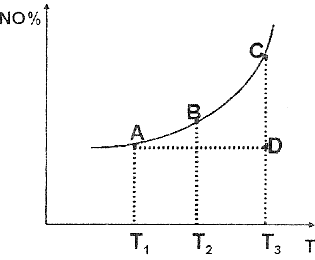
① 2NO(g)+2CO(g)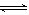 N2(g)+2CO2(g) 的△H _____0( 填 “>” 或 “<”)
N2(g)+2CO2(g) 的△H _____0( 填 “>” 或 “<”)
②若温度为Tl 、T2, 反应的平衡常数分别为 Kl、K2, 则K1_____K2;若反应进行到状态D 时,V正___V逆(填“>”、“<”或“=”)
③在恒容的密闭容器中,该反应达平衡后,改变某一条件,下列示意图不正确的是
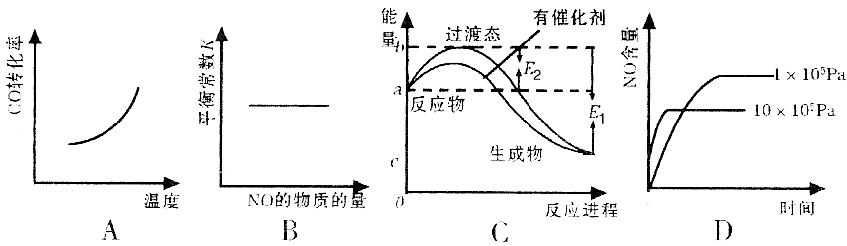
(4)分析下表提供的数据:
化学式
?电离常数
HClO
Ki=3×10-8
H2CO3
Ki1=4.3×10-7
H2CO3
Ki2=5.6×10-11
① 84 消毒液 ( 有效成分为 NaClO) 久置于空气中会失效,写出发生反应的离子方程式:____________; __________________。
②判断在等浓度的 NaClO、NaHCO3混合溶液中,各种离子浓度由大到小的顺序:_________________。
5、选择题 高温下某反应达到平衡,平衡常数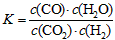 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
[? ]
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2O CO2+H2
CO2+H2