微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素
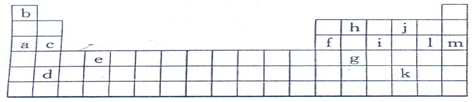
(1)下列?(填写编号)组元素的单质可能都是电的良导体。
①a、c、h?②b、g、k?③c、h、l?④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响。
原子核失去核外不同电子所需的能量(KJ・mol-1)
?
| 锂
| X
| Y
|
失去第一个电子
| 519
| 502
| 580
|
失去第二个电子
| 7 296
| 4 570
| 1 820
|
失去第三个电子
| 11 799
| 6 920
| 2 750
|
失去第四个电子
| ?
| 9 550
| 11 600
|
①通过上述信息和表中的数据分析,为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量?。
②表中X可能为13种元素中的?(填写字母)元素。用元素符号表示X和j形成的化合物的化学式? ?。
③Y是周期表中?族的元素。
④以上13种元素中,?(填写字母)元素原子失去核外第一个电子需要的能量最多。
(3)g元素原子基态时的核外电子排布式为______。
参考答案:(8分)(1)①④?(2)①Li原子失去1个电子后形成稳定结构,再失去1个电子很困难?②a;Na2O或Na2O2?③ⅢA?④? m?(3)1s22s22p63s23p63d104s24p2
本题解析:a~m元素分别为:Na、H、Mg、Sr、Ti、Al、Ge、C、P、O、Se、Cl、Ar
(1)电的良导体一般为金属或碳
(2)由电离能数据可看出,X最外层是一个电子,而且第一电离能小于锂,所以X可能为钠;同理Y最外层为3个电子,应该属于第IIIA元素;由于m(Ar)已经为稳定结构,其第一电离能最大
本题难度:一般
2、选择题 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Z为地壳中含量最高的金属元素。下列说法正确的是
?
A.工业上电解ZW3饱和溶液冶炼金属Z
B.元素X的最高正价与W的最高正价相同
C.简单离子半径的大小顺序:r(Y+)>r(X―)
D.Y、W的最高价氧化物的水化物均能溶解金属Z
参考答案:D
本题解析:短周期元素X、Y、Z、W分别为F、Na、Al、Cl。A、工业上电解熔融氧化铝制备金属铝,错误;B、氟元素没有负价,错误;C、两者电子层结构相同,钠离子质子数多半径小,错误;D、铝能与强酸和强碱反应,正确。
本题难度:一般
3、选择题 下列有关元素周期表中的某些推断正确的是
A?位于同一主族的元素的价电子数相同,则各元素的常见化合价也一定相同
B?碱金属族元素同卤族元素一样,其单质的熔沸点随元素原子序数的增大而逐渐升高
C?若x是ⅡB族中元素的原子序数, 那么原子序数为x+1的元素是ⅢA族
D?在周期表中金属和非金属元素的分界线附近的元素是过渡元素
参考答案:C
本题解析:A不正确,例如氟元素没有正价。B不正确,其单质的熔沸点随元素原子序数的增大而逐渐降低。D不正确,过渡元素位于元素周期表的中间,所以正确的答案选C。
本题难度:简单
4、选择题 和Ne原子电子层结构相同的微粒是(?)
A.Na+
B.Cl-
C.K+
D.Ar
参考答案:A
本题解析:Ne原子的结构示意图为 ,.Na+、Cl-、K+、Ar分别为
,.Na+、Cl-、K+、Ar分别为
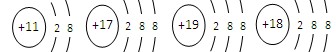
本题难度:简单
5、填空题 (共7分)有七种金属:钾、锌、铁、锡、铜、银、铂,它们的标号分别为A、B、C、D、E、F、G。①常温下,只有A和水反应生成氢气;②D、E、G都能和稀硫酸反应生成氢气,B、C、F无此性质;③C、F组成原电池时,F为正极;④在G的硫酸盐溶液中加入D,发现D溶解,G析出;⑤将G、E接触放置,E不易锈蚀;⑥以铂作电极,电解相同浓度的B和C的硝酸盐溶液时,在阴极上首先得到C,G在空气中放置极易生锈。则A是___?_,B是___?_,C是__?__,D是_?___,E是_?___,F是____?,G是____?
参考答案:A:K? B:Cu? C:Ag? D:Zn? E:Sn ?F:Pt? G:Fe
本题解析:考查金属性强弱比较。根据①可知A的金属性最强,所以A是K。根据③可知C的金属性强于F的。根据④可知,金属性是D强于G。根据⑤可知,金属性是E小于G。又因为G易生锈,所以G是铁,因此根据②可知,D是Zn,E是Sn。根据⑥可知B的金属性强于C,所以根据②可知Cu,C是Ag,F是Pt。
本题难度:一般