微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述不正确的是
[? ]
A.原电池是将化学能转化为电能的装置
B.铁船底镶嵌锌块,锌作负极,以防船体被腐蚀
C.钢铁腐蚀的正极反应:Fe→Fe3++3e-
D.用惰性电极电解CuSO4溶液一段时间后,向其中加入CuO固体可以使溶液恢复到原来的浓度
参考答案:C
本题解析:
本题难度:一般
2、填空题 (10分)在玻璃圆筒中盛有两种无色的互不相溶的中性液体,上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图.接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成.停止通电,取出电极,用搅棒上下剧烈搅动.静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色.根据上述实验回答:
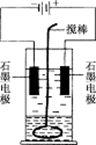
(1)阳极上的电极反应式为________.
(2)阴极上的电极反应式为________.
(3)原上层液体是________.
(4)原下层液体是________.
(5)搅拌后两层液体颜色发生变化的原因是__________________________________.
(6)要检验上层液体中含有的金属离子,其方法是______________________________,现象是__________________________________.
参考答案:(1)2I--2e-===I2?(2)2H++2e-===H2↑
(3)KI(或NaI等)水溶液?(4)CCl4(或CHCl3等)
(5)I2在CCl4中的溶解度大于在水中的溶解度,所以绝大部分I2都转移到CCl4中
(6)焰色反应 透过蓝色钴玻璃观察火焰呈紫色(其他合理答案同样给分.例如,若③中答NaI水溶液,这里答火焰呈黄色)
本题解析:本题是以电解知识为主干,考查了电极反应方程式的书写以及电解原理的应用。但在此实验试题中实际上隐含了对实验基本知识(如萃取原理、焰色反应)的考查,同时在试题中推测溶液的成分富有一定的开放性,而本实验试题的解题的突破口是对实现现象的分析。本题通过溶液分层现象及上层溶液能进行电解可以推断上下两层溶液为无机试剂和有机试剂,通过阳极周围溶液颜色的变化及静置后下层液体显紫色可以推测电解溶液为碘盐溶液,再根据溶液为中性,可进一步推测电解液应为中学中常见的钠盐或钾盐溶液。再根据电极反应方程式的书写规律和基本实验的分析可以顺利完成试题中的问题。
本题难度:一般
3、填空题 (14分)纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
方法Ⅰ
| 用炭粉在高温条件下还原CuO
|
方法Ⅱ
| 电解法:2Cu+H2O 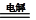 Cu2O+H2↑ Cu2O+H2↑
|
方法Ⅲ
| 用肼(N2H4)还原新制Cu(OH)2
|
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是反应条件不易控制,若控温不当易生成 而使Cu2O产率降低。
(2)已知:①C(s)+O2(g)=CO2(g) △H=akJ・mol―1;
②2CO(g)+O2(g)=2CO2(g) △H=bkJ・mol―1;
③2Cu2O(s)+O2(g)=4CuO(s) △H=ckJ・mol―1.
方法Ⅰ制备过程会产生有毒气体,写出制备反应的热化学方程式 。
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为 。
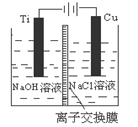
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为 。
(5)方法Ⅲ可以用甲醛稀溶液替代肼,但因反应温度较高而使部分产品颗粒过大, (填操作名称)可分离出颗粒过大的Cu2O。
(6)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的Cu2O分别进行催化分解水的实验:
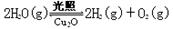
参考答案:
本题解析:
本题难度:困难
4、选择题 用含锌、银杂质的粗铜作阳极,纯铜作阴极,CuSO4溶液做电解液进行电解,下列有关电解液中Cu2+物质的量浓度的叙述中,正确的是
A.c(Cu2+)增大
B.c(Cu2+)减小
C.c(Cu2+)不变
D.无法确定