微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol,同温下,向体积相同的密闭容器甲、乙中分别充入2molSO2、1molO2和1molSO2、0.5molO2,当反应分别达平衡时放出的热量分别为Q1和Q2(单位为kJ),则下列比较正确的是( )
A.Q2=0.5Q1<98.5
B.Q2<0.5Q1=98.5
C.0.5Q1<Q2<98.5
D.Q2<0.5Q1<98.5
参考答案:D
本题解析:
本题难度:简单
2、填空题 标准状况下,1.68L无色可燃气体在足量氧气中完全燃烧。若将产物通过足量的澄清石灰水,得到的白色沉淀质量为15.0g;若用足量碱石灰吸收燃烧产物,增重9. 3g。
(1)计算燃烧产物中水的质量为___________g。
(2)若气体是单一气体,它完全燃烧放出的热量是____________。
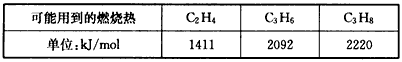
(3)若原气体是两种等物质的量的气体混合物,其中一种是烃,另一种气体的燃烧热为287kJ/mol,混合气体完全燃烧共放热94kJ,则该烃燃烧的热化学方程式为____________________。
参考答案:(1)2.7
(2)105.8kJ
(3)C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) △H=-2220kJ/mol
本题解析:
本题难度:一般
3、填空题 煤燃烧的反应热可通过以下两个途径来利用:
a.利用煤在充足的空气中直接燃烧产生的反应热;
b.先使煤与水蒸气反应得到氢气和一氧化碳,再将得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式分别为:
a. C(s)+O2(g)==CO2 (g) △H =E1 ①
b. C(s)+H2O(g)==CO(g)+H2 (g) △H =E2 ②
H2(g)+1/2O2(g)==H2O(g) △H=E3 ③
CO(g)+1/2O2(g)==CO2 (g) △H =E4 ④
请回答:
(1)根据两种途径,下列说法错误的是 ( )
A.途径b制水煤气时增加能耗,故途径b的做法不可取
B.与途径a相比,途径b可以减少对环境的污染
C.与途径a相比,途径b可以提高煤的燃烧效率
D.将煤转化为水煤气后,便于通过管道进行运输
(2)上述四个热化学方程式中哪个反应△H>0?____(填序号)。
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是 (? ?)
A.a比b多
B.a比b少
C.a与b在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为________。
参考答案:(1)A
(2)②
(3)C
(4)E1=E2+E3+E4
本题解析:
本题难度:一般
4、选择题 现有CO、H2和CO2组成的混合气体116. 8L(标准状况),经完全燃烧后放出的总能量为867.9kJ,并生成18g液态水。已知2H2(g)+O2(g)=2H2O(l) △H=-571. 6kJ/mol;2CO(g)+O2(g)=2CO2(g) △H=-566kJ/mol。则燃烧以前混合气体中CO的体积分数最接近于
[? ]
A.80%
B.60%
C.40%
D.20%
参考答案:C
本题解析:
本题难度:一般
5、填空题 CO、CH4均为常见的可燃性气体。
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是______________。
(2)已知在101 kPa时,CO的燃烧热为283 kJ/mol。相同条件下,若2 molCH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30 倍,CH4完全燃烧反应的热化学方程式是:_____________ 。
(3)120℃、101 kPa下,a mL由CO、CH4组成的混合气体在bmL O2中完全燃烧后,恢复到原温度和压强。 ① 若混合气体与O2恰好完全反应,产生b mL CO2,则混合气体中CH4的体积分数为____________ (保留2位小数)。
② 若燃烧后气体体积缩小了a/4 mL ,则a与b关系的数学表示式是______________ 。
参考答案:(1) 转移的电子数之比是 1:4 。
(2) 热化学方程式是:CH4(g) + 2O2(g) == CO2(g) +2H2O(l) ΔH= -891.45 kJ・mol-1
(3)①体积分数为 33.33% (保留2位小数)。
②a与b关系式 b≥5/4a
本题解析:
本题难度:一般