��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��14�֣���ҵ������CO��ˮ������һ�������·�����Ӧ��ȡ������
CO(g)��H2O(g)  ?CO2(g)��H2(g)?��H����41 kJ/mol
?CO2(g)��H2(g)?��H����41 kJ/mol
ijС���о�����ͬ�¶��¸÷�Ӧ�����е������仯�����Ƿֱ��������ΪV?L���������º����ܱ������м���һ�����ķ�Ӧ�ʹ������ͬ�¶��·�����Ӧ������������£�
�������
| ��ʼʱ���������ʵ���/mol
| �ﵽƽ���ʱ��/min
| ��ƽ��ʱ��ϵ�����ı仯/kJ
|
CO
| H2O
| CO2
| H2
|
��
| 1
| 4
| 0
| 0
| t1
| �ų�������32.8 kJ
|
��
| 2
| 8
| 0
| 0
| t2
| �ų�������Q
|
| | | | | | |
|
��1���÷�Ӧ�����У���Ӧ����ӻ�ѧ������ʱ�����յ�������?������ڡ�����С�ڡ����ڡ�����������ӻ�ѧ���γ�ʱ���ͷŵ���������
��2���������з�Ӧ��ƽ��ʱ��CO��ת����Ϊ?%��
��3�������������з�Ӧ��ƽ�ⳣ��K=?��
��4������������ȷ���� ?������ĸ��ţ���
a��ƽ��ʱ����������H2������������
b���������з�Ӧ��ƽ��״̬ʱ��Q > 65.6 kJ
c����Ӧ��ʼʱ���������з�Ӧ�Ļ�ѧ��Ӧ�������
d���������У���Ӧ�Ļ�ѧ��Ӧ����Ϊ��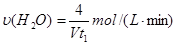
��5����֪��2H2 (g) + O2 (g) ="=" 2H2O (g)?��H����484 kJ/mol��д��CO��ȫȼ������CO2���Ȼ�ѧ����ʽ��?��
��6���������з�Ӧ���е�t minʱ����û��������CO2�����ʵ���Ϊ0.6 mol������
200 mL 5 mol/L��NaOH��Һ������ȫ���գ���Ӧ�����ӷ���ʽΪ����һ�����ӷ���ʽ��ʾ��?��
�ο��𰸣���1��С�ڣ���<�����۷֣�?��2��80?��3��1?��4��a
��5��2CO(g) + O2(g) ="==" 2CO2(g)?��H =" -566" kJ/mol?
��6��3CO2 + 5OH- ="==" 2CO32- + HCO3- + 2H2O
�����������1���÷�Ӧ�Ƿ��ȷ�Ӧ����Ӧ����ӻ�ѧ������ʱ�����յ�������С����������ӻ�ѧ���γ�ʱ���ͷŵ���������
��2���������з�Ӧ��ƽ��ʱ���ų�����Ϊ32.8 kJ����Ϊ1molCO��ȫת��ʱ�ų�������41 kJ��˵��ת����COΪ32.8/41=0.8����CO��ת����Ϊ80%��
��3����Ϊ�¶�û�б仯�����������������з�Ӧ��ƽ�ⳣ����ȫһ�����������з�Ӧ��ƽ�ⳣ��Ϊ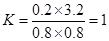 ������������K=1��
������������K=1��
��4����Ϊ����ƽ����¶���ͬ����������ɱ������ﵽƽ��ʱ�����ʵ���Ҳ�ɱ������ӣ���������H2�����������ȣ��������з�Ӧ��ƽ��״̬ʱ���ų��������������ٵ�2����Q ="65.6" kJ�������ڵ�Ũ�ȴ�ѧ��Ӧ����Ҫ���������У���Ӧ�Ļ�ѧ��Ӧ����Ӧ����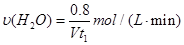 ��
��
��5��CO(g)��H2O(g)  ?CO2(g)��H2(g)����H����41 kJ/molΪ�٣�2H2 (g) + O2 (g) ="=" 2H2O (g)����H����484 kJ/molΪ�ڣ��١�2+�ڼ����Դﵽ����ʽ2CO(g) + O2(g) ="==" 2CO2(g)����H =" -566" kJ/mol��
?CO2(g)��H2(g)����H����41 kJ/molΪ�٣�2H2 (g) + O2 (g) ="=" 2H2O (g)����H����484 kJ/molΪ�ڣ��١�2+�ڼ����Դﵽ����ʽ2CO(g) + O2(g) ="==" 2CO2(g)����H =" -566" kJ/mol��
��6��CO2�����ʵ���Ϊ0.6 mol��1 mol��NaOH��Һ������ȫ��Ӧ���������CO32-�� HCO3-�����ݷ�Ӧ������ʵ���֮�ȿ���д������ʽΪ3CO2 + 5OH- ="==" 2CO32- + HCO3- + 2H2O��
��������������ȡ����Ϊ���壬���ؿ��黯ѧ��Ӧ���ʡ���ѧƽ�⼰�Ȼ�ѧ����ʽ������֪ʶ���ۺ��Խ�ǿ�������ѶȽϴ��ϰ�⡣
�����Ѷȣ�һ��
2�������� ij�¶��£Σ��ϣ��ͣΣϣ�֮�佨�������µ�ƽ��Σ��ϣ�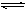 2�Σϣ������ƽ������Կ���������ܶ�Ϊ2��644����Σ��ϣ��ķֽ��ʡ�
2�Σϣ������ƽ������Կ���������ܶ�Ϊ2��644����Σ��ϣ��ķֽ��ʡ�
�ο��𰸣��Σ��ϣ��ķֽ���Ϊ20����
�����������Σ��ϣ�����ʼ���ʵ���Ϊ1
����ת���˵ģΣ��ϣ����ʵ���Ϊ��
����?�Σ��ϣ�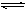 2�Σϣ�
2�Σϣ�
������ʼ���ʵ���?1?0
����ת�����ʵ���?��?2��
����ƽ�����ʵ���?1����?2��
����ƽ��ʱ�������������ʵ���Ϊ
�������ܣ�1������2����1����
������ ��29���ģ�29��2��644��76��68
��29���ģ�29��2��644��76��68
������֪�Σ��ϣ��ͣΣϣ�����Է��������ֱ�Ϊ92��46�����У�
����76��68����92����1��������46��2����1������
��������0��2�����
������Σ��ϣ��ķֽ���Ϊ����0��2��1����100����20��
�����Ѷȣ���
3������� һ�������£����Ϊ1 L���ܱ������з������·�Ӧ��SiF4(g)��2H2O(g) SiO2(s)��4HF(g)����H����148.9 kJ��mol��1��
SiO2(s)��4HF(g)����H����148.9 kJ��mol��1��
(1)���и�������˵���÷�Ӧ�Ѵﻯѧƽ��״̬����________(����ĸ���)��
a��v����(SiF4)��4v����(HF)
b������������ѹǿ���ٱ仯
c����������������������ٱ仯
d��HF������������ٱ仯
(2)��Ӧ�����вⶨ�IJ����������±�(����t2��t1)��ʾ��
��Ӧʱ��/min
| n(SiF4)/mol
| n(H2O)/mol
|
0
| 1.20
| 2.40
|
t1
| 0.80
| a
|
t2
| b
| 1.60
|
ͨ��a��b��ֵ����ѧƽ��ԭ��˵��t1ʱ��Ӧ�Ƿ�ﵽ��ѧƽ��״̬��________��
(3)��ֻ�ı�һ������ʹ������Ӧ�Ļ�ѧƽ�ⳣ����÷�Ӧ________(�����)��
a��һ��������Ӧ�����ƶ�
b��һ�����淴Ӧ�����ƶ�
c��һ���Ǽ�Сѹǿ��ɵ�
d��һ���������¶���ɵ�
e��SiF4��ƽ��ת����һ������
�ο��𰸣�(1)bcd
(2)a��1.60(��b��0.80)��˵����һ�������£�t1��t2ʱ����ֵ�Ũ��(�����ʵ���)���Ѳ��ٷ����ı䣬��t1ʱ��Ӧ�Ѿ��ﵽ��ѧƽ��״̬
(3)ade
���������(2)0��t1 min����Ӧ���ĵ�SiF4Ϊ0.40 mol��������֪��Ӧ��ȷ�����ĵ�H2OΪ0.80 mol����a��1.60 mol��t2 minʱ��H2O��Ϊ1.60 mol����b��0.80 mol���ɴ˿��ж�t1ʱ�÷�Ӧ�Ѿ��ﵽ��ѧƽ��״̬��
�����Ѷȣ�һ��
4������� ��ÿ��2�֣���16�֣�������ʵ����գ�
��1����25�桢101kPa�£�1g�״�Һ����ȫȼ������CO2��Һ̬ˮʱ����22.68kJ�����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ_____________________________?
��2����֪��1molH��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ_________________?
��3������ȼ�ϵ�������ں���ɻ�����30%KOH��ҺΪ����ʵ����ֵ����ʹ��ʱ�ĵ缫��Ӧʽ��?������?��������??
(4)��25��ʱ���ܱ�������X��Y��Z��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±���
����
| X
| Y
| Z
|
��ʼŨ��/mol��L-1
| 0.1
| 0.2
| 0
|
ƽ��Ũ��/mol��L-1
| 0.05
| 0.05
| 0.1
|
�÷�Ӧ�ķ�Ӧ����ʽ�ɱ�ʾΪ??��ƽ��ʱY�����ת����?��
��5��ij����AZX���Ȼ���XCl2 1.11 g�����Һ������1mol��L-1����������Һ20 ml���ܰ���������ȫ������������X��������Ϊ?����X�ĺ���������Ϊ20����37 g XCl2���������ӵ����ʵ���?��
�ο��𰸣�(1) CH3OH(l)+ O2(g)��CO2(g)+2H2O(l)?��H���C725.76kJ��mol��1
O2(g)��CO2(g)+2H2O(l)?��H���C725.76kJ��mol��1
��2��N2(g)+3H2(g)=2NH3(g)?��H����92kJ��mol��1
��3��O2��2H2O��4e-==4OH- ?2H2��4OH-��4e-==4H2O
(4) X+3Y  ?2Z? 75%
?2Z? 75%
(5) 40 ;? 18mol
�����������
�����Ѷȣ�һ��
5������� ��һ�������£����淴ӦA2(g)+B2(g)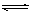 2C(g)��һ���ܱ������дﵽƽ��ʱ,���c(A2)=0��5mol��L-1��c(B2)=0��1mol��L-1��c(C)=1��6mol��L-1����
2C(g)��һ���ܱ������дﵽƽ��ʱ,���c(A2)=0��5mol��L-1��c(B2)=0��1mol��L-1��c(C)=1��6mol��L-1���� ��
��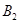 ��C����ʼŨ�ȷֱ�Ϊa mol��L-1��b mol��L-1��g mol��L-1��ȷ����
��C����ʼŨ�ȷֱ�Ϊa mol��L-1��b mol��L-1��g mol��L-1��ȷ����
(l)a��gӦ����Ĺ�ϵʽΪ_____________��
(2)����Ӧ������Ӧ����ʼ���У���g=_________,a�����ֵΪ__________��
(3)����Ӧ���淴Ӧ����ʼ���У���b=_________��a����СֵΪ_________��
(4)b��ȡֵ��ΧΪ___________________��
�ο��𰸣���1��a+g�M2=1��3��2��0? 1��3��3��0? 0��4��4��0��b��0��9
�����������1������Ŀ�����ķ�Ӧƽ����˵�����ĵ�Ч��ʼ״̬Ϊc(A2)=1��3mol��L-1��c(B2)=0��9mol��L-1��c(C)=0mol��L-1����c(A2)=0��4mol��L-1��c(B2)=0mol��L-1��c(C)=1��8mol��L-1������A2 ��B2��C����ʼŨ�ȷֱ�Ϊa mol��L-1��b mol��L-1��g mol��L-1�ɿ���C��g mol��L-1�����ķ�Ӧ������ģ���Чת����ȥ��a+g�M2=1��3? b+g�M2=0��9������Ӧ���淴Ӧ����ʼ����a��b�Ĺ�ϵ��a-b=0��4��2b+g=1��8��2������Ӧ������Ӧ����ʼ���У���a+g�M2=1��3��֪��g=0ʱ��aȡ���ֵ�����Ϊ1��3�� (3)����Ӧ���淴Ӧ����ʼ���У�����һ����Ч��ʼ״̬c(A2)=0��4mol��L-1��c(B2)=0mol��L-1��c(C)=1��8mol��L-1��֪����b=0ʱ��aȡ��Сֵ��Ϊ0��4��(4)��������������֪������ʼ��bȡ���ֵ��������ʼ��bȡ��Сֵ������b��ȡֵ��Χ��0��b��0��9��
�����Ѷȣ�һ��