��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ���е����ʵ�����Mg��Al�Ļ����a g��100 ml���ᷴӦ,������������Ա�״�����㣩
��1�����û������Mg��Al��������Ϊ?
��2�����������������ǡ����ȫ��Ӧ���������Ũ��Ϊ?
��3���������Ӧ�������ʣ�࣬����㣬Ҫ��������H2�����������Ҫ֪��?
�ο��𰸣�
��1����������Ϊ 8:9?��2���������Ũ��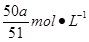
��3��������Ҫ֪�������Ũ�Ȼ�����������
��4����H2�����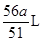
��5������Χ?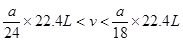
���������
(1)��Mg��XgAl��Yg������X24=Y/27,��֪X:Y=8:9
(2)���ݵ���غ�ɵã�Mg��Mg2+��Al��Al3+ �����У�[(8/17/24)2+(9/17/27)3]a/0.1=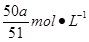
(3)H2�е���ȫ�����������ᣬ����ֻ��֪����������ʵ������Ϳ�֪�����ɵ�������������������֪�������������ֻ��֪�������Ũ�ȼ��ɡ�
�����������漰���˻�������ᷴӦ�Ķ������㣬�����Ѷ�������ѧ���ڽ���ʱ�������÷���ʽ����������Ҫ����Ԫ���غ㣬����غ�ȡ�
�����Ѷȣ���
2������� ��R�Ļ�ѧʽΪXmYbZp��X��Y��ZΪ���ֲ�ͬ���ӣ��������Ԫ�ؾ�Ϊ������Ԫ�أ�ȡ���ݵ�������Ũ��R��ˮ��Һ��5 mL��������ʵ�飺
I��ȡһ��R��ˮ��Һ�������Ba(OH)2��Һ��Ӧ����Ӧ���������ɰ�ɫ�����������������Ӻ���٣�����ʣ�������2.33 g���Ҽײ�����ϡ���ᡣ
��ȡ��һ��R��ˮ��Һ�������NaOH��Һ��ϼ��ȣ����ɾ��д̼�����ζ��������0.112 L����״����������ʹʪ��ĺ�ɫʯ����ֽ������
�ݴ˻ش�
(1)д��R�ͼĻ�ѧʽ��R___����____��
(2)��ȡ1 LR��ˮ��Һ����������μ���NaOH��Һ�����ó��������NaOH�����ʵ�����ϵ��ͼ��ʾ����
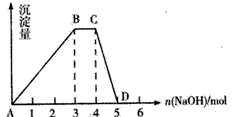
��R��Һ�����ʵ���Ũ��Ϊ____��
��BC�α�ʾ�ĺ�����____��
��CD�η�Ӧ�����ӷ���ʽΪ____��
�ο��𰸣�(1)NH4Al(SO4)2 �� BaSO4
(2)��1 mol��L-1
��NH4+��OH -�������NH3��H2O
��Al(OH)3+OH-==AlO2-+2H2O
���������
�����Ѷȣ�һ��
3��ѡ���� 14gͭ�����Ͻ���������ijŨ�ȵ����ᷴӦ�����ų���������1.12L����״���£�������ϣ�ͨ��ˮ��ǡ��ȫ�������գ���Ͻ���ͭ������Ϊ (? )
A��9.6g
B��6.4g
C��3.2g
D��1.6g
�ο��𰸣�C
���������n(O2) =" 1.12/22.4" =" 0.05mol" �� 0.05mol O2��Ӧ�õ�0.05��4 = 0.2mol����
��NO��NO2��O2��Ӧ��ʧȥ0.2mol���ӣ���Cu��Ag��HNO3��Ӧ��ʧȥ0.2mol���ӣ���ʧ�����غ㣩�������У�2��n(Cu) + n(Ag) = 0.2mol���������غ�ã��У�64��n(Cu) + 108��n(Ag) =" 14g" �����n(Cu) = 0.05mol����m(Cu) = 64��0.05 =" 3.2g" ��ѡC
����������������û�ѧ����ʽ����⣬������̽���ܸ��ӣ�������������غ����ʧ�����غ㣬����ܺõļ��㡣
�����Ѷȣ���
4������� ��0.1molþ�����Ͻ�����100mL2mol/L��H2SO4��Һ�У�Ȼ��μ�1mol/L��NaOH��Һ�����ɳ���������NaOH��Һ����Ĺ�ϵ��ͼ��ʾ���Իش��������⣺
��1������Һ��Mg2+��Al3+ǡ�ó�����ȫʱ��V��NaOH��=______mL��
��2����V1=160mLʱ��������ĩ��þ�����ʵ���Ϊ���٣���ʱV2��ֵ���Ƕ��٣�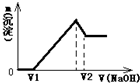
�ο��𰸣���þ�����Ͻ�����H2SO4��Һ�У�������Ӧ��Mg+H2SO4=MgSO4+H2����2Al+3H2SO4=Al2��SO4��3+3H2����0.1molþ�����Ͻ���ȫ��Ӧ��Ҫ���᷶Χ��0.1mol��n��H2SO4����0.15mol��H2SO4��ʣ�ࣨ�۲�ͼ������ó�������Һ��MgSO4��
Al2��SO4��3��H2SO4���Һ��
��0--V1�Σ��μӵ�NaOH�����к�ʣ���H2SO4��������Ӧ�ǣ�H2SO4+2NaOH=Na2SO4+2H2O
��V1mlʱ��ʣ���H2SO4��μӵ�NaOHǡ����ȫ��Ӧ����Һ��MgSO4��Al2��SO4��3��Na2SO4���Һ��
��V1--���������Σ������μӵ�NaOH��MgSO4��Al2��SO4��3��Ӧ������������������Ӧ��
Al2��SO4��3+6NaOH=2Al��OH��3��+3Na2SO4��MgSO4+2NaOH=Mg��OH��2��+Na2SO4
�ܳ��������ʱʱ��MgSO4��Al2��SO4��3��ȫ��Ӧ�������ﵽ���ֵ����ʱ����Һ��Na2SO4��Һ��
�ݳ��������--V2ml�Σ������μӵ�NaOH��Al��OH��3��Ӧ����������ʼ���٣�������Ӧ��Al��OH��3+NaOH=NaAlO2+2H2O
��V2mlʱ��Al��OH��3��ȫ��Ӧ��������Mg��OH��2����Һ��Na2SO4��NaAlO2���Һ��
��1������Һ��Mg2+��Al3+ǡ�ó�����ȫʱ���������ﵽ���ֵ����ʱ����Һ��Na2SO4��Һ������SO42-���Ӻ�Na+�����غ��У�n��Na+��=2n��Na2SO4��=2n��H2SO4��=2��0.1L��2mol/L=0.4mol�����ԣ���ʱ��V��NaOH��=0.4mol1mol/L=0.4L=400ml
�ʴ�Ϊ��400��
��2����V1=160mLʱ����ʱ����Һ��MgSO4��Al2��SO4��3��Na2SO4���Һ��
��Na+�����غ��֪��n��Na2SO4��=12n��Na+��=12n��NaOH��=12��0.16L��1mol/L=0.08mol
��MgSO4Ϊxmol��Al2��SO4��3Ϊymol������Mgԭ�ӡ�Alԭ�ӡ�SO42-�����غ��У�
���������
�����Ѷȣ�һ��
5��ѡ���� �ס������ձ��зֱ�ʢ��10mL?1mol?L-1AlCl3��Һ���ڼ��ձ��м���һ����NaOH��Һ�����ձ��м���������NaOH��Һ���������pH�İ�ˮ�������й������ձ���˵���У���ȷ����
A.���в����ij���һ�������ж�
B.���в����ij���һ���ȼ��ж�
C.���Ҳ����ij���һ��һ����
D.�����в����ij�������һ����
�ο��𰸣�D
��������������������������������ʣ����������������Ƶ������ڰ�ˮ���ʿ�ʼ����ʱ�����ձ������ɵĶ�����������������
��ͬ�������ͬpH������Һ�е�����һˮ�ϰ������������ƣ�
�����߾�������ʱ�����ɵij�����ˮ�ࣻ
��ˮ�������������Ʋ�����ʱ�����ɵij�����ˮ�ࣻ
��ˮ��������������ǡ��ʱ�����ɵij���һ���ࣻ
��ˮ���������ƶ�����ʱ�����ɵij�����ˮ�࣮
�����ˮ��NaOH��Һ�У�������10mL?0.1mol?L-1?AlCl3��Һ������������������������ˮΪ������ʣ����ֵ��룬��������Ϊǿ����ʣ���ȫ���룬��ͬ�������ͬpH�İ�ˮ��NaOH��Һ�е�����һˮ�ϰ������ʵ��������������Ƶ����ʵ�����
�����߶�������ʱ�����ɵ�������������������һˮ�ϰ�������������������һˮ�ϰ������ʵ��������������Ƶ����ʵ��������Լ��г��������е��٣�
?����ˮ�������������Ʋ���ʱ���������ɵ��������������ʵ���Ϊ10mL��10-3L/mL��0.1mol?L-1=0.001mol���������ɵ��������������ʵ���С��0.001mol�����Լ��г����������٣�
����ˮ��������������ǡ��ʱ�����ɵij���ȡ�����Ȼ������Ȼ���������ȣ����Լ��������ɵij���һ���ࣻ
����ˮ���������ƶ�����ʱ�������������������������Ƶ������ڰ�ˮ���������ɵ���������Ϊ0.001mol���������ɵ������������ڹ������������ƣ�������������С��0.001mol�����Լ��г����������٣�
ͨ�����Ϸ���֪�����г������ڻ�������г�������ABC����D��ȷ��
��ѡD��
���������⿼���������������ʡ���ѧ����ȣ�������ʱ�������������������ʲ������۵ķ������н������ȷ���зֶ��ǽⱾ��Ĺؼ����ѶȽϴ�
�����Ѷȣ�һ��