微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如图中M、N为含X元素的常见化合物,则? X元素为羧
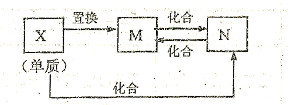
A.C或Al
B.Cu或Fe
C.N或S
D.Fe或C
参考答案:D
本题解析:略
本题难度:一般
2、填空题 W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为?。
(2)W与Y可形成化合物W2Y,该化合物的电子式为?。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为?
?。
(4)比较Y、Z气态氢化物的稳定性:?>?(用分子式表示)。
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是?>?>
?>?。
参考答案:(每空1分,共5分)
(1)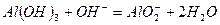 ?(2)
?(2)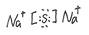
(3)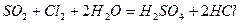 (4)? HCl、H2S(填写完整给分,否则零分)
(4)? HCl、H2S(填写完整给分,否则零分)
(5)S2―、Cl―、Na+、Al3+?(填写完整给分,否则零分)
本题解析:略
本题难度:简单
3、选择题 今有A、B两种原子,已知A原子的核外电子总数是B原子核外电子总数的1/2倍,B原子的L层电子数为A原子L层电子数的2倍,A和B分别是(?)
A.硼和氦? B.碳和镁? C.氯和碳? D.铍和氧
参考答案:B
本题解析:A原子的核外电子总数是B原子核外电子总数的1/2倍,B原子的L层电子数为A原子L层电子数的2倍,B原子的L层已经全部排满,则A是碳元素,所以B是镁元素,答案选B。
本题难度:一般
4、选择题 关于碱金属单质的性质叙述错误的是(?)
A.在空气中燃烧都能生成过氧化物
B.都能够与水反应
C.都有较强的还原性
D.最高价氧化物对应水化物都是强碱
参考答案:A
本题解析:锂在空气中燃烧生成Li2O,故A错误
本题难度:一般
5、填空题 (12分)下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
?
| ⅠA
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
| 0
|
1
| A
| ?
|
2
| ?
| ?
| ?
| D
| E
| K
| G
| ?
|
3
| B
| ?
| C
| J
| F
| ?
| H
| I
|
(1)表中元素,化学性质最不活泼的是?;可用于制半导体材料的元素是_______; 非金属性最强的是?。
(2)最高价氧化物的水化物碱性最强的是?,该物质的水溶液与C最高价氧化物的水化物反应的离子方程式是?
H最高价氧化物的水化物是?
(3)由A、K两种元素组成的含10个电子的化合物的结构式是?,
B的氧化物的电子式是?,该氧化物属于?晶体。
参考答案:(1)Ar? Si? F (2)NaOH?略? HClO? (3)H-O-H;? ; 离子
本题解析:
?
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
0
1
H
?
2
?
?
?
C
N
O
F
?
3
Na
?
Al
Si
P
?
Cl
Ar
(1) Ar是惰性气体元素,化学性质最不活泼;Si在周期表中位于金属、非金属的分界线处,既表现金属的性质,又表现非金属的性质,故可用作半导体材料;同周期,由左到右,元素的非金属性逐渐增强,同主族,由上到下,元素的非金属性逐渐减弱,故非金属性最强的是F;
(2)同主族,由上到下,原子的失电子能力逐渐增强,则最高价氧化物对应水化物的碱性逐渐增强,同周期,由左到右,原子的失电子能力逐渐减弱,则最高价氧化物对应水化物的碱性逐渐减弱,则最高价氧化物的水化物碱性最强的是NaOH;Al(OH)3+OH-=[Al(OH)4]-;
(3)水分子中氧原子与每个氢原子间共用1对电子,从而使氢原子达2电子稳定结构,氧原子达8电子稳定结构,故水分子的结构式为? H-O-H;氧化钠的电子式为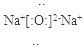
由Na+、O2-离子按一定比例组成的晶体,故属离子晶体;
本题难度:一般