微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,向10mL 0.1 mol・L-1NaOH溶液中逐滴加入0.1 mol・L-1醋酸溶液,所得滴定曲线如下图所示。下列说法正确的是?(?)
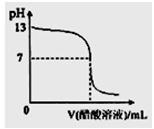
A.pH=7时,所加醋酸溶液的体积为10mL
B.pH<7时,溶液中:c(CH3COO-)>c(Na+)
C.7<pH<13时,溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.继续滴加0.1 mol・L-1醋酸溶液,溶液pH可以变为1
参考答案:B
本题解析:当NaOH溶液和醋酸恰好完全反应时,生成醋酸钠水解而使溶液显碱性,故A错。当pH<7时有c(H+)>c(OH-),根据电荷守恒可得c(CH3COO-)>c(Na+),故B正确。当7<pH<13时,溶液也有c(Na+)> c(OH-)> c(CH3COO-)>c(H+)这一种情况,C错。对于选项D可作一极端设想,若溶液就是0.1 mol・L-1醋酸,由于醋酸是弱酸,溶液的pH也大于1,故D也错。
本题难度:一般
2、选择题 关于用水制取二级能源氢气,以下研究方向正确的是(?)
A.构成水的氢和氧都是可以燃烧的物质,因此,可研究在水不分解的情况下,使氢成为二级能源
B.设法将太阳光聚集,产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放能量
D.寻找特殊化学物质,用于开发廉价能源,以分解水制取氢气
参考答案:BD
本题解析:略
本题难度:简单
3、选择题 室温下,将1.000 mol・L-1盐酸滴入20.00 mL 1.000 mol・L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。
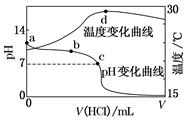
下列有关说法正确的是( )
A.a点由水电离出的c(H+)=1.0×10-14 mol・L-1
B.b点:c(NH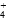 )+c(NH3・H2O)=c(Cl-)
)+c(NH3・H2O)=c(Cl-)
C.c点:c(Cl-)=c(NH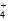 )
)
D.d点后,溶液温度略下降的主要原因是NH3・H2O电离吸热
参考答案:C
本题解析:本题考查电解质溶液中的离子浓度关系,意在考查学生对化学图像的分析能力及对酸碱中和滴定和混合溶液中离子浓度关系的掌握情况。a点即是1.000 mol・L-1的氨水,NH3・H2O是弱电解质,未完全电离,c(OH-)<1 mol・L-1,水电离出的c(H+)>1.0×
10-14 mol・L-1,A项错误;b点处,加入盐酸的体积未知,不能进行比较,B项错误;c点溶液显中性,即c(OH-)=c(H+),结合电荷守恒关系:c(OH-)+c(Cl-)=c(H+)+c(NH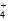 ),有
),有
c(Cl-)=c(NH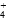 ),C项正确;d点后,溶液温度下降是由于加入的冷溶液与原溶液发生热传递,D项错误。
),C项正确;d点后,溶液温度下降是由于加入的冷溶液与原溶液发生热传递,D项错误。
本题难度:一般
4、选择题 下列叙述正确的是(?)
A.将等体积的PH=3的醋酸溶液和PH=4的醋酸溶液完全中和时消耗氢氧化钠的物质的量,前者是后者的10倍
B.向0.1mol/L的氨水里,加入0.1mol/L的HCl溶液至反应PH=7时,消耗HCl溶液的体积小于氨水的体积
C.pH=3.6的0.1mol/L HX与0.1mol/L NaX的混合溶液中,2c(Na+)=c(X-)
D.0.1mol・L-1的硫化钠溶液中:c(OH-)= c(H+)+ c(HS-)+ c(H2S)
参考答案:B
本题解析:弱电解质的浓度越大,其电离程度越小,所以PH=3的醋酸溶液的物质的量浓度大于PH=4的醋酸溶液的物质的量浓度的10倍,所以A选项错误(或者说:前者c(H+)是后者的10倍,但醋酸的电离程度不同,所以前者的物质的量浓度不是后者的10倍);B选项中,若恰好完全中和生成NH4Cl溶液,显酸性,要使PH=7,氨水应略过量,所以B选项正确;C选项考查的是物料守恒,应是2c(Na+)=c(X-)+ c(HX),所以C错误;D选项考查的是质子守恒,正确的应是:c(OH-)= c(H+)+c(HS-)+2c(H2S)所以D选项错误;
本题难度:一般
5、选择题 常温下,柠檬水溶液的PH是3,其中水电离的c(H+)为
A.1×10-3mol/L
B.1×10-7mol/L
C.1×10-11mol/L
D.1×10-14mol/L
参考答案:C
本题解析:溶液的PH是3,则溶液中OH-的浓度是1×10-11mol/L。酸是抑制水的电离的,所以溶液中水电离的c(H+)就是溶液中OH-的浓度,答案选C。
本题难度:一般