微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 .已知酸碱发生中和反应生成1molH2O时释放的热量称为中和热,强酸与强碱反应的中和热为57.3 kJ・mol
参考答案:
本题解析:
本题难度:一般
2、选择题 已知25℃时,Ksp[Cu(OH)2]=2×10-20。要使0.2 mol・L-1 CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为(?)
A.4
B.6
C.8
D.10
参考答案:B
本题解析:Cu2+的浓度为0.2mol・L-1×10-3=2×10-4mol・L-1,又因为Ksp=(Cu2+).(OH-)2,则OH-的浓度为10-8mol・L-1,25℃时,(OH-).(H+)=10_14,则H+的浓度为10-6mol・L-1,即PH=6sp及PH的计算
点评:此题考核了沉淀Ksp的计算及引伸出来的关于溶液PH的计算,难度不大。
本题难度:简单
3、选择题 取浓度相同的Na0H和HCl溶液,以3∶2 体积比相混合,所得溶液的pH 等于12,则原溶液的浓度为?(?)
A.0.01mol/L
B.0.017mol/L
C.0.05mol/L
D.0.50mol/L
参考答案:C
本题解析:考查pH的有关计算。根据题意氢氧化钠过量,反应后溶液中OH-的浓度为0.01mol/L。所以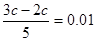 ,解得c=0.05mol/L。答案是C。
,解得c=0.05mol/L。答案是C。
本题难度:简单
4、选择题 已知反应:①101kPa时,C(s) + 1/2O2(g)=CO(g);△H1=-110.5kJ/mol
②稀溶液中,H+(aq) + OH-(aq)=H2O(1);△H2=-57.3kJ/mol
下列结论正确的是(?)
A.若碳的燃烧热用△H3来表示,则△H3<△H1
B.若碳的燃烧热用△H3来表示,则△H3>△H1
C.稀硫酸与稀NaOH溶液反应的中和热△H=-57.3kJ/mol
D.浓硫酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
参考答案:AC
本题解析:燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,所以碳完全燃烧放热多,但放热越多,△H越小,选项A正确,B不正确;浓硫酸溶于水会放出大量的热,所以选项D不正确,C正确,答案选AC。
本题难度:一般
5、填空题 (14分)已知25℃、101kPa下,氢气、甲烷和葡萄糖的燃烧热依次为285.8 kJ/mol、890.3kJ/mol、2800 kJ/mol。
(1)0.1mol甲烷和0.2mol氢气组成的混合气体在25℃、101kPa下完全燃烧释放的热量为 ;
(2)写出表示葡萄糖燃烧热的热化学方程式: ;
(3)有人利用甲烷和氧气的反应设计成如图所示燃料电池,若使用酸性电解质溶液,则两极的电极反应式为:
a极: ,b极: ;
若使用碱性电解质溶液,则b极的电极反应式为:b极: ;
放电时电极a作 极,外电路中电流从 流向 ,电解质溶液中阳离子移向 极;
参考答案:(14分)(1) (2分/个) 146.19kJ/mol
(2) C6H12O6(s) + 6O2(g) 6CO2(g) + 6H2O(l) △H= -2800kJ/mol
6CO2(g) + 6H2O(l) △H= -2800kJ/mol
(3)a极:2O2+ 8H++ 8e-=== 4H2O ;b极:CH4+ 2H2O -8e-===CO2+ 8H+
b极:CH4+ 10OH--8e-===CO32-+7H2O
(1分/个) 正 a b a
本题解析:略
本题难度:简单