微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质含有离子键的是?
A.CO2
B.H2
C.NH3
D.NaOH
参考答案:D
本题解析:一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键,据此可知选项A、C中含有极性键,B中含有非极性键,D中含有离子键和极性键,答案选D。
点评:该题是高考中的常见考点,属于基础性试题的考查,主要是检验学生对化学键以及化学键判断的熟悉了解程度,侧重对学生基础知识的巩固和训练。该题的关键是明确离子键、共价键的含义和判断依据,然后结合题意灵活运用即可。
本题难度:简单
2、选择题
A.同种原子形成的分子,两原子间的化学键一定是共价键
B.非金属元素的原子之间形成的化学键一般是共价键
C.不管是含氧酸还是无氧酸,分子内原子间的化学键都是共价键
D.凡是不含金属元素的化合物一定是共价化合物
参考答案:C
本题解析:含氧酸与无氧酸分子内不存在阴阳离子,因此分子内所有的化学键都是共价健。
本题难度:简单
3、简答题 下列关于化学键的说法正确的是( )
A.化学键是分子与分子之间的作用力
B.形成物质中的化学键时,要吸收能量
C.化学键的断裂和形成是化学反应中能量变化的主要原因
D.形成或断裂同一种化学键,放出或吸收的能量是不相等的,这是化学反应中能量变化的主要原因
参考答案:A、化学键是相邻原子之间的强烈的作用力,分子与分子之间的作用力为范德华力,故A错误;
B、形成化学键要放出能量,断裂化学键要吸收能量,故B错误;
C、化学反应的实质是旧键的断裂和新键的形成,形成化学键要放出能量,断裂化学键要吸收能量,则化学反应一定伴随着能量变化,故C正确;
D、一种化学键的键能是一定的,形成或断裂同一种化学键,放出或吸收的能量相同,故D错误.
故选C.
本题解析:
本题难度:一般
4、选择题 有机物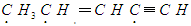 中标有“・”的碳原子的杂化方式依次为?
中标有“・”的碳原子的杂化方式依次为?
A.sp、sp2、sp3
B.sp3、sp2、sp
C.sp2、sp、sp3
D.sp3、sp、sp2
参考答案:B
本题解析:有机物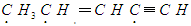 中标有“・”的碳原子的杂化方式依次为sp3、sp2、sp,故选项是B。
中标有“・”的碳原子的杂化方式依次为sp3、sp2、sp,故选项是B。
本题难度:一般
5、填空题 已知拆开1 mol H―H键、1 mol I―I、1 mol H―I键分别需要吸收的能量为436kJ、151k J、299k J。则由氢气和单质碘反应生成1 mol HI需要 (填“放出”或“吸收”) k J的热量。
参考答案:放出 ; 5.5
本题解析:氢气和单质碘反应的方程式:H2+I2="2HI," 拆开1 mol H―H键、1 mol I―I、1 mol H―I键分别需要吸收的能量为436kJ、151k J、299k J,可知由氢气和单质碘反应生成2mol HI需要放出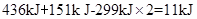 ,而生成1mol HI需要放出
,而生成1mol HI需要放出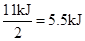
考点:化学反应热量计算
点评:化学反应与能量的变化是高考的一个高考,难度不大,计算量也不大,考生要抓住放热反应反应物总能量大于生成物总能量的特征,即可解答。
本题难度:一般