��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1���ƶ��� ��֪��A��FΪ�������ʣ�D��EΪ��̬���ʣ������Ϊ���������C����ɫ��Ӧ�ʻ�ɫ��BΪ��ɫ��ĩ��JΪ��ɫ�����������ʼ��ת����ϵ����ͼ��ʾ(��������������ȥ)��
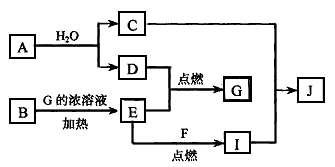
(1)A��ԭ�ӽṹʾ��ͼΪ ________________�� B�Ļ�ѧʽΪ_______________��
(2)д����ӦC+I��J�����ӷ���ʽ��________________________��
(3)д��E+F��I�Ļ�ѧ��Ӧ����ʽΪ______________��D��E�е�ȼʱ������Ϊ_________________��
�ο��𰸣���1��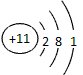 �� MnO2
�� MnO2
��2��Cu2+ + 2OH-��Cu(OH)2��
��3��Cu + Cl2 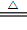 CuCl2?�� ������ɫ����
CuCl2?�� ������ɫ����
���������
�����Ѷȣ�һ��
2������� A+��B+��C-��D��E�������ӣ����ӻ����ӣ������Ƿֱ�10�����ӣ���֪����������ת����ϵ����A++C-��D+E����B++C-��2D��
�ݴˣ��ش��������⣺
��1������10�����ӵ���������______������10�����ӵ���������______��
��2��A+��B+�ĵ���ʽA+______��B+______��
��3��C-��D��E�������ӽ�����ӣ�H+����������ǿ������˳���ǣ������ӵĻ�ѧʽ��ʾ��______����һ˳������������ӷ���ʽ����˵����
��______��
��______��
�ο��𰸣���1�����˵����=������=�����������Ϊԭ�ӣ����˵����=�������������������Ϊ�����ӣ����˵����=�������������������Ϊ�����ӣ�����10�����ӵķ����У�NH3��H2O������10�����ӵ���������H3O+��NH4+������10�����ӵ���������OH-���ʴ�Ϊ��H3O+��NH4+��OH-��
��2������A++C-��D+E��B++C-��2D��֪A+��B+�ֱ���NH4+��H3O+�����ǵĵ���ʽΪ��
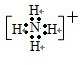
��
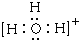
���ʴ�Ϊ��
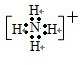
��
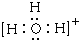
��
��3����ӦNH4++OH-=NH3?H2O��֤��������ӣ�H+��������OH-��NH3����ӦNH3+H3O+=NH4++H2O֤��������ӣ�H+��������NH3��H2O������ȷ��OH-��NH3��H2O��������ӵ�����Ϊ��
OH-��NH3��H2O���ʴ�Ϊ��OH-��NH3��H2O��NH4++OH-=NH3?H2O��NH3+H3O+=NH4++H2O��
���������
�����Ѷȣ�һ��
3������� ��7�֣���ͼ��A��B��Ϊ���壬����BΪ���嵥�ʡ���ͼ�����ڹ�ҵ����Һ��F��F��������������Ϊһ�����ҹ�ҵ��չˮƽ�ı�־���ش��������⣺
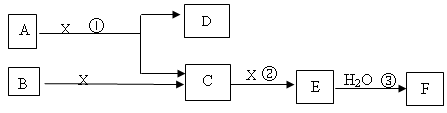
��1��A������Ԫ�ع��ɣ�ԭ�Ӹ�����Ϊ1:2��DΪ����ɫ���壬A�Ļ�ѧʽ?
��2��д��D�������ʷ�Ӧ�Ļ�ѧ����ʽ?
��3����Ӧ���ǿ��淴Ӧ����2 L���ܱ�������Ͷ��4 molC��3 molX,10���Ӻ�Ӧ�ﵽƽ��,ƽ��ʱ������干6 mol,������˵����ȷ����?
A����10������,X��ƽ��������0. 1mol/( L��min)
B. �ڹ�ҵ�����п���ͨ������X���������C��ת����
C����C��X���������ʱ�Ϊ2:1ʱ,��־�ŷ�Ӧ�ﵽƽ��
D��ƽ��ʱC��ת������50%
��4��д����״����2.24L����C��0.15mol����������Һ��Ӧ�����ӷ���ʽ?
�ο��𰸣���1��FeS2��1�֣�?��2��2Al + Fe2O3 2Fe +Al2O3
2Fe +Al2O3
��3��BD?��4��2SO2+3OH- =SO32-+HSO3-+H2O
�����������1��F��������������Ϊһ�����ҹ�ҵ��չˮƽ�ı�־������F�����ᡣ��E��SO3��C��SO2��X������������B�ǵ���S������ΪDΪ����ɫ���壬���D��Fe2O3������A�к�����Ԫ�ء�����A��ԭ�Ӹ�����Ϊ1:2������A��FeS2��
��2�����ܺ��������������ȷ�Ӧ������ʽΪ2Al + Fe2O3 2Fe +Al2O3��
2Fe +Al2O3��
��3��������淴Ӧ���йؼ��㣬һ���������ʽ����
2SO2?��? O2 2SO3
2SO3
��ʼ����mol��? 4? 3? 0
ת������mol��? 2x? x? 2x
ƽ������mol��? 4��2x? 3��x? 2x
����4��2x��3��x��2x��6mol
���x��1mol
����10������������ƽ�������� ��0.05mol/( L��min)��A����ȷ��SO2��ת������
��0.05mol/( L��min)��A����ȷ��SO2��ת������ ��D��ȷ������������Ũ�ȣ�ƽ��������Ӧ�����ƶ����������SO2��ת���ʣ�B��ȷ�����ڷ�Ӧ����֮������Ӧ�Ļ�ѧ������֮�ȣ�����C��X���������ʱ�����2:1�ģ�C����ȷ����ѡBD��
��D��ȷ������������Ũ�ȣ�ƽ��������Ӧ�����ƶ����������SO2��ת���ʣ�B��ȷ�����ڷ�Ӧ����֮������Ӧ�Ļ�ѧ������֮�ȣ�����C��X���������ʱ�����2:1�ģ�C����ȷ����ѡBD��
(4)��״����2.24LSO2��0.1mol������������0.15mol�������������м����������ƣ��������������ƣ��Ҷ�����1�U1�ģ���˷���ʽΪ2SO2+3OH- =SO32-+HSO3-+H2O��
�����Ѷȣ�һ��
4���ƶ��� A��B��C����ѧ��ѧ�г������������ʣ�����֮����ת����ϵ����(���ַ�Ӧ��?����������ȥ)��
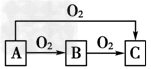
A��B��C����ѧ��ѧ�г������������ʣ�����֮����ת����ϵ����(���ַ�Ӧ��?����������ȥ)��
(1)��?A?��һ�ֽ�����C�ǵ���ɫ���壬��B�Ļ�ѧʽΪ________��A��C��Ӧ�Ļ�ѧ����ʽΪ______________________��
(2)��A��һ�ַǽ������䳣������Ϊ��ɫ���壬C������Ҫ���������壬��C�ķ���ʽΪ________��B��C��Ӧ�Ļ�ѧ����ʽΪ__________________�� A��C�Ƿ���Է�Ӧ________�����ܣ�д����Ӧ�Ļ�ѧ����ʽ�������ܣ��˿ղ���______________________��
�ο��𰸣�(1)Na2O��2Na��O2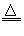 Na2O2
Na2O2
(2)CO2��2CO��O2 2CO2���ܣ�C��CO2
2CO2���ܣ�C��CO2 2CO
2CO
���������
�����Ѷȣ�һ��
5������� ��12�֣���ͼ��A~ O ��ת����ϵ����֪A��һ�ֽ������ʣ�B��C��D��E��F��H��I��J��K���³�ѹ�¾�Ϊ���壬��B��C��D��E�ǵ��ʣ�I��һ�ֺ���ɫ���壬G��һ�ֵ���ɫ���壬M�ǻ����������壬J��K����������������̡���ش��������⣺

��1��д��G��ˮ��Ӧ�Ļ�ѧ����ʽ?��д������E��N��Һ��Ӧ�����ӷ���ʽ?��
��2��������G�к��еĻ�ѧ��Ϊ?��
��3��д��F�ĵ���ʽ?��������O�ĵ���ʽ?��
��4��E��F��Ӧ��������Ļ�ѧ����ʽΪ?��
�ο��𰸣���1��2Na2O2+2H2O=4NaOH+O2����Cl2+2OH-=Cl-+ClO-+H2O��
��2�����Ӽ������ۼ���?��3��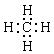 ��
�� ����4��CH4+Cl2��CH3Cl+HCl(����)
����4��CH4+Cl2��CH3Cl+HCl(����)
�����������
�����Ѷȣ���