微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用水稀释0.lmol・L-1的氨水时,溶液中随着水量的增加而减小的是
A.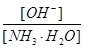
B.
C.[H+]和和[OH-]的乘积
D.OH-的物质的量
参考答案:B
本题解析:氨水中存在如下平衡: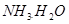 ?
?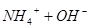 加水稀释,平衡将向右移动,所以A错,根据电离常数只受温度影响,只要温度不变电离常数不变,所以
加水稀释,平衡将向右移动,所以A错,根据电离常数只受温度影响,只要温度不变电离常数不变,所以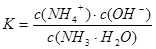 ,则
,则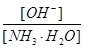
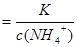
加水稀释,铵根离子浓度减小,比值增大;B正确;C错,[H+]和和[OH-]的乘积为水的离子积常数,只受温度影响;D错,加水稀释,平衡向右移动,氢氧根离子的物质的量增大;
本题难度:一般
2、选择题 常温下,浓度均为0.1mol/L的三种溶液:①CH3COOH溶液②NaOH溶液③CH3COONa溶液,下列说法中不正确的是(忽略混合前后溶液体积变化)…………………(?)
A.溶液的pH值:②>③>①
B.水电离出的c(OH-):③>①>②
C.①和②等体积混合后的溶液:c(CH3COOH)+ c(CH3COO-)=0.1mol/L
D.②和③等体积混合后的溶液:c(Na+)+ c(H+)=c(OH-)+c(CH3COO-)
参考答案:C
本题解析:①、②、③分别是弱酸、强碱、盐? A对
水电离出的c(OH-)受①电离出H+、②电离出的OH-、③水解出的OH-的影响 B对
①和②反应生成水,溶液总质量增加,n不变,c一定变小,C 错
溶液的阴阳离子平衡,D对
本题难度:一般
3、选择题 H2A为二元弱酸,则下列说法正确的是
A.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
B.在等物质的量浓度的Na2A、NaHA两溶液中,前者pH大于后者
C.在NaHA溶液中一定有:c(Na+)>c(HA-)>c(OH-)>c(H+)
D.在Na2A溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-)
参考答案:B
本题解析:A、因为阴离子发生水解,水解后离子数目增大,故阴离子总数不等;
B、酸性H2A>HA-;越弱越水解,故前者水解程度大,碱性强。
C、因电离水解程度未知,不能判断;
D、该等式为电荷守恒,但硫离子有2个负电荷。故为 c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
本题难度:一般
4、选择题 25℃时,向10mLpH=12的某碱溶液中加入10mLpH=2的盐酸,充分反应后滴入石蕊试液,溶液显蓝色,则此碱一定是( )
A.弱碱
B.一元强碱
C.多元强碱
D.任何强碱
参考答案:A
本题解析:石蕊溶液显蓝色,说明溶液显碱性,如果此碱是强碱则10mLpH=12的该碱与10mLpH=2的盐酸恰好完全反应,溶液呈中性,所以此碱为弱碱。选A。
点评:如果酸碱的pH相加等于14,且等体积混合,混合后的溶液呈什么性质,由弱的溶液决定。
本题难度:一般
5、选择题 300 mL某浓度的NaOH溶液中含有60 g溶质。现欲配制1 mol /L NaOH溶液,应取原溶液与蒸馏水的体积比约为(?)
A.1∶4
B.1∶5
C.2∶1
D.2∶3
参考答案:A
本题解析:依据题意可知即需要NaOH的质量m=n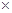 M=c
M=c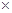 V
V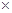 M=1
M=1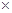 1
1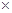 40g=40g,所以需要200mL(300/60
40g=40g,所以需要200mL(300/60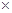 40 mL="200" mL),即还需要蒸馏水800 mL,即200:800=1∶4
40 mL="200" mL),即还需要蒸馏水800 mL,即200:800=1∶4
点评:该题是基础性试题的考查,属于高考中的常见考点之一,难度不大。
本题难度:简单