微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列溶液中微粒的物质的量浓度关系一定正确的是 ( )
A.0.1mol/LNH4Cl溶液与0.05mol/LNaOH溶液等体积混合后所得的碱性溶液中:
c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+)
B.等物质的量的NaClO、NaHCO3混合溶液中:
c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)
C.pH=2的HA溶液与pH=12的MOH溶液等体积混合:
c(M+)=c(A-)>c(OH-)=c(H+)
D.某二元弱酸的酸式盐NaHA溶液:c(Na+)+ c(H+)=c(OH-)+c(HA-)+c(A2-)
参考答案:B
本题解析:A.混合后,存在水解平衡NH4++ OH- NH3・ H2O ,溶液中c(Cl-)=0.05mol/L,c(Na+)=0.025mol/L,由于NH4+只有少数发生电离,所以c(NH4+)略小于0.05mol/L,c(OH-)略小于0.025mol/L,所得溶液显碱性,则c(OH-)>c(H+),所以c(Cl-) >c(NH4+)>c(Na+) >c(OH-)>c(H+),A不正确;
NH3・ H2O ,溶液中c(Cl-)=0.05mol/L,c(Na+)=0.025mol/L,由于NH4+只有少数发生电离,所以c(NH4+)略小于0.05mol/L,c(OH-)略小于0.025mol/L,所得溶液显碱性,则c(OH-)>c(H+),所以c(Cl-) >c(NH4+)>c(Na+) >c(OH-)>c(H+),A不正确;
B.根据物料守恒可知等物质的量的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-),B正确;
C.只有当HA为强酸,MOH为强碱时,c(M+)=c(A-)>c(OH-)=c(H+)才能成立,C不正确;
D.根据电荷守恒,某二元弱酸的酸式盐NaHA溶液:c(Na+)+ c(H+)=c(OH-)+c(HA-)+2c(A2-),D不正确。故选B。
点评:本题考查弱电解质的电离及盐类的水解的知识,有一定的难度,对于此类题目,考生应熟悉掌握物料守恒、质子守恒和电荷守恒。
本题难度:简单
2、选择题 某温度下,体积和pH都相同的盐酸和AlCl3溶液加水稀释时的pH变化曲线如图,下列有关说法正确的是( )
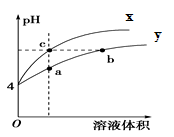
A.Al(OH)3的电离方程式为:Al(OH)3=Al3++3OH-
B.a点溶液中有: c(H+)+c(Al3+)=c(OH-) +3c(Cl-)
C.曲线X表示盐酸稀释过程的pH变化
D.b、c两溶液c(OH-)及c(Cl-)均相等
参考答案:C
本题解析:A. Al(OH)3是弱电解质。在溶液中存在电离平衡。所以其的电离方程式为:Al(OH)3 Al3++3OH-。错误。B.在任何溶液中都存在电荷守恒。所以在a点溶液中有: c(H+)+3c(Al3+)=c(OH-) +c(Cl-)。错误。C. HCl是强酸,电离产生H+使溶液显酸性,在溶液中不存在电解质的电离平衡。而AlCl3是强酸弱碱盐,水解使溶液显酸性。在水溶液中存在水解平衡。当加水稀释时,强酸的溶液的pH变化较大,盐溶液的pH变化较小。所以曲线X表示盐酸稀释过程的pH变化。正确。D.b、c两点pH相同,则两溶液c(OH-)相同。而c(Cl-)HCl的小于AlCl3的。错误。
Al3++3OH-。错误。B.在任何溶液中都存在电荷守恒。所以在a点溶液中有: c(H+)+3c(Al3+)=c(OH-) +c(Cl-)。错误。C. HCl是强酸,电离产生H+使溶液显酸性,在溶液中不存在电解质的电离平衡。而AlCl3是强酸弱碱盐,水解使溶液显酸性。在水溶液中存在水解平衡。当加水稀释时,强酸的溶液的pH变化较大,盐溶液的pH变化较小。所以曲线X表示盐酸稀释过程的pH变化。正确。D.b、c两点pH相同,则两溶液c(OH-)相同。而c(Cl-)HCl的小于AlCl3的。错误。
本题难度:一般
3、选择题 pH=2的两种一元酸x和y,体积均为100mL,稀释过程中,pH与溶液体积的关系如右图所示。分别滴加NaOH溶液(c="0.1" mol・L-1)至pH=7。消耗NaOH溶液的体积为Vx、Vy,则(?)
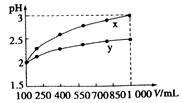
A.x为弱酸,Vx < Vy
B.x为强酸,Vx > Vy
C.y为弱酸,Vx < Vy
D.y为强酸,Vx > Vy
参考答案:C
本题解析:由图可知x为强酸,y为弱酸;在PH相同且体积相同的情况下,弱酸y的物质的量比x多,消耗NaOH的物质的量更多,所以正确选项为C;
本题难度:一般
4、选择题 在室温下等体积的酸和碱的溶液混合后,pH一定小于7的是
A.pH=3的硝酸跟pH=11的氢氧化钾溶液
B.pH=3的盐酸跟pH=11的氨水
C.0.1mol/LCH3COOH与0.1mol/LNaOH溶液
D.pH=3的醋酸跟pH=11的氢氧化钡溶液
参考答案:D
本题解析:在室温下等体积的酸和碱的溶液混合, A.pH=3的硝酸跟pH=11的氢氧化钾溶液混合后,pH=7;B.pH=3的盐酸跟pH=11的氨水pH大于7;C.0.1mol/LCH3COOH与0.1mol/LNaOH溶液考点,pH=3的盐酸跟pH=11的氨水pH大于7;D.pH=3的醋酸跟pH=11的氢氧化钡溶液,pH一定小于7。
点评:pH=3的弱酸与pH=3的强酸,所对应的一元酸的浓度前者大于后者。
本题难度:一般
5、选择题 将0.20mol・L-1的NH3・H2O溶液和0.10mol・L-1的HCl溶液等体积混合,充分反应后,下列有关该溶液中各粒子浓度的关系不正确的是?(?)
A.c(NH4+)>c(Cl-)>c(H+)>c(OH-)
B.c(Na+)+c(H+)=c(Cl-)+c(OH-)
C.c(NH4+)+c(NH3・H2O)=0.10mol・L-1
D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
参考答案:A
本题解析:两溶液中和后形成了等浓度的NH3・H2O与NH4Cl溶液,由于前者的电离程度大于后者NH4+的水解程度,最终溶液呈碱性:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
溶液中电荷守恒:c(Na+)+c(H+)=c(Cl-)+c(OH-)
N原子的物料守恒:c(NH4+)+c(NH3・H2O)=0.10mol・L-1
故A错误
本题难度:一般