微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
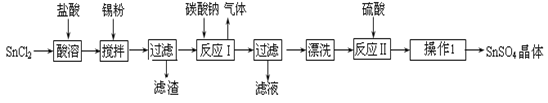
1、简答题 (14分)硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:
查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡, Sn相对原子质量为119
回答下列问题:
(1)锡原子的核电荷数为50,锡元素在周期表中的位置是 。
(2)操作Ⅰ是 。
(3)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因 。
(4)加入Sn粉的作用有两个:①调节溶液pH ② 。
(5)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是 。
(6)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是 。
(7)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl===SnCl2 + H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:
6FeCl2 + K2Cr2O7 + 14HCl ===6FeCl3 + 2KCl + 2CrCl3 +7H2O
取1.226 g锡粉,经上述各步反应后,共用去0.100 mol/L K2Cr2O7溶液32.0ml。锡粉中锡的质量分数是 。
参考答案:(1)五周期ⅣA族
(2)加热浓缩、冷却结晶、过滤、洗涤
(3)Sn Cl2 + H2O  Sn(OH)Cl + HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解
Sn(OH)Cl + HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解
(4)防止Sn2+被氧化 (5)Sn2+ + CO32- ===SnO↓ + CO2↑
(6)Sn2+ + H2O2 +2H+ ="==" Sn4+ + 2H2O
(7)93.2%
本题解析:(1)Sn核电荷数为50,则:50-2-8-8-18=14,故Sn处于第五周期,ⅣA族; (2)从溶液中得到晶体的实验操作:蒸发浓缩、冷却结晶、过滤洗涤;(3)由信息可知,SnCl2可水解SnCl2+H2O?Sn(OH)Cl+HCl,盐酸浓度增大,平衡向左移动,从而抑制Sn2+水解;(4)因为Sn2+易被氧化,所以加入Sn粉除调节溶液pH外,还可防止Sn2+被氧化;(5)加入Na2CO3得到沉淀SnO,Sn元素化合价无变化,可知反应Ⅰ属于非氧化还原反应,因此所得气体为CO2,离子方程式为:Sn2++CO32-
本题难度:困难
2、简答题 科研人员将软锰矿(MnO2含量≥65%,SiO2含量约20%,A12O3含量约4%,其余为水分)和闪锌矿(ZnS含量≥80%,FeS、CuS、SiO2含量约7%,其余为水分)同槽酸浸开发出综合利用这两种资源的新工艺,如图所示为工艺流程的一部分.

已知:ZnCO3不溶于水,但溶于酸.部分阳离子以氢氧化物形式深沉时溶液的pH见下表:
| 物质 | Fe(OH)3 | A1(OH)3 | Zn(OH)2 | Fe(OH)2 | Mn(OH)2
开始沉淀pH
2.7
3.3
5.4
7.6
8.3
完全沉淀pH
4.4
5.2
8.0
9.6
9.8
|
请回答:
(1)反应器I过滤所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、A12(CO4)3等.试完成反应器I中生成CuSO4的化学方程式(不须配平):CuS+______+H2SO4→______+______+CuSO4+H2O
(2)反应器II中发生反应的离子方程式为______.
(3)从沉淀溶解平衡的角度分析反应器III中生成A1(OH)3沉淀的原因______.检验ZnCO3是否过量的操作方法是______.
(4)反应器中IV中,试剂A可以是下列物质中______(填代号).a.氨水? b.氢氧化钠? c.MnO2 d.稀硫酸
(5)欲从反应器IV的滤液中完全沉淀出Zn(OH)2,而不析出Mn(OH)2,则滤液的pH范围为______,要将分离出沉淀后的滤液进行浓缩,需将温度控制在90℃~100℃,可采用的加热方法是______.
参考答案:(1)反应I为酸浸过程,Mn、Al、Zn、Fe、Cu元素在该过程均转化为金属阳离子进入溶液,而难溶于酸的S、SiO2则通过过滤而分离出来,
故答案为:MnO2;S↓;MnSO4;
(2)加入Zn后,Zn把Cu置换出来,而且Zn还原Fe3+,发生氧化还原反应.故答案为:Zn+2Fe3+=2Fe2++Zn2+、Zn+Cu2+=Cu+Zn2+;
(3)加入ZnCO3后,ZnCO3与溶液中的H+反应,导致溶液中c(H+)减小,c(OH-)增大,c(Al3+)?c(OH-)>Ksp[Al(OH)3],从而生成Al(OH)3沉淀;取少许沉淀于试管中,滴加适量的稀硫酸,若有气泡产生,则说明ZnCO3过量;若无气泡产生,则说明ZnCO3不过量.故答案为:ZnCO3与溶液中的H+反应,导致溶液中c(H+)减小,c(OH-)增大,从而生成Al(OH)3沉淀;取少许沉淀于试管中,滴加适量的稀硫酸,若有气泡产生,则说明ZnCO3过量;若无气泡产生,则说明ZnCO3不过量.
(4)在所得虑液中加入MnO2将Fe2+氧化为Fe3+,再加入ZnCO3调节溶液pH 在5.2-5.4之间使Fe3+、Al3+完全转化为Fe(OH)3、Al(OH)3而分离(超过5.4Zn(OH)2会析出).故选c;
(5)从反应器IV的滤液中完全沉淀出Zn(OH)2,而不析出Mn(OH)2,则滤液的pH范围为8.0≤pH<8.3(超过8.3Mn(OH)2会析出);将温度控制在90℃~100℃,最好采用水浴加热.故答案为:8.0≤pH<8.3;水浴加热.
本题解析:
本题难度:一般
3、填空题 研究碳及其化合物的综合利用对促进低碳社会的构建具有重要的意义。请运用相关知识研究碳及其化合物的性质。
(1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:______C+________K2Cr2O7+________――________CO2↑+________K2SO4+________Cr2(SO4)3+________H2O。
①完成并配平上述化学方程式。
②在上述化学方程式上标出该反应电子转移的方向与数目。
(2)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是_________________________________________________________。
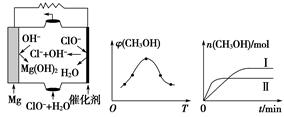
②由MgO可制成“镁-次氯酸盐”燃料电池,其装置示意图如图(a)所示,该电池反应的离子方程式为________________________________________。
(a) ? (b) (c)
(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH。
CH3OH(g)+H2O(g) ΔH。
①该反应的平衡常数表达式为K=________。
②取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图(b)所示,则上述CO2转化为甲醇反应的ΔH________(填“>”“<”或“=”)0。
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图(c)所示,曲线Ⅰ、Ⅱ对应的平衡常数大小关系为KⅠ________KⅡ(填“>”“<”或“=”)。
参考答案:(1)①3 2 8 H2SO4 3 2 2 8
② +8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O
+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O
(2)①2MgSO4+CO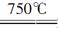 2MgO+SO2+CO2+SO3
2MgO+SO2+CO2+SO3
②Mg+ClO-+H2O=Cl-+Mg(OH)2
(3)①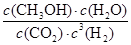 ②< ③>
②< ③>
本题解析:(1)①反应中C→CO2,化合价升高4,K2Cr2O7→Cr2(SO4)3,化合价降低6,根据得失电子守恒、质量守恒定律即可配平反应的化学方程式。
②得失电子的最小公倍数为12,用单线桥或双线桥表示均可,单线桥表示如下:
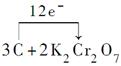 +8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O。
+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O。
(2)①CO作还原剂,反应中CO→CO2,化合价升高2,MgSO4→SO2,化合价降低2,据此即可配平化学方程式。
②从图(a)可知,放电时Mg→Mg(OH)2,化合价升高2;ClO-+H2O→Cl-+OH-,化合价降低2,由此可配平反应的化学方程式。
(3)①平衡常数为生成物浓度幂之积与反应物浓度幂之积的比值。
②从图(b)的最高点(平衡点)之后看,随着反应的进行,升高温度,平衡逆向移动,故正反应为放热反应,ΔH<0。
③从图(c)看,反应Ⅰ中生成甲醇的物质的量大于反应Ⅱ中生成甲醇的物质的量,说明Ⅰ条件下有利于平衡正向移动,平衡常数大。
本题难度:困难
4、填空题 KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为
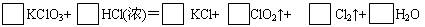
(1)请配平上述化学方程式(计量数填入框内)
(2)浓盐酸在反应中显示出来的性质是___________(填编号)
①只有还原性?②还原性和酸性?③只有氧化性?④氧化性和酸性
(3)产生0.1mol Cl2,则转移的电子的物质的量为________mol。
参考答案:(1)2,4=2,2,1,2; (2)②; (3)0.2
本题解析:略
本题难度:简单
5、选择题 管道工人曾经用浓氨水检查氯气管道是否漏气。已知能发生如下反应:(在有水蒸气存在的条件下) 2NH3+3Cl2=6HCl+N2?下列说法中错误的是(?)
A.用该方法检验管道泄漏处会产生白烟
B.管道泄漏处会闻到刺激性气味
C.该反应生成1mol氮气时,转移3mol电子
D.可以用浸有稀碱液的布包裹在管道泄漏处,暂时防止氯气的危害
参考答案:C
本题解析:A、若管道漏气,发生反应3Cl2+2NH3=N2+6HCl,反应生成的HCl与NH3反应生成NH4Cl,有白烟生成,正确;B、氯气具有刺激性气味,所以管道泄漏处会闻到刺激性气味,正确;C、该反应中氮元素的化合价由反应前的-3价变为反应后的0价,所以生成1mol氮气转移6mol电子,错误;D、氯气能与碱溶液反应,所以可以用浸有稀碱液的布包裹在管道泄漏处,暂时防止氯气的危害,正确。
本题难度:一般