|
�߿���ѧ���⡶ԭ���ԭ������Ƶ����̣�2017�����°棩(��)
2017-08-06 11:53:27
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
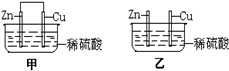
1��ѡ���� ����пƬ�ʹ�ͭƬ��ͼ��ʾ������ͬŨ�ȵ�ϡ�����У������й�������ȷ���ǣ�������
A����װ���е���ת��Ϊ��ѧ��
B����װ���е���ת��Ϊ��ѧ��
C����װ����ͭƬ���������ݲ���
D����װ����ͭƬ��������������
| 
�ο��𰸣�����ԭ��صĹ��������жϣ�����ԭ��أ��Ҳ���ԭ��أ�
A������ԭ��أ����Լ��ǰѻ�ѧ��ת��Ϊ���ܵ�װ�ã���A����
B���Ҳ���ԭ��أ����ǰѻ�ѧ��ת��Ϊ���ܵ�װ�ã���B����
C������ͭƬ���������ü��������ӵõ���������������C��ȷ��
D������пƬ���Ժ����ᷴӦ��������������ͭ�������Ӧ��ͭƬ�������������ɣ���D����
��ѡC��
���������
�����Ѷȣ�һ��
2��ѡ���� һ����ȼ�ϵ�أ�һ��ͨ���������һ��ͨ�붡�����壻������Dz��������ƣ�Y2O3��������ﯣ�ZrO2�����壬������״̬���ܴ���O2-�����жԸ�ȼ��˵����ȷ���ǣ�������
A�������ڵ�����У�O2-�ɸ�����������
B����ص��ܷ�Ӧ�ǣ�2C4H10+13O2�T8CO2+10H2O
C��ͨ�������һ���Ǹ������缫��ӦΪ��O2+4e-=2O2-
D��ͨ�붡���һ���Ǹ������缫��ӦΪ��C4H10-26e-+13O2-=4CO2+5H2O
�ο��𰸣�BD
���������
�����Ѷȣ�һ��
3������� �ҹ��Ǹ��������,��������Ϊ�����һ,��¯��������Ϊ�ձ������������
I.��֪��Ӧ  Fe2O3(s)+ CO(g) Fe2O3(s)+ CO(g) 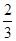 Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1���÷�Ӧ�� Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1���÷�Ӧ��
1000���ƽ�ⳣ������4����һ���ݻ�Ϊ10L���ܱ�������,1000��ʱ����Fe��Fe2O3��CO��CO2��1. 0mol,��Ӧ����l0min��ﵽƽ�⡣
��1��CO��ƽ��ת����=____________
��2�������CO��ƽ��ת����,�ٽ�Fe2O3��ת��,�ɲ�ȡ�Ĵ�ʩ��________
a����߷�Ӧ�¶�
b������Ӧ��ϵ��ѹǿ
c��ѡȡ���ʵĴ���
d����ʱ���ջ��Ƴ�����CO2
e�������ʯ,ʹ����ƽ���������ֽӴ�
��.��¯���������ķ����е�CO�ɽ��л���,ʹ����һ�������º�H2��Ӧ�Ʊ��״�:
CO(g)+ 2H2(g) CH3OH(g)�������ͼʾ�ش���������: CH3OH(g)�������ͼʾ�ش���������:
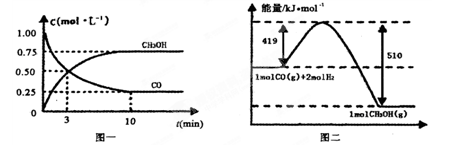
��1���ӷ�Ӧ��ʼ��ƽ��,��H2Ũ�ȱ仯��ʾƽ����Ӧ����v(H2)=________
��2�������¶Ⱥ�������ͬ�������ܱ�������,����ͬ��ʽͶ�뷴Ӧ��,��÷�Ӧ�ﵽƽ��
�ο��𰸣�
���������
�����Ѷȣ�����
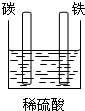
4��ѡ���� ����װ�����ܹ���ԭ��ص��ǣ�������
A��
B��

C��
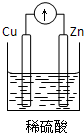
D��
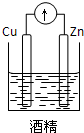
�ο��𰸣�A��û���γɱպϻ�·�����ܹ���ԭ��أ���A����
B���缫��ͬ�����ܹ���ԭ��أ���B����
C�����Ϲ���ԭ��ص��������ܹ���ԭ��أ���C��ȷ��
D���ƾ����ǵ���ʣ����ܹ���ԭ��أ���D����
��ѡC��
���������
�����Ѷȣ���
5��ѡ���� �����ͼ�жϣ�����������ȷ����
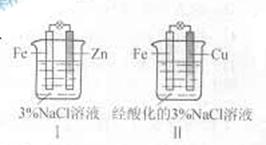
A����͢���������������
B����͢��и�����Ӧ����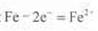
C����͢���������Ӧ����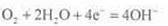
D����͢��зֱ��������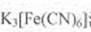 ��Һ��������ɫ���� ��Һ��������ɫ����
�ο��𰸣�A
�����������
�����Ѷȣ���
| 