微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知某粒子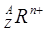 ,则元素R的原子序数是(?)。
,则元素R的原子序数是(?)。
A.Z
B.A-Z
C.Z-n
D.Z+n
参考答案:A
本题解析: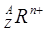 表示质子数为Z。质量数为A,带有n个正电荷的阳离子。因此元素R的原子序数是Z。选项为A。
表示质子数为Z。质量数为A,带有n个正电荷的阳离子。因此元素R的原子序数是Z。选项为A。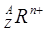 各个角标的含义的知识。
各个角标的含义的知识。
本题难度:简单
2、填空题 A、B、C、D、E为五种常见的短周期元素,常温下,A、B可形成B2A2和B2A两种液态化合物,B与D可组成分子X,X水溶液呈碱性,C元素的焰色反应呈黄色,E与C同周期,且E的简单离子半径是同周期元素形成的简单离子中半径最小的。试回答:
(1)D元素在周期表中的位置为?。
(2)B2 A和X的分子结合质子的能力不同,只用一个离子方程式就能证明,写出该离子反应方程式?。
(3)A、D、E三种元素形成的盐(化学式A9D3E)的水溶液呈酸性,用离子方程式解释其原因?;
(4)W、Q是由A、B、C、D四种元素中任意三种组成的不同类型的强电解质,常温下0.1mol・L―1W的水溶液的pH为13,Q的水溶液呈酸性且能和W反应放出气体,物质的量浓度相同的 W、Q溶液中水的电离程度是前者小于后者。则:W为?,Q为?(填化学式)。
(5)B和E形成的化合物E2B6常在有机合成中作强还原剂,甚至可将二氧化碳重新还原成甲烷,写出该反应方程式?。
(6)已知工业合成X的反应方程式:D2 (g)+3B2 (g) 2X(g);△H ="-92.4" kJ・mol-1,在适当的催化剂和恒温恒压条件下反应,下列说法正确的有?。
2X(g);△H ="-92.4" kJ・mol-1,在适当的催化剂和恒温恒压条件下反应,下列说法正确的有?。
A.达到化学平衡时,正逆反应速率相等
B.反应过程中不断分离出X,使平衡常数K减小,平衡正向移动有利于合成X
C.达到平衡后,升高温度,平衡常数K增大,B2的转化率降低
D.达到化学平衡的过程中,气体平均相对分子质量减小
参考答案:
(1)第二周期ⅤA族?
(2)H3O++NH3=NH4++H2O
(3)Al3++3H2O Al(OH)3+3H+?
Al(OH)3+3H+?
(4)W? NaOH?,Q? NH4NO3 ?
(5)3CO2+2Al2H6=3CH4+2Al2O3?
(6)A
本题解析:根据题意得出A、B、C、D、E元素分别为O、H、Na、N、Al。(2)结合质子(H+)的能力不同,可以通过一种物质把另一种物质中结合的质子夺走来加以证明;(3)A、D、E三种元素形成的盐为Al(NO3)3,铝离子水解溶液呈酸性;(4)常温下0.1mol・L―1W的水溶液的pH为13,即氢氧根离子浓度为0.1mol・L―1,确定为一元强碱溶液,故为A为NaOH;Q的水溶液呈酸性且能和W反应放出气体,确定为NH4NO3;(6)A、平衡状态的标志,正逆反应速率相等,正确;B、温度不变,平衡常数不变,错误;C、反应为放热反应,升高温度平衡逆向移动,平衡常数变小,反应物转化率降低,错误;D、在达到平衡的过程中,随反应进行气体的物质的量变少,但总质量不变,摩尔质量变大,错误。
本题难度:困难
3、选择题 2003年,IUPAC(国际纯粹与应用化学联合会)推荐原子序数为110的元素的符号为Ds,以纪念该元素的发现地(Darmstadt,德国)。下列关于Ds的说法不正确的是(?)
A.Ds原子在周期表中位于第7周期第ⅦB族
B.Ds是过渡元素
C.Ds原子的核外电子数为110
D.Ds为金属元素
参考答案:A
本题解析:
A.不正确,第7周期最后一种元素为118号,往前去掉一个0族,5个主族,2个副族,Ds原子在周期表中位于第7周期第Ⅷ族;B、C、D均正确。
本题难度:简单
4、选择题 X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是(?)
A.元素非金属性由弱到强的顺序为Z<Y<X
B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4
C.3种元素的气态氢化物中Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z<Y<X
参考答案:A
本题解析:X原子的最外层电子数是其电子层数的3倍,说明X不可能是3层或1层电子,所以X是O元素;则Y是S元素,Z是P元素。A、非金属性的强弱是O>S>P,正确;B、S的最高价氧化物对应水化物的化学式可表示为H2YO4,错误;C、3种元素的气态氢化物中X的气态氢化物最稳定,错误;D、原子半径有电子层数、核电荷数决定,所以原子半径由大到小的顺序为X<Y<Z,错误,答案选A。
本题难度:一般
5、选择题 下列排序不正确的是
A.原子半径:钠>硫>氯
B.最高价氧化物对应的水化物的酸性:H3PO4<H2SO4<HClO4
C.最高正化合价:氯>硫>磷
D.热稳定性:碘化氢>溴化氢>氯化氢
参考答案:D
本题解析:A 正确,钠、硫、氯为同一周期元素,从左到右半径逐渐减小
B 正确,P、S、Cl非金属性逐渐增强,最高价含氧酸的酸性也逐渐增强。
C 正确,P、S、Cl最外层电子数逐渐增大,最高正化合价也逐渐增大。
D 错误,非金属性越强,氢化物的稳定性就越强,应该是碘化氢<溴化氢<氯化氢
本题难度:一般