微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 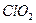 是一种常用的预防“禽流感”的消毒剂,可通过以下反应制得(未配平):
是一种常用的预防“禽流感”的消毒剂,可通过以下反应制得(未配平):
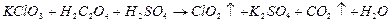
下列说法正确的是?
A.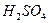 做氧化剂
做氧化剂
B.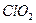 是氧化产物
是氧化产物
C.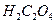 被氧化
被氧化
D.每消耗lmol 就有2mol电子转移
就有2mol电子转移
参考答案:C
本题解析:略
本题难度:一般
2、填空题 据新闻媒体报道,误食亚硝酸钠已造成多起人畜中毒事件,因为它外观类似食盐又有像食盐一样的咸味。亚硝酸钠能引起人体中毒。已知亚硝酸钠能发生如下反应:
NaNO2+HI――NO↑+I2+NaI+H2O
(1)上述反应中,氧化剂是__________,若有0.05 mol还原剂被氧化,则被还原的氧化剂是____________mol。
(2)根据上述反应,可以用试纸和一些生活中常见的物质进行实验,以鉴别亚硝酸钠和食盐。可供选用的物质有:①自来水,②碘化钾淀粉试纸,③淀粉,④白糖,⑤食醋,⑥白酒。进行实验时,必须使用的物质有(填编号)____________。
(3)某厂废切削液中有2%―5%NaNO2,直接排放会造成环境污染,在下列试剂中:①NaCl,②NH4Cl,③H2O2④浓H2SO4,能使NaNO2转化为不引起二次污染的N2的是(填编号)_________,化学方程式为___________________________________________。
参考答案:(1)NaNO2? 0.05?(2)②⑤?(3)②? NH4Cl+NaNO2====N2↑+NaCl+2H2O
本题解析:(1)根据反应方程式中价态变化可知NaNO2中N的化合价降低,被还原,NaNO2作氧化剂,
又因为2NaNO2+4HI====2NO↑+I2+2NaI+2H2O
所以参加反应的HI有一半被氧化,被还原的氧化剂是0.05 mol。
(2)根据题意可知鉴别NaNO2与NaCl只能利用(1)中反应,在酸性条件下,NaNO2可把I-氧化成I2,故选用②⑤。
(3)②,NH4Cl+NaNO2====N2↑+NaCl+2H2O
本题难度:简单
3、选择题 8NH3?+ 3Cl2?="=" 6NH4Cl + N2的反应中,若有8 mol的NH3被氧化,则
A.有3 mol Cl2被还原
B.氧化产物为1 mol
C.氧化产物为8 mol
D.生成N24 mol
参考答案:D
本题解析:本题考查氧化还原反应的有关计算。由反应前后元素的化合价变化可知,氯气作氧化剂(由0价降低到-1价);但氨气作还原剂(N的化合价由-3价升高到0价),8mol氨气中只有2mol作还原剂。所以若有8 mol的NH3被氧化时,被还原的氯气应是12mol,A不正确;8 mol的NH3被氧化,则氧化产物N2的物质的量是4mol,B、C不正确,D正确。
本题难度:简单
4、填空题 将0.08mol KMnO4固体(质量为12.64g)加热一段时间后,收集到a molO2;向反应后残留的固体中加入足量的浓盐酸,又收集到b molCl2,此时Mn元素全部以Mn2+的形式存在于溶液中。
(1)请配平下列方程式:
KMnO4+?HCl -?KCl+?MnCl2+?Cl2↑+?H2O
(2)上式反应中的还原剂是?,当还原剂失去1mol电子时,氧化产物的物质的量为?。
(3)a +b的最大值为?,a +b最小值为?。
(4)当 a +b =0.18时,残留固体的质量为?。
参考答案:(1)2? 16? 2? 2? 5? 8?(2)HCl? 0.5?(3)0.2? 0.16?(4) 12g.
本题解析:本题综合考查重要的化学基本概念――氧化还原反应的配平及计算,利用字母进行讨论分析、解决问题的能力,属于较高要求――综合应用层次。
(1)配平时注意不要漏掉等号。
(2)依据化合价变化情况,可较容易判断出还原剂是HCl,再弄清氧化产物是对应还原剂,即可得出结果。
(3)经对题目涉及的反应分析可知:a+b的最大值为只产生氯气时,即a=0时;则b=0.2,∴a+b="0.2?" a+b的最小值为产生氧气为最大量时,根据方程式可知产生氧气0.04mol,即a=0.04时;根据电子守恒知产生的二氧化锰还可氧化盐酸产生氯气的量:即b为=0.12,∴a+b=0.16
(4)当a+b=0.18时,4a+2(0.18-a)=0.4,a=0.02,
即:产生氧气:0.02mol×32g・mol-1=0.64g
由质量守恒可求出残留固体12g。
本题难度:简单
5、选择题 Cl2在70℃的NaOH水溶液中,能同时发生两个自身氧化还原反应,反应完全后测得溶液中NaClO和NaClO3的物质的量比为4∶1,则溶液中NaCl和NaClO的物质的量之比为:
A.9∶4
B.5∶1
C.11∶2
D.1∶1 ( )
参考答案:A
本题解析:略
本题难度:一般