微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 元素的性质在元素周期表中按其排列呈现一定的规律。下表为元素周期表中部分元素,根据要求回答下列问题:
K
| Ca
| Sc
| Ti
| V
| Cr
| Mn
| Fe
| Co
| Ni
| Cu
| Zn
| Ga
| Ge
|
?
(1)在以上元素的基态原子的电子排布中4s轨道上只有1个电子的元素有?(填元素名称)。
(2)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域:s区、p区、d区、ds区和f区,以上12种元素分别属于s区、d区、ds区和p区,则属于s区的元素有?种,属于d区的元素有?种。
(3)铜晶胞是面心立方结构。其空间利用率为?(用含“π”和“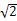 ”的式子表示,不必算结果)
”的式子表示,不必算结果)
参考答案:(1)钾,铬,铜(2)2? 8 (3)π/ (3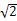 )
)
本题解析:(1)当原子核外各个轨道上的电子处于全充满、半充满、全空时是稳定的状态。在给定的元素中,K的核外电子排布为:1s22s22p63s23p64s1.最外层只有1个电子;Cr的核外电子排布为:1s22s22p63s23p63d54s1.最外层只有1个电子;Cu的核外电子排布为:1s22s22p63s23p63d104s1.最外层只有1个电子;因此在以上元素的基态原子的电子排布中4s轨道上只有1个电子的元素有钾,铬,铜。(2)属于s区的元素有K、Ca两种元素;属于d区的元素有Sc、Ti、V、Cr、Mn、Fe、Co、Ni8种元素。(3)铜晶胞是面心立方结构。在每个晶胞中含有的Cu原子的个数为8×1/8+6×1/2=4.假设晶胞的边长为a,Cu原子的半径为R,则 a=4R.a=2
a=4R.a=2 R.晶胞的体积为a3=16
R.晶胞的体积为a3=16 R3.4个Cu原子的体积为:4×4/3ПR3=16ПR3/3.所以在Cu晶体中的空间利用率为(16πR3/3)÷16
R3.4个Cu原子的体积为:4×4/3ПR3=16ПR3/3.所以在Cu晶体中的空间利用率为(16πR3/3)÷16 R3="π/" (3
R3="π/" (3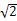 )。
)。
本题难度:一般
2、选择题 下列离子中,用来除去溶液中的镁离子效果最好的是
A.CO32-
B.OH-
C.SO42-
D.Cl-
参考答案:B
本题解析:分析:根据除去溶液中的镁离子用沉淀法以及碳酸镁、氢氧化镁、硫酸镁、氯化镁的溶解度.
解答:因硫酸镁、氯化镁都易溶于水,碳酸镁微溶于水、氢氧化镁难溶于水、要使溶液中的镁离子完全沉淀下来,应加入OH-使它形成难溶性的氢氧化镁,故选:B.
点评:本题主要考查了镁离子的除杂,抓住碳酸镁和氢氧化镁的性质是解题的关键.
本题难度:简单
3、选择题 下列关于电负性的叙述中不正确的是( )
A.电负性用来描述不同元素的原子对键合电子吸引力的大小
B.电负性是以氟为4.0、锂为1.0作为标准的相对值
C.元素电负性越小,元素金属性越强
D.元素电负性越大,元素非金属性越强
参考答案:C
本题解析:钙的金属性强于钠的,但电负性也大于钠的,所以选项C不正确,其余选项都是正确的,答案选C。
点评:该题是基础性试题的考查,试题难易适中,注重基础,侧重能力的培养和训练。该题的关键是明确电负性的含义和变化规律,然后灵活运用即可。
本题难度:一般
4、选择题 下列气体中,不能用排空气取气法收集的是
A.Cl2
B.SO2
C.NO
D.NH3
参考答案:C
本题解析:试题分析:不能用排空气法收集的气体应该是和空气中某些成分发生反应或者密度和空气的相差不大,选项中只有C项NO可以被氧气氧化为NO2,所以选择C。
考点:考查常见气体实验室收集方法
点评:熟悉常见气体的收集方法并能灵活应用,此题属于简单题型
本题难度:一般
5、选择题 研究下表信息可直接得出的结论是
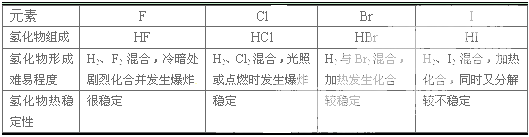
A.元素性质随原子序数的递增而呈周期性变化
B.同周期元素的非金属性随原子序数递增而增强
C.第VII A族元素的金属性随电子层数增加而减弱
D.第VIIA族元素的非金属性随电子层数的增加而减弱
参考答案:D
本题解析:表中只列出了第VIIA的四元素的氢化物性质的递变性,所以答案为D
本题难度:一般