��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �й���ͼ��˵����ȷ����(? )
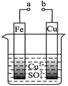
A��a��b���ӹ���ԭ��أ���Һ��SO42������Cu��
B��a��b���ӹ���ԭ��أ�Cu���Ϸ�����ԭ��Ӧ
C��a��b�ֱ��ֱ����Դ�������������Ӵ�CuƬ����b
D��a��b�ֱ��ֱ����Դ����������������FeƬ�϶�Cu
�ο��𰸣�B
�����������ͼ��a��b���ӣ����װ���γ�ԭ��أ���Fe��������ʧȥ���ӱ���������Һ��SO42-���ƶ���Cu��������Cu2+�õ����ӱ���ԭ����Һ��Cu2+�������ƶ�������A����B��ȷ����a��b�ֱ��ֱ����Դ�������������װ���γ��˵��أ�Fe��������Feʧȥ���ӷ���������Ӧ���ܽ⣬Cu��������Cu2+�õ�������ͭƬ������ͭ������C��D������ѡB��
�����Ѷȣ�һ��
2������� ij�����ų��ķ�ˮ�к��д�����Fe2+��Cu2+��SO42-��Ϊ�˼�����Ⱦ�����Ϊ��������ʦ��������������̣��Ի���ͭ��������������ش�
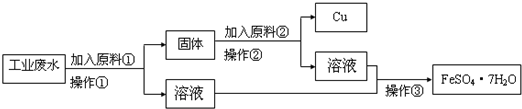
��1��ԭ�Ϣ�Ϊ______���ѧʽ����
��2��д������ԭ�Ϣں�Ӧ�����ӷ���ʽ��______��
��3������ʵ��������ɸ����̣���������Ҫ�õ��IJ���������������______��
______��______������ʵ����������в������õ���װ����______������ĸ����
�ο��𰸣���1����������֪���������ܺ�ͭ���ӷ�Ӧ�Ҳ������µ��������ӣ�����ֻ���������ʴ�Ϊ��Fe��
��2���������м��������������ʹͭ������ȫ��Ӧ���������ù���ijɷ�������ͭ����������ͭ�һ���ͭ�����Լ���ij����������Ӧ����ͭ����Ӧ����������Ӧ��������������������Һ�����ʵijɷ�һ�������������ֻ����ϡ���ᣬ���Է��������ӷ�ӦΪFe+2H+�TFe2++H2�����ʴ�Ϊ��Fe+2H+�TFe2++H2����
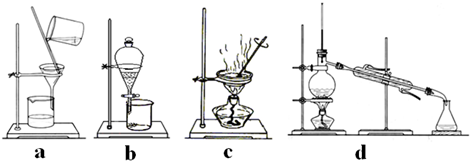
��3�������ڵķ����ǹ��塢Һ����룬����Ӧ�ù��˵ķ��������õ��IJ��������в�������©�����ձ���
�����١��ڵķ����ǹ��塢Һ����룬����Ӧ�ù��˵ķ�������������������ˮ�֣�ʹ���ʴ���Һ������������Ӧ�������ᾧ�ķ�����
a����װ���ǹ���װ�ã���������Һ�壻
b����װ������ȡװ�ã������ܽ�ȵIJ�ͬ���룻
c����װ���������ᾧװ�ã������ܼ������ʣ�
d����װ��������װ�ã����ݷе�IJ�ͬ����Һ���Һ�壻
����ѡbd
�ʴ�Ϊ����������©�����ձ���bd��
���������
�����Ѷȣ�һ��
3��ѡ���� ��0.1 L����0.02mol CuSO4��0.01 molNaCl��ˮ��Һ�ö��Ե缫��⡣���һ��ʱ���һ�缫�ϵõ�0.01 mol Cu����һ�缫����������
A��ֻ��Cl2
B������Cl2����O2
C��ֻ��O2
D��ֻ��H2
�ο��𰸣�B
���������
�������ѧ��Ӧ��ǵ��ʱ���������ӷŵ�˳�����������������ԭ��Ӧ��ץס������ԭ��Ӧʵ�ʾ��ǵ���ת�ƣ��������ǣ����ӵ�ʧ��ȡ�
������Ӧ��Cu2+ + 2e- =" Cu"
����0.01 mol Cu ת�Ƶ��ӹ���0.01��2 =" 0.02" mol
������Ӧ����ֻ��? 2Cl-�� 2e- = Cl2�� ?��ת�Ƶ���ֻ�У�0.01 mol ?
��Ӧ������Ϊ��0.01��2 =" 0.005" mol
��ˣ�������Ӧ���У�4OH-�� 4e- = 2H2O + O2�� ���Ҵ˷�Ӧ��ת�Ƶ���Ϊ��0.01mol ?
��Ӧ������Ϊ��0.01��4 =" 0.0025" mol
�����Ѷȣ���
4��ѡ���� ͭ������í�����ϳ�ʱ��ؽ����ں�ˮ�л������������ã��丯ʴԭ������ͼ��ʾ�������йش˹��̵�˵������ȷ����
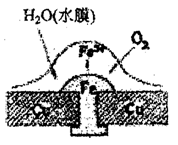
A�������ϵ���Ҫ�缫��ӦʽΪ��
B���˹�����ͭ��δ����ʴ
C�����Ӵ�Cu����Fe
D���˹����л������漰����Ӧ��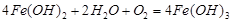
�ο��𰸣�C
�����������������ĵ绯ѧ��ʴ
A����ȷ
B��ͭ����ص���������δ������ѧ��Ӧ����ȷ
C������Ӧ����Ի��õĸ���������������ȷ
D���绯ѧ��ʴ�IJ���Fe(OH)2�ɱ���������ΪFe(OH)3����ȷ
�����Ѷȣ�һ��
5������� ��ҵ�ϲ��õ�һ����ˮ������������:������ˮ��pH��5.0~6.0֮��,ͨ���������Fe(OH)3������Fe(OH)3��������,�������������������,���о���ˮ�����á��������������ݰ���ˮ�����������ˮ���γɸ�����,��ȥ(��Ʋ��)������,�����˸�ѡ���������á�ij����С���ø�ԭ��������ˮ,���װ��ʾ��ͼ��ͼ��ʾ��
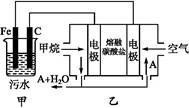
(1)ʵ��ʱ����ˮ������Ũ�Ƚ�С,���������ϲ�,�����������ʻ���,��ʹ�������γɸ�������ʱӦ����ˮ�м�������������������?
a.H2SO4��b.CH3CH2OH��c.Na2SO4
d.NaOH��e.BaSO4
(2)��������ʵ�ʷ����������缫��Ӧ,����һ����Ӧ����һ����ɫ����,�������ĵ缫��Ӧʽ�ֱ��Ǣ�.��������������;��.����������������?
(3)��ȼ�ϵ����������̼����Ϊ�����,CH4Ϊȼ��,����Ϊ������,ϡ�������������缫��Ϊ��ʹ��ȼ�ϵ�س�ʱ���ȶ�����,��صĵ�������Ӧ�����ȶ�,��ع���ʱ�����в���A���ʲμ�ѭ��(����ͼ)��A���ʵĻ�ѧʽ��������������������?
(4)��֪ȼ�ϵ������1.6 g CH4�μӷ�Ӧ,��C�缫�������������������� L(��״��)��?
�ο��𰸣�(1)c��(2)Fe-2e- Fe2+��4OH--4e-
Fe2+��4OH--4e- O2��+2H2O��(3)CO2��(4)8.96
O2��+2H2O��(3)CO2��(4)8.96
���������H2SO4�����ԡ�CH3CH2OH�Ƿǵ���ʡ�NaOH�Լ��ԡ�BaSO4������ˮ;Na2SO4��ǿ�����������,���ʱNa+��S �����ŵ�,ֻ��c����;(2)��װ��ͨ������ĵ缫Ϊԭ�������,���Լ�װ��FeΪ����,��ʧ����,������һ����ɫ�����֪����������,���Ի���OH-ʧ����;(3)�����е���ʿ�֪,����ȼ������CO2��H2O,����AΪCO2,�����������缫��ӦʽΪO2+4e-+2CO2
�����ŵ�,ֻ��c����;(2)��װ��ͨ������ĵ缫Ϊԭ�������,���Լ�װ��FeΪ����,��ʧ����,������һ����ɫ�����֪����������,���Ի���OH-ʧ����;(3)�����е���ʿ�֪,����ȼ������CO2��H2O,����AΪCO2,�����������缫��ӦʽΪO2+4e-+2CO2 2C
2C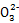 ;(4)���ȱ껯�ϼۿ����ϼ۱仯:
;(4)���ȱ껯�ϼۿ����ϼ۱仯: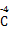 H4��
H4��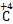 O2,0.1 mol CH4ת��0.8 mol����,C�缫��ӦΪ2H++2e-
O2,0.1 mol CH4ת��0.8 mol����,C�缫��ӦΪ2H++2e- H2��,��������n(H2)="0.4" mol
H2��,��������n(H2)="0.4" mol
�����Ѷȣ�һ��