微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 工业上生产Na、Ca、Mg都用电解其熔融的氯化物,但钾却不能用电解熔融KCl的方法制得,因金属钾易溶于熔融态的KCl中而有危险,难获得钾,且降低电流效率。现生产钾是用属钠和熔化的KCl在一定的条件下反应制取:
 ? KCl + Na?NaCl + K + Q (Q<0)
? KCl + Na?NaCl + K + Q (Q<0)
有关数据如下表:
?
| 熔点℃
| 沸点℃
| 密度(g/cm3)
|
Na
| 97.8
| 882.9
| 0.97
|
K
| 63.7
| 774
| 0.86
|
NaCl
| 801
| 1413
| 2.165
|
KCl
| 770
| 1500(升华)
| 1.984
|
(1) 工业上制取金属钾的化学原理是?,在常压下金属钾转为气态从反应混合物中分离的最低温度约为?,而反应的最高温度应低于?。
(2)在制取金属钾的过程中,为了提高原料的转化率可采取的措施是?。
(3)生产中常向反应物中通入一种气体,并将从反应器中导出的气体进行冷却得到金属钾,?
且将该气体可循环利用,该气体是________。
a.干燥的空气? b.氮气? c.二氧化碳? d.稀有气体
(4)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为K=?。
参考答案:(1) 化学平衡移动原理(勒夏特列原理/钾蒸汽逸出使生成物浓度减小,平衡向正反应方向移动,可不断得到金属钾) 774℃? 882.9℃?(每空1分,共3分)?
(2) 适当的升高温度、降低压强或移去钾蒸气 (2分)?
(3)d (1分)?
(4)?c(K)/c(Na) (1分)
本题解析:略
本题难度:一般
2、选择题 将分别盛有熔融的KCl、MgCl2和Al2O3的三个电解槽串联,在一定条件下通电一段时间后,析出K、Mg、Al的物质的量之比为( )
A.1:2:3
B.3:2:1
C.6:3:1
D.6:3:2
参考答案:串联电路中电流强度相等,即通过的电子数相等,
由:KCl~1e-~K;MgCl2~2e-~Mg;Al2O3~6e-~2Al可知,
当通过1 mol电子时分别析出K、Mg、Al的物质的量为1、12、13,
故其物质的量之比为1:12:13=6:3:2,
故选D.
本题解析:
本题难度:一般
3、选择题 如图所示,各烧杯中盛有海水,铁(含杂质C)在其中被腐蚀由快到慢的顺序为( )
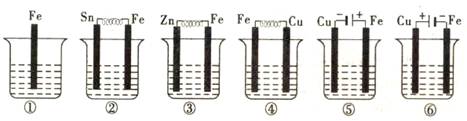
A.⑤④②①③⑥ B.⑤④③①②⑥ C.②①③④⑤⑥ D.⑤③②④①⑥
参考答案:A
本题解析:当铁作为电解池的阳极时,其腐蚀的速度是最快的,当作为电解池的阴极是,其腐蚀速率是最慢的,当铁与金属构成原电池时,铁作为负极时,两者金属的活动性相差越大,铁的腐蚀速率就越大,但铁作为负极时,即铁的腐蚀速率就会减慢,所以铁(含杂质C)在其中被腐蚀由快到慢为⑤④②①③⑥,故本题的答案选择A。
考点:原电池、电解池
点评:本题考查了原电池、电解池的运用,这些知识点是高考考查的重点和难点,本题难度适中,关键是要掌握当铁作为电解池的阳极时,其腐蚀的速度是最快的,当作为电解池的阴极是,其腐蚀速率是最慢的,当铁与金属构成原电池时,铁作为负极时,两者金属的活动性相差越大,铁的腐蚀速率就越大,但铁作为负极时,即铁的腐蚀速率就会减慢。
本题难度:简单
4、选择题 现将氯化铝溶液蒸干灼烧并熔融后用铂电极进行电解,下列有关电极产物的判断正确的是
[? ]
A.阴极产物是氢气
B.阳极产物是氧气
C.阴极产物是铝和氧气
D.阳极产物只有氯气
参考答案:B
本题解析:
本题难度:一般
5、选择题 如图所示,a、b、c、d均为石墨电极,通电一段时间后,各电极上的生成物的物质的量之比依次为4:1:2:2,则甲、乙两池中的电解质分别是( )
A.AgNO3、KBr
B.CuSO4、NaNO3
C.稀H2SO4、Cu(NO3)2
D.NaOH、稀H2SO4
