��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ͭƬ�϶���ʱ������������ȷ���ǣ�?��
�ٽ�ͭƬ���ڵ�ص������ϣ��ڽ���Ƭ���ڵ�Դ�������ϣ�����ͭƬ�Ϸ����ķ�Ӧ�ǣ�Ag++e-=Ag��������Ƭ�Ϸ����ķ�Ӧ�ǣ�4OH--4e-=O2+2H2O��������CuSO4��Һ��������AgNO3��Һ�����Һ
A���٢ۢ�
B���ڢۢ�
C���٢ܢ�
D���ڢۢܢ�
�ο��𰸣�B
������������ʱ�����ƽ����������͵�Դ�ĸ����������Ʋ�������������͵�Դ���������������жƲ�������ӵ���Һ�ǵ������Һ����������ͭƬ�϶���ʱ��ͭ�͵�Դ�ĸ������������͵�Դ�������������������ǵ������Һ����ѡB��
�����������ǵ��ԭ��Ӧ�õĿ��飬��Ҫ�ǿ���ѧ���Ե��ԭ������Ϥ�˽�̶ȣ����ڹ���ѧ���Ļ��������ѧ��������������Ĺؼ�����ȷ���صĹ���ԭ����Ȼ��������������ü��ɡ�
�����Ѷȣ�һ��
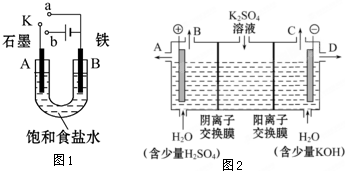
2������� ij����С������ͼ1װ�ý���ʵ�飬�Իش��������⣮
��1������ʼʱ����K��a���ӣ���B���ĵ缫��ӦʽΪ______��
��2������ʼʱ����K��b���ӣ���B���ĵ缫��ӦʽΪ______���ܷ�Ӧ�����ӷ���ʽΪ______���й�����ʵ�飬����˵����ȷ���ǣ�����ţ�______��
����Һ��Na+��A���ƶ�
�ڴ�A�����ݳ���������ʹʪ���KI������ֽ����
�۷�Ӧһ��ʱ������������ɻָ������ǰ����ʵ�Ũ��
������״����B������2.24L���壬����Һ��ת��0.2mol����
��3����С��ͬѧ��Ϊ�����ģ�ҵ�����ӽ���Ĥ�����ռ�ķ�������ô������������ͼ2װ�õ���������Һ����ȡ������������������������أ�
�ٸõ��۵�������ӦʽΪ______��
��ʱͨ�������ӽ���Ĥ��������______������ڡ�����С�ڡ����ڡ���ͨ�������ӽ���Ĥ����������
�������Ƶõ�����������������������Һ���Ϊ����ȼ�ϵ�أ����������ĵ缫��ӦʽΪ______��
�ο��𰸣���1����ʼʱ����K��a�����γ�ԭ��ط�Ӧ��B�缫��������ʧ���������������ӣ��缫��ӦΪ��Fe-2e-=Fe2+���ʴ�Ϊ��Fe-2e-=Fe2+��
��2������K��b���ӣ�װ��Ϊ���أ���Ϊ������������ԭ��Ӧ�������ӵõ�����������������B�缫��ӦΪ2H++2e-=H2������ⱥ��ʳ��ˮ�����������ơ�����������������ܷ�Ӧ�����ӷ���ʽΪ2Cl-+2H2Oͨ��.2OH-+H2��+Cl2����
�ٵ��������������������ƶ���BΪ�������ʢٴ���
��A������������ʹʪ��KI������ֽ�������ʢ���ȷ��
�۷�Ӧһ��ʱ��������HCl���壬�ɻָ������ǰ����ʵ�Ũ�ȣ����Ǽ������ᣬ�ʢ۴���
������״����B������2.24L������Ϊ�������ʵ���Ϊ0.1mol�����ݵ缫��Ӧ���㣬��2H++2e-=H2���õ���Һ��ת��0.2mol���ӣ��ʢ���ȷ��
�ʴ�Ϊ��2H++2e-�TH2����2Cl-+2H2Oͨ��.2OH-+H2��+Cl2�����ڢܣ�
��3���ٵ��ʱ��������ʧ���ӷ���������Ӧ����Һ�е����������ӵķŵ�����������������ӵķŵ���������������������������ʧ��������ˮ������4OH--4e-=2H2O+O2�����������������ӷŵ磬�������������������ƶ������������ӷŵ磬����������������ƶ�������ͨ����ͬ����ʱ��ͨ�������ӽ���Ĥ��������С��ͨ�������ӽ���Ĥ����������
�ʴ�Ϊ��4OH--4e-=2H2O+O2����С�ڣ�
��ȼ��ԭ����У�ȼ���ڸ�����ʧ���ӷ���������Ӧ���������������ϵõ��ӷ�����ԭ��Ӧ����ȼ��ԭ����У������������������������������ϵõ��Ӻ�ˮ��Ӧ�������������ӣ��缫��ӦʽΪO2+2H2O+4e-=4OH-��
�ʴ�Ϊ��O2+2H2O+4e-=4OH-��
���������
�����Ѷȣ�һ��
3��ѡ���� ���ϡH2SO4��Cu(NO3)2��NaCl�Ļ��Һ�����һ��ʱ�������������Ϸֱ����������ʷֱ��ǣ�?��
A��H2��Cl2
B��Cu��Cl2
C��H2��O2
D��Cu��O2
�ο��𰸣�B
��������������������жϡ����Ե缫���ʱ����������Һ�е�������ʧȥ���ӣ���������Һ�е������ӵõ����ӡ��������Ӷ�ŵ�˳���֪�����������ͭ���ӵõ���������ͭ��������������ʧȥ���ӣ��������������Դ�ѡB��
�����Ѷȣ�һ��
4��ѡ���� 1 Lij��Һ�к��е��������±���
����
| Cu2��
| Al3��
| NO
| Cl��
|
���ʵ���Ũ��(mol/L)
| 1
| 1
| a
| 1
|
�ö��Ե缫������Һ������·����3 mol e��ͨ��ʱ(���Ե��ʱ��Һ����ı仯���缫������ܴ��ڵ��ܽ�����)������˵����ȷ����( )
A��������Һ��pH��0 B��a��3
C����������1.5 mol Cl2 D�����������Ľ�����ͭ����
�ο��𰸣�A
������������ݵ����غ��֪���÷�Ӧ�������漰�ķ�Ӧ�У�������2Cl����2e��=Cl2��(�����������������״����Ϊ0.5 mol)��4OH����4e��=2H2O��O2����������Cu2����2e��=Cu,2H����2e��=H2�����ӵ����غ�ĽǶ�֪��������Һ��pH��0��A����ȷ���ӵ���غ�ĽǶȿ�֪��a��4��B����ȷ��
�����Ѷȣ�һ��
5��ѡ���� ����˵����ȷ����
A������Ȼ�þ������Һ�����Ƶý���þ
B��ú�ɾ������ýྻ��ȼ��
C���ǽ��������в����Ժ��н���Ԫ��
D���ö����ЧӦ�������ֽ������Һ
�ο��𰸣�D
�����������
�����Ѷȣ�һ��