微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (13分)已知:正盐A强热可得到B、C、D、E四种物质,B通常情况下为无色无味液体,E、F 是空气主要成分,D能产生酸雨,I为红棕色气体,C与J反应可得A,J、K为两种常见的酸。物质之间的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。 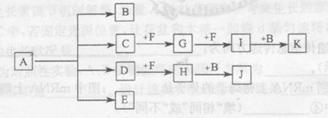
请回答下列问题:
(1)E物质的电子式是________。
(2)检验C的试纸是________,检验D的试剂是________(填试纸、试剂名称)。
(3)写出A强热分解生成B、C、D、E的化学方程式________。
(4)写出D通人FeCl3溶液时,发生反应的离子方程式_____ 。
(5) ―定浓度J、K混合后的稀溶液200mL,平均分成两份。向其中一份中逐渐加人铜粉,最多能溶解a g(产生气体只为G)。向另一份中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示。则①a=________g,②气体G标准状况下体积为________,③J的物质的量浓度为______。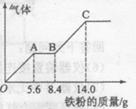
参考答案:(13分)(1) (2分) (2)红色石蕊试纸?品红溶液 (2分)
(2分) (2)红色石蕊试纸?品红溶液 (2分)
(3)3(NH4)2SO4 6H2O+4NH3↑+3SO2↑+N2↑ (3分)
6H2O+4NH3↑+3SO2↑+N2↑ (3分)
(4)SO2+2Fe3++2H2O=SO42-+2Fe2++4H+ (3分)
(5)①9.6g (1分) ②2.24L (1分) ③2.5mol/L (1分)
本题解析:B通常情况下为无色无味液体,因此B应该是水。E、F 是空气主要成分,则二者是氮气和氧气。D能产生酸雨,所以D是SO2。SO2能和F反应生成H,则F是氧气,E是氮气,H是三氧化硫。三氧化硫和水反应生成J,J是硫酸。I为红棕色气体,则I是NO2。G和氧气反应生成NO2,所以G是NO。NO2溶于水生成硝酸和NO。K是酸,则K是硝酸。C和氧气反应生成NO,且C与J反应可得A,所以C是氨气,A就是硫酸铵。
(1)氮气是含有非极性键的单质,其电子式是 。
。
(2)氨气是碱性气体,可用红色石蕊试纸检验;SO2具有漂白性,可用品红溶液检验。
(3)A强热分解生成B、C、D、E的化学方程式3(NH4)2SO4 6H2O+4NH3↑+3SO2↑+N2↑。
6H2O+4NH3↑+3SO2↑+N2↑。
(4)SO2具有还原性,能被铁离子氧化,因此该反应的离子方程式是SO2+2Fe3++2H2O=SO42-+2Fe2++4H+。
(5)硝酸是氧化性酸,所以根据图像可知,O→A发生的反应是Fe+4H++NO3-=Fe3++NO↑+2H2O。A→B发生反应的方程式是2Fe3++Fe=3Fe2+;B→C发生反应的方程式是Fe+2H+=Fe2++H2↑。三阶段中消耗铁的物质的量分别是5.6g÷56g/mol=0.1mol、(8.4g-5.6g)÷56g/mol=0.05mol、(14.0g-8.4g)÷56g/mol=0.1mol,所以根据氮元素守恒可知,硝酸的物质的量是0.1mol。最终溶液中只有硫酸亚铁,则根据原子守恒可知,硫酸亚铁的物质的量是0.25mol,因此硫酸的物质的量也是0.25mol,则硫酸的浓度是0.25mol÷0.1L=2.5mol/L。另一份溶液中,氢离子和NO3-的物质的量分别是0.6mol和0.1mol,则根据方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O可知,氢离子过量,所以NO3-完全被还原生成NO,则NO的物质的量是0.1mol,在标准状况下的体积是2.24L。其中溶解铜的质量是0.15mol×64g/mol=9.6g。
本题难度:困难
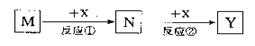
2、选择题 M、N、X、Y四种物质之间有如下转化关系(反应条件和其它产物已略去)。下列选项不符合的是(?)
A.
B.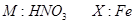
C.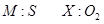
D.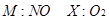
参考答案:D
本题解析:如果M是NO,X是氧气,则N是NO2,但NO2和氧气是不反应的没声音选项D是可不能的,其余都是正确的,答案选D。
本题难度:一般
3、推断题 下图中的反应①是重要的电化学工业反应,反应②可用于制备新型消毒净水剂Na2FeO4。常温下B、C为气态单质,G是当代社会使用量最大的金属,其余均为化合物。(反应时加入或生成的水,以及生成沉淀I时的其他产物均已略去)。

请回答下列问题:
(1)L的电子式为_______________。
(2)J溶液蒸干灼烧得到的物质是(填化学式)_______________。
(3)反应①的化学方程式是____________________________________。
(4)反应②的离子方程式是____________________________________。
(5)Na2FeO4能起到消毒净水的原理是______________________。(用文字叙述)
参考答案:(1)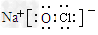 (2)Fe2O3
(2)Fe2O3
(3)2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(4)2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O
(5)Na2FeO4中+6铁具有强氧化性,能起到杀菌消毒作用,其还原产物为+3价铁易水解,形成Fe(OH)3胶体,具有净化作用
本题解析:
本题难度:一般
4、填空题 下图表示有关物质(均是中学化学常见的物质)之间的转化关系(其
中部分参加反应的水和生成的水未列出),其中B、C为金属单质,E为非金属单质,其余均为化合物,Y、Z的组成元素相同,D为淡黄色的固体。回答系列问题:
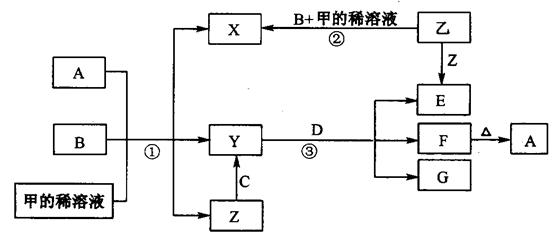
(1)B与甲稀溶液不反应,但与甲的浓溶液在加热条件下能反应。则甲为?,C为?(填写化学式)。
A与B物质的量应满足的关系为?。
(2)写出反应③的化学方程式?。
(3)反应②观察到溶液由无色变成蓝色,并且有无色气泡产生。请写出反应②发生的化学反应方程式?,并分析产生气体的原因?。
参考答案:(1)H2SO4? Fe(2分)? n(A):n(B)≥1:1(2分)
(2)4FeSO4+4Na2O2+6H2O=4Fe(OH)3+4Na2SO4+O2↑(2分)(其他正确答案也可)
(3)Cu+H2O2+H2SO4=CuSO4+2H2O(2分)? 2H2O2=2H2O+O2↑(1分)
Cu2+催化H2O2分解(1分)
本题解析:略
本题难度:简单
5、简答题 有X、Y、Z三种元素:
(1)X、Y、Z的单质在常温下均为气体;
(2)X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色;
(3)XZ极易溶于水,在水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红;
(4)每2个X2分子能与1个Y2分子化合成2个X2Y分子,X2Y常温下为液体;
(5)Z单质溶于X2Y中,所得溶液具有漂白性.
请根据以上信息写出所给化合物的分子式:XZ______,X2Y______.
参考答案:(1)X、Y、Z的单质在常温下均为气体;依据所学单质气体应为H2,O2,Cl2,N2等
(2)X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色;是氯气和氢气反应生成氯化氢产生的现象;
(3)XZ极易溶于水,在水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红;证明XZ为HCl,
(4)每2个X2分子能与1个Y2分子化合成2个X2Y分子,X2Y常温下为液体;
(5)Z单质溶于X2Y中,所得溶液具有漂白性,说明Z为Cl2,X2Y为H2O;
综上所述;X、Y、Z、XZ、X2Y分别为H2,Cl2,HCl,H2O;
化合物XZ的化学式为:HCl;H2Y?化学式为:H2O;
故答案为:HCl;H2O;
本题解析:
本题难度:一般