微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去),下列推断不正确的是(?)
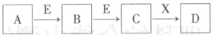
A.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
B.若D是一种强碱,则A、B、C均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可能与铜反应生成B或C
参考答案:A
本题解析:A、若D是一种白色沉淀,在空气中最终变为红褐色,则E是铁,错误;B、若D是一种强碱,则A为Na、B为Na2O、C为Na2O2,都能与E(H2O)反应,正确;C、若D为NaCl,且A可与C反应生成B,则A可能为NaOH、B可能为Na2CO3、C可能为NaHCO3,X可能为HCl、E可能为CO2,正确;D、若D是一种强酸,则A可能为S或N2,也可能为H2S或NH3,D为浓硫酸或浓硝酸或稀硝酸,可与铜反应,正确。
本题难度:一般
2、填空题 (16分)A 、B 、C 、D 、E 、F、G为原子序数依次增大的元素,其中前六种属于短周期元素。已知B 、C 、F 三种原子的最外层共有11 个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应并且生成盐和水。请完成下列问题:
(1)只根据以上条件一定能判断出的元素的及符合条件的离子的符号填写在下表空格处
编号
| A
| B
| C
| D
| E
| F
| G
| 半径最小的离子
|
符号
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
 ?(2)写出B、C 的最高价氧化物对应的水化物间反
?(2)写出B、C 的最高价氧化物对应的水化物间反
应的离子方程式____________
(3)己知D的单质在F单质中燃烧可生成X、Y两
种化合物并产生白色烟雾,写出X、Y中各原子
最外层均满足8 电子结构的分子的电子式___。
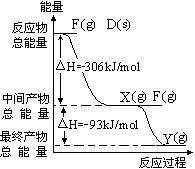
D、F的单质反应过程和能量关系如图所示(图
中的△H表示生成1mol产物的数据),写出指定
条件下两种单质作用生成Y时的热化学方程式
_______________________。
(4) G的单质是目前用途最广泛的一种金属材料,但在使用中受环境影响易被腐蚀,试写出发生腐蚀时的电极反应式_________________________________________。
(5)A与E能形成两种常见的化合物,这两种化合物中属于非极性分子的物质化学式_______
参考答案:(1) 各1分
A
B
C
D
E
F
半径最小的离子
?
Na
Al
?
?
Cl
Al3+
?(2)OH-+Al(OH)3=AlO2-+2H2O(2分)
(3)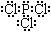 ,P(s)+2.5Cl2(g)=PCl5(g);△H = -399kJ/mol:(各2分)
,P(s)+2.5Cl2(g)=PCl5(g);△H = -399kJ/mol:(各2分)
(4)负极:Fe一2e-=Fe2+,正极:O2+2H2O+4e-=4OH-(各2分) (5)SO3(2分)
本题解析:由B、C、F最高价氧化物对应的水化物的性质知有铝元素,再结合原子序数及价电子数关系知B是钠,C是铝、F是氯;另外四种无法确定,己确定的元素中离子半径最小的是Al3+。由D是与氯气反应现象及产物种类知D是磷,它在氯气燃烧可生成PCl3、PCl5两种物质,其中PCl3满足8电子结构,由图示知,生成1molPCl5时放出的热量是399kJ。由此也可知道E是硫。由有关G的信息知其是铁,发生的腐蚀主要形式为吸氧腐蚀。A是原子序数比钠小的元素,与硫能形成两种常见化合物,故它是氧,其中SO3是非极性分子。
本题难度:一般
3、填空题 某白色粉末A在农业上用作杀菌剂,进行下列实验:
(1)白色粉末溶解在水中,得到蓝色溶液,分成等量的两份
(2)在其中一份蓝色溶液中加入适量的盐溶液B,恰好沉淀完全,过滤,得到白色沉淀和蓝色溶液;向该蓝色溶液中加入AgNO3并加入HNO3,生成白色沉淀且不溶解。
(3)在另一份蓝色溶液中加入适量C溶液,恰好沉淀完全,过滤,得到蓝色沉淀和纯净的硫酸钾溶液。
根据实验现象推断:
A? ?B ??C ?
参考答案:ACuSO4? B BaCl2? C.KOH
本题解析:略
本题难度:简单
4、填空题 (13分)A、B、C、D、E、X、Y为中学常见的七种物质,它们有如下转化关系(部分产物与反应条件略去):
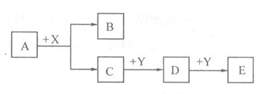
(1)若A为金属单质,B为氢气,X为盐酸,Y为易溶强碱溶液。则A物质的名称是?;D与Y反应的离子方程式为;?
(2)若A为固体非金属单质,B为水,X为强酸,Y为含钠元素的化合物。则A物质的名称可能是?;D与Y反应的离子方程式为可能为
?;
(3)若A、C为同主族元素组成的单质,通常状况下,A为气体,C为液体,Y为金属单质。则D溶液显?(填酸或碱)性,原因是
?(用离子方程式作答)
将NaOH溶液加入E的溶液中,可观察到的现象是?;
D→E的化学反应方程式为?。
参考答案:(1)铝;(1分) OH-+Al(OH)3=AlO2-↑+2H2O;(2分)(无↑扣1分)
(2)?碳或硫?;(1分)
OH-+HCO3-=CO32-+H2O或OH-+HSO3-=SO32-+H2O;(2分)
(3)?酸?;(1分)? Fe3++3H2O Fe(OH)3↓+3H+(2分)(无↓扣1分)
Fe(OH)3↓+3H+(2分)(无↓扣1分)
先出现白色沉淀然后沉淀迅速变成灰绿色,最终变成红褐色;(2分)
2FeBr3+ Fe=3FeBr2?。(2分)
本题解析:(1)根据图中的转化特点可知,C和强碱反应生成物D还能溶解在强碱中,常见的是铝的化合物的转化,再结合A是金属可知,A是铝和盐酸的÷生成氢气和氯化铝,所以D是氢氧化铝,E是偏铝酸钠。
(2)常见非金属单质能和酸反应生成水的,一般强氧化性酸和C或S反应,生成的CO2或SO2可与氢氧化钠反应生成正盐或酸式盐。
(3)常见的液体单质是溴,A能置换出溴,说明A是氯气。根据转化特点可判断,Y是变价的金属铁。铁离子在溶液中存在水解平衡,溶液显酸性。
本题难度:一般
5、填空题 (9分)如图每一方框中的字母代表一种反应物或生成物,产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,D是淡黄色固体单质。试填写下列空白:
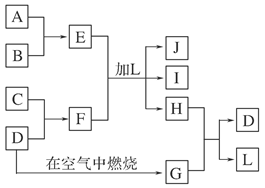
(1)L的化学式为:________,F的化学式为:________。
(2)J受热分解反应的化学方程式为:________________________________________
________________________________________________________________________。
(3)H与G之间反应的化学方程式为:________________________________________
________________________________________________________________________。
参考答案:(1)H2O? Na2S? (2)2Al(OH)3Al2O3+3H2O (3)2H2S+SO2===3S+2H2O
本题解析:D是淡黄色固体单质,应为硫;J是含金属元素的白色胶状沉淀,应为Al(OH)3,则A为Al;I为NaCl,则F应为Na2S,E为AlCl3,L为H2O。Na2S与AlCl3发生双水解反应生成NaCl、Al(OH)3和H2S。D(S)在空气中燃烧生成G(SO2),G与H(H2S)反应又生成D(S)和L(H2O)。
本题难度:一般