微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)质子交换膜燃料电池广受关注。
(1)质子交换膜燃料电池中作为燃料的H2通常来自水煤气。
已知:C(s)+O2(g) CO(g) ΔH1=-110.35kJ・mol-1
CO(g) ΔH1=-110.35kJ・mol-1
2H2O(l) 2H2(g)+O2(g) ΔH2=+571.6kJ・mol-1
2H2(g)+O2(g) ΔH2=+571.6kJ・mol-1
H2O(l) H2O(g) ΔH3=+44.0kJ・mol-1
H2O(g) ΔH3=+44.0kJ・mol-1
则C(s)+H2O(g) CO(g)+H2(g) ΔH4= 。
CO(g)+H2(g) ΔH4= 。
(2)燃料气(流速为1800mL・h-1;体积分数为50% H2,0.98% CO,1.64% O2,47.38% N2)中的CO会使电极催化剂中毒,使用CuO/CeO2催化剂可使CO优先氧化而脱除。
①160 ℃、CuO/CeO2作催化剂时,CO优先氧化反应的化学方程式为 。
②灼烧草酸铈[ Ce2(C2O4)3]制得CeO2的化学方程式为 。
③在CuO/CeO2催化剂中加入不同的酸(HIO3或H3PO4),测得燃料气中CO优先氧化的转化率随温度变化如图1所示。

加入 (填酸的化学式)的CuO/CeO2催化剂催化性能最好。催化剂为CuO/CeO2―HIO3,120℃时,反应1h后CO的体积为 mL。
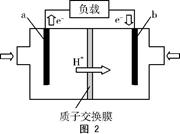
(3)图2为甲酸质子交换膜燃料电池的结构示意图。该装置中 (填“a”或“b”)为电池的负极,负极的电极反应式为 。
参考答案:(1) +131.45 kJ・mol-1
(2) ①2CO+O2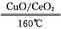 2CO2
2CO2
②Ce2(C2O4)3 2CeO2+4CO↑+2CO2↑
2CeO2+4CO↑+2CO2↑
③HIO3; 3.528
(3) a; HCOOH-2e- CO2↑+2H+
CO2↑+2H+
本题解析:(1)C(s)+O2(g) CO(g) ΔH1=-110.35kJ・mol-1 ①
CO(g) ΔH1=-110.35kJ・mol-1 ①
2H2O(l) 2H2(g)+O2(g) ΔH2=+571.6kJ・mol-1 ②
2H2(g)+O2(g) ΔH2=+571.6kJ・mol-1 ②
H2O(l) H2O(g) ΔH3=+44.0kJ・mol-1 ③
H2O(g) ΔH3=+44.0kJ・mol-1 ③
ΔH=ΔH1+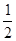 ΔH2-ΔH3="+131.45" kJ・mol-1
ΔH2-ΔH3="+131.45" kJ・mol-1
(2)①160 ℃、CuO/CeO2作催化剂时,CO优先氧化生成CO2,反应的化学方程式为2CO+O2 2CO2
2CO2
②灼烧草酸铈[ Ce2(C2O4)3]制得CeO2,CO2和CO,化学方程式为Ce2(C2O4)3 2CeO2+4CO↑+2CO2↑
2CeO2+4CO↑+2CO2↑
③在CuO/CeO2催化剂中加入不同的酸(HIO3或H3PO4),测得燃料气中CO优先氧化的转化率随温度变化如图1所示。从图中可知,加入HIO3反应速度快,所需温度低,CO的转化率大;120℃时,CO的转化率为80%
反应1h后CO的体积为×1800×0.98%×80%=3.528mL;
(3)由图2可知,电子从a端进入,从b端流出,说明a为电池的负极;且电极反应为HCOOH-2e- CO2↑+2H+。
CO2↑+2H+。
考点:反应热的计算,化学反应方程式的书写,化学反应方程式的计算,原电池的相关知识
本题难度:困难
2、选择题 已知下列热化学方程式
⑴C(s)+1/2O2(g)=CO(g) △H1="-110." 5kJ/mol
⑵2H2(g)+O2(g)=2H2O(g) △H2=-483.6 kJ・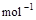
由此可知C(s)+ H2O(g) ="=" CO(g) + H2(g) ΔH3。则 ΔH3等于
A.+131.3kJ・mol-1
B.-131.3kJ・mol-1
C.+373.1kJ・mol-1
D.-373.1kJ・mol-1