��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����Ѵ�ƽ��״̬�ķ�Ӧ��X(g)��3Y(g)? 2Z(g)������ӦΪ���ȷ�Ӧ����Ϊ��ʹƽ��������Z�ķ����ƶ���Ӧѡ�����е����������ǣ�?��
2Z(g)������ӦΪ���ȷ�Ӧ����Ϊ��ʹƽ��������Z�ķ����ƶ���Ӧѡ�����е����������ǣ�?��
�ٸ���?�ڵ���?�۸�ѹ?�ܵ�ѹ?�ݼӴ���?��ȥZ
A���٢ܢ�
B���ڢۢ�
C���٢ۢ�
D���ڢۢ�
�ο��𰸣�D
�������������Z�ķ����������Ӧ��������������ԭ�����ɲ�ȡ��ѹ�����£�����ZŨ�ȵķ�����ʹ��������Ӧ�����ƶ�����ӦѡD��
�����Ѷȣ���
2��ѡ���� ��һ���¶��£����ڿ��淴ӦC(s)+H2O(g) 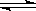 CO(g)+H2(g)����ƽ�ⳣ������ʽ��ȷ���ǣ�?��
CO(g)+H2(g)����ƽ�ⳣ������ʽ��ȷ���ǣ�?��
A��K=[c(C)��c(H2O)]/ [c(CO)��c(H2)]? B��K= [c(CO)��c(H2)]/ [c(C)��c(H2O)]
C��K=[c(H2O)]/ [c(CO)��c(H2)]?D��K=[c(CO)��c(H2)/ [c(H2O)]]
�ο��𰸣�D
������������ݷ�Ӧ�ķ���ʽ��֪���÷�Ӧ��ƽ�ⳣ��K��[c(CO)��c(H2)/ [c(H2O)]]����ѡD��
��������ѧ��������һ�������µĿ��淴Ӧ�У������淴Ӧ��Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ���ݴ˿����жϷ�Ӧ��ƽ�ⳣ������ʽ��
�����Ѷȣ�һ��
3��ѡ���� �ں���ʱ��һ�̶��ݻ��������ڷ������·�Ӧ��2NO2��g��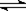 N2O4(g) �ﵽƽ��ʱ������������ͨ��һ������NO2��g�������´ﵽƽ������һ��ƽ��ʱ��ȣ�NO2�����������?��
N2O4(g) �ﵽƽ��ʱ������������ͨ��һ������NO2��g�������´ﵽƽ������һ��ƽ��ʱ��ȣ�NO2�����������?��
A������
B������
C����С
D�����ж�
�ο��𰸣�C
������������ڷ�Ӧ������������һ�֣������ڼ���NO2ʱ�൱��������ѹǿ��ƽ��������Ӧ�����ƶ���NO2������������ͣ���ѡC��
�������������е��Ѷȵ����⣬Ҳ�Ǹ߿��еij������͡����������ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������������ѧ���������������ʹ���˼ά���������ѧ�������Ӧ��������Ӧ��������
�����Ѷȣ���
4��ѡ���� ij�¶��£���һ����㶨���ܱ������ڷ�����ӦA(s)��2B(g) C(g)��D(g)�����������������ٱ仯ʱ���ܹ�������Ӧ�Ѵ�ƽ�����
C(g)��D(g)�����������������ٱ仯ʱ���ܹ�������Ӧ�Ѵ�ƽ�����
A�������ѹǿ
B������������ʵ���
C�������ƽ���ܶ�
D�������ƽ����Է�������
�ο��𰸣�CD
�����������
�����Ѷȣ���
5�������� ��3 mol A��2.5 mol B�����2L���ܱ������У�������Ӧ�Ļ�ѧ����ʽΪ��3A(��) + B(��)  ?xC(��) + 2D(��)��5 min��Ӧ�ﵽƽ��״̬�������ڵ�ѹǿ��С����֪D��ƽ����Ӧ�ٶ�Ϊ 0.1 mol/(L�qmin), ��д���пհף�
?xC(��) + 2D(��)��5 min��Ӧ�ﵽƽ��״̬�������ڵ�ѹǿ��С����֪D��ƽ����Ӧ�ٶ�Ϊ 0.1 mol/(L�qmin), ��д���пհף�
(1) x =______
(2) ƽ��ʱC��Ũ��Ϊ ________________
(3) ƽ��ʱB��ת����Ϊ _____________
(4) ƽ��ʱ�������ڵ�ѹǿ��ԭ������ѹǿ�ı�ֵΪ ___________
�ο��𰸣�(1)X="1" ?(2) 0.25mol��L-1?��3��20%?��4��10��11
��������������ڵ�ѹǿ��С��˵��3+1��x+2������Ϊx������������x��1��D��ƽ����Ӧ�ٶ�Ϊ 0.1 mol/(L�qmin),��������D��0.1 mol/(L�qmin),��2L��5min��1.0mol
3A(��) + B(��)  ?C(��) + 2D(��)
?C(��) + 2D(��)
��ʼ����mol��? 3? 2.5? 0? 0
ת������mol��? 1.5? 0.5? 0.5? 1.0
ƽ������mol��? 1.5? 2.0? 0.5? 1.0
����ƽ��ʱC��Ũ��Ϊ0.5mol��2L��0.25mol/L
ƽ��ʱB��ת����Ϊ0.5��2.5��100����20��
��Ϊѹǿ֮�������ʵ�����֮��
����ƽ��ʱ�������ڵ�ѹǿ��ԭ������ѹǿ�ı�ֵΪ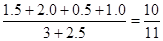
�����Ѷȣ�һ��