微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一定温度下,将等物质的量A和B充入一密闭容器中,发生如下反应:A(g)+2B(g)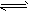 2C(g),反应达到平衡时,若A和B的物质的量之和与C相等,则此时A的转化率为
2C(g),反应达到平衡时,若A和B的物质的量之和与C相等,则此时A的转化率为
[? ]
A.50%
B.60%
C.40%
D.70%
参考答案:C
本题解析:
本题难度:一般
2、填空题 (4分)已知2NH3(g)  ?N2(g) +3 H2(g)?;在某温度下,在2 L密闭容器中加入一定量的NH3,反应到10分钟时各组分的浓度不再改变,此时测得各组分的浓度如下:
?N2(g) +3 H2(g)?;在某温度下,在2 L密闭容器中加入一定量的NH3,反应到10分钟时各组分的浓度不再改变,此时测得各组分的浓度如下:
物质
| NH3
| N2
| H2
|
物质的量(mol)
| 0. 1
| 0.2
| 0.6
|
该时间内平均反应速率v(N2) =?
达到平衡状态后,下列说法正确的是:?
a.通过改变反应 条件可使现有平衡移动
条件可使现有平衡移动
b.NH3的分解速率和合成速率相等
c.NH3不再分解了
d.通过改变反应条件可使NH3全部分解成N2和H2
参考答案:0.01moll-1min-1??ab
本题解析:略
本题难度:一般
3、选择题 100℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g)  ?2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
?2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①N2O4的消耗速率与NO2的生成速率之比为1:2 ;②NO2生成速率与NO2消耗速率相等;
③烧瓶内气体的压强不再变化;?④烧瓶内气体的质量不再变化;
⑤NO2的物质的量浓度不再改变;?⑥烧瓶内气体的颜色不再加深;
⑦烧瓶内气体的平均相对分子质量不再变化?⑧烧瓶内气体的密度不再变化。
A.②③⑥⑦
B.①④⑧
C.只有①④
D.只有⑦⑧
参考答案:A
本题解析:①N2O4的消耗速率与NO2的消耗速率之比为1:2 ①错误。BC错误。②NO2生成速率与NO2消耗速率相等,②正确。④烧瓶内气体的质量不再变化,质量一直保持不变,不能作为判断平衡状态的依据,④错误。物质的量的总量和压强可以作为判断平衡状态的依据。③⑥⑦正确。⑧烧瓶内气体的密度不再变化,m、v不变密度也一直不变,⑧错误。BCD错误。
本题难度:一般
4、填空题 (每小题3分,共9分)恒温恒压下,在一个容积可变的密闭容器中发生如下反应: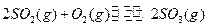
(1)若开始时通入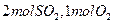 ,达平衡时生成
,达平衡时生成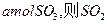 的转化率为?。
的转化率为?。
(2)若开始时通入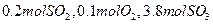 ,达平衡时SO2的物质的量为?mol。
,达平衡时SO2的物质的量为?mol。
(3)若在(2)的平衡混合物中再通入bmol SO3,则达到平衡时SO3的体积分数是?。
参考答案:(1)50 a%?(2)4-2a?(3)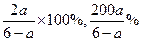
本题解析:略
本题难度:简单
5、计算题 在557℃时,密闭容器中进行下列反应CO+H2O CO2+H2。若(1)(2),达到平衡时,测得CO2的浓度为1.2mol/L。求CO及H2O的转化率。
CO2+H2。若(1)(2),达到平衡时,测得CO2的浓度为1.2mol/L。求CO及H2O的转化率。
参考答案:

本题解析:在掌握起始浓度、转化率、平衡浓度之间的关系和正确理解转化率概念的基础上,抓住转化浓度,利用常规解题方法。
CO? +? H2O(气) ?CO2+ H2
?CO2+ H2
起始浓度(mol・L-1)? 2? 3? 0? 0
转化浓度(mol・L-1)? 1.2? 1.2?1.2? 1.2
平衡浓度(mol・L-1)? 0.8? 1.8? 1.2? 1.2
本题难度:简单