��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �ߴ��������������Ƹ�ѹ�ƵƵ��մɹܣ�ʵ������ȡ�ߴ����������������£�
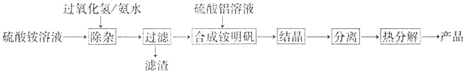
��1�������ӡ������Ǽ������������ð�ˮ������Һ��pHԼΪ8.0���Գ�ȥ�������Һ�е�����Fe2+������Fe2+�Ƿ������ʵ�������______��
��2��������������Һʱ�����������ữ���ữ��Ŀ����______��
��3����������ͼ����ᾧ���ⲽ�����У�ĸҺ��______?�õ�����������ᾧˮ����
��4����������ͼ������롱�������Ӧ��������______?������ĸ���ţ�
A������B����ҺC������D��ϴ�Ӿ��壮
2��ѡ���� ��ͼ����ȡ��ϴ�Ӳ������������������װ��ʾ��ͼ,���ø�װ�ý����±�����ʵ�飬�ܴﵽʵ��Ŀ�ĵ��� ��?��

 ���� ����
ʵ��
| a��Һ�壩
| b(����)
| c(Һ��)
|
A
| ϡ����
| �
| ŨH2SO4
|
B
| ϡ����
| ʯ��ʯ
| ŨH2SO4
|
C
| Ũ����
| CuƬ
| NaOH��Һ
|
D
| ϡHNO3
| CuƬ
| H2O
|
?
3��ʵ���� ��1��С���������о��¶ȶԷ�Ӧ���ʵ�Ӱ�족ʵ��ʱ����ȡ����ֻ�Թܣ�������4mL 0��01mol/L��KMnO4������Һ��2mL 0��1mol/L? H2C2O4���Ҷ��ᣩ��Һ����A�Թ�������ˮ�У�B�Թ�������ˮ�У���¼��Һ��ɫ�����ʱ�䡣
����Ҫ����?���ữKMnO4��Һ����ɫ����ʱ��tA?��tB�����������=����������
��д���÷�Ӧ�����ӷ���ʽ��?����
��2��ʵ������ƿ������ɳ���Ҷ�����Ʒ��С�����������Ӧ��ԭ�����ⶨ�京�����������Ϊ��
������250mL��Һ��ȷ����5��0g�Ҷ�����Ʒ�����250mL��Һ��
�ڵζ���ȷ��ȡ25��00mL������Һ����ƿ�У����������ữ����0��1000mol��L��1KMnO4��Һװ��
��?�������ʽ����ʽ�����ζ��ܣ����еζ���������ʵ���з��֣��յ�������KMnO4��Һʱ����ҺѸ�ٱ���Ϻ�ɫ������ƿҡ��һ��ʱ����Ϻ�ɫ������ʧ���ټ����μ�ʱ���Ϻ�ɫ�ͺܿ���ɫ�ˡ������ԭ����?������?��֤���ﵽ�ζ��յ㣮
�ۼ��㣺���ظ���������2�Σ���¼ʵ���������£�
���
| �ζ�ǰ������mL��
| ��������mL��
|
1
| 0��00
| 20��10
|
2
| 1��00
| 20��90
|
3
| 0��00
| 21��10
|
������KMnO4��Һ��ƽ�����Ϊ��?��mL����֪H2C2O4����Է�������Ϊ90�������Ʒ�Ĵ���Ϊ��?����
�������������в����ᵼ�²ⶨ���ƫ�ߵ�����?����
A��δ�ñ�Ũ�ȵ�����KMnO4��Һ��ϴ�ζ���
B���ζ�ǰ��ƿ������ˮ
C���ζ�ǰ�ζ��ܼ��첿�������ݣ��ζ���������ʧ
D����С�Ľ���������KMnO4��Һ������ƿ��
E���۲����ʱ���ζ�ǰ���ӣ��ζ����ӣ�
4������� ij��ѧ��ȤС���ú���������ͭ�ĺϽ���ȡ�������Ȼ�����Һ���̷����壨FeSO4?7H2O���͵������壨CuSO4?5H2O������̽����ҵ���ϵ������ã���ʵ�鷽����ͼ��

�Իش��������⣺
��1��д����ҺAת��Ϊ����D�����ӷ���ʽ______��
��2������ҺA��AlCl3��Һ��;����I��II����������Ϊ��������;��______���I����II������������______��
��3������ҺE�еõ��̷������ʵ������ǣ�������E�е����ʱ�������һ���أ���______��
��4��H2O2��һ����ɫ��������Ӧ��ʮ�ֹ㷺��������F�м���ϡ�����H2O2���Ʊ�����������һ����ɫ���գ��÷�Ӧ���ܵĻ�ѧ����ʽΪ______��
��5����ͬѧ����ɽ�����������ܽ�Ͻ���ռ�������ᣬ������Ʒ�����Ҳ���Ƶ��������ʣ�����Ϊ���ߵķ����Ƿ������______��������______��
5������� ��ѧѧϰС���ijþ���Ͻ����������ʵ���о���������벢��ɶ��й�����Ľ��
ʵ��ҩƷ��9.0gþ���Ͻ�100mLamol/Lϡ���ᣬ260mL5mol/L����������Һ��
ʵ�鲽��
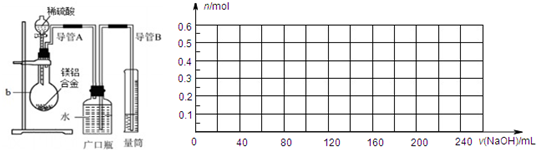
�ٽ�9.0gþ���Ͻ���100mLamol/Lϡ������ͼ��ʾװ���г�ַ�Ӧ����Ӧ��ϣ����ռ����ɵ�ȫ�����壮
����b�ڵĻ��Һ����μ���260mL5mol/L����������Һ����ֻ�ϣ�������������Һ�μ���200mLʱ���ɵij��������
��������
��1������b��������______��
��2������ʵ��Ŀ�Ŀ�֪��9.0gþ���Ͻ���100amol/Lϡ���ᷴӦʱ��Ӧ�ù����㣩����������______���þ���Ͻ𡱻�ϡ���ᡱ�����Ա�֤��һ�������ܹ���ȫ��Ӧ��ʣ�࣮
��3��ʵ�鲽����У���b�ڻ��Һ����μ�����������Һ�����ɵij��������ʱ����ʱ������Һ�е�������______��
��4��ʵ�鲽��ٽ�����ȡ��Ͳ�����ֵ�����ʱ����Ҫע���������Ҫ�����ǣ�һ��Ҫ______������Ҫ������ͲҺ������ƿҺ����ƽ������Ҫʹ��������Ͳ�ڵİ�Һ����ƽ��
��5������״���£���ʵ�鲽��ٵõ����������Ϊ10.08L����Ͻ���þ����������Ϊ______��
��6���ڡ�amol/Lϡ���ᡱ��a��ֵΪ______��
��7������ͼ�л���ʵ�鲽��������ɳ��������ʵ�����n�����������������Һ�����[v��NaOH��]�ı仯���ߣ�