��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij��Һ����������ˮ�����NaOH��Һ���г������������������ۻ�ͭ����Һ���������ӣ�����Һ�п��ܺ����������ӵ�
A.Al3+
B.Fe2+
C.Fe3+
D.Mg2+
�ο��𰸣�C
���������
�����Ѷȣ���
2��ѡ���� 11.2L���顢���顢HCHO��g��Դ��www.91exam.org����ɵĻ�����壬��ȫȼ�պ�����15.68L CO2������������ڱ�״���²ⶨ������������м���������������Ϊ
A.20%
B.60%
C.70%
D.80%
�ο��𰸣�A
�������������������n=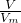 ���������弰������̼�����ʵ���������Cԭ���غ�����������ƽ��Cԭ����Ŀ���������ȩ��̼ԭ����Ŀ����1�����Կ���1����֣�������ֻ�����2��ֻ�������ƽ��Cԭ����Ŀ��������������������������������ȩ���������֮�ͣ��ݴ˽��
���������弰������̼�����ʵ���������Cԭ���غ�����������ƽ��Cԭ����Ŀ���������ȩ��̼ԭ����Ŀ����1�����Կ���1����֣�������ֻ�����2��ֻ�������ƽ��Cԭ����Ŀ��������������������������������ȩ���������֮�ͣ��ݴ˽��
���11.2L���顢���顢HCHO��g����ɵĻ����������ʵ���Ϊ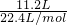 =0.5mol��
=0.5mol��
15.68LCO2�����ʵ���Ϊ =0.7mol��
=0.7mol��
�ʻ��������ƽ��Cԭ����ĿΪ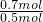 =1.4��
=1.4��
�������ȩ��̼ԭ����Ŀ����1�����Կ���1����֣������������2��ֻ���
������������������ʵ���Ϊxmol���������ȩ���ܵ����ʵ���Ϊymol����
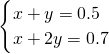
��ã�x=0.3��y=0.2��
��������������Ϊ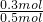 ��100%=60%��
��100%=60%��
�������ȩ���������֮��Ϊ1-60%=40%��
��ѡA��
����������������йؼ��㣬�Ѷ��еȣ������ǽ�������ֻ�����2��ֻ���ע��ƽ���������ã�
�����Ѷȣ�����
3��ѡ���� ��amL?0.1mol/L��������Һ��bmL?0.5mol/L����������Һ��ϣ��õ�cmol������������������֪a��b��c����������ֵ������һ��ֵ�������ֵ��ֹһ������ǣ���ѡ���У���λ������ȥ��
A.a=100 b=90 c=
B.b=100 c=0.015 a=
C.b=90 c=0.015 a=
D.a=75 c=0.015 b=
�ο��𰸣�C
�������������������Al3++3OH-�TAl��OH��3����Al��OH��3+OH-�TAlO2-+2H2O�����ɳ��������ʵ���һ������c������������ʱ���������ֿ������������
���A��a=100 b=90ʱ�����������ӵ����ʵ����������ӵ����ʵ���֮��Ϊ4.5��2��ֻ����Al3++3OH-�TAl��OH��3�����Ҽ�㣬��cֻ��һ������A��ѡ��
B��b=100 c=0.015ʱ���������������������ӵ����ʵ���С�ڼ�����ʵ���������������Ӧ�����������Ϊ0.015mol����������B��ѡ��
C��b=90 c=0.015ʱ����cһ�����Ҳ�����������ʱ����������ֿ��ܣ��������ֵ��ֹһ���⣬
����ֻ����Al3++3OH-�TAl��OH��3������㣬
b=90��c=0.015ʱ����������������������ʵ�����Ϊ3��1��
���ɷ�Ӧ����ʽ�ɼ���a=75mL���������ӿ��ܹ�������a��75mL��
�������������ӵ����ʵ����������ӵ����ʵ�������3��1����С��4��1��
����Al3++3OH-�TAl��OH��3��ʱ�����������Al��OH��3+OH-�TAlO2-+2H2Oʱ��㣬
�������ӵ����ʵ���Ϊx���������ĵļ��֪��3x+��x-0.015��=0.09��0.5��
���x=0.015mol��a=75mL����Cѡ��
D��a=75 c=0.015ʱ�������ӵ����ʵ��������������������ʵ�������ֻ����Al3++3OH-�TAl��OH��3��������ǡ����ȫ��Ӧ����bֻ��һ���⣬��D��ѡ��
��ѡC��
���������⿼�����������ķ�Ӧ����ȷ�����������ܽ���ǿ����Һ�У����������Ĺ�ϵ���жϷ����Ļ�ѧ��Ӧ�ǽ��Ĺؼ���
�����Ѷȣ�һ��
4��ѡ���� ������������ȷ����
A.�п��Ľ���Na��¶�ڿ����У������ı����䰵�������ķ�ӦΪ2Na+O2 �TNa2O2
B.4.6?g?Na��O2��ȫ��Ӧ������7?g����ʱʧȥ���ӵ����ʵ���Ϊ0.2?mol
C.Na�Ż�ʱ������ˮ��𣬿���ϸɳ�������
D.������NaͶ�뵽CuS04��Һ�У����г���������������ų�
�ο��𰸣�A
���������������A������ͨ�������·�Ӧ���������ƣ�
B�����������������ʵ������������������Ӧ��������ϵ����õ���
C���ƺ�ˮ��������̼��Ӧ��
D���ƺ�ˮ��Ӧ�����������ƺ��������������ƺ�����ͭ��Ӧ����������ͭ������
���A������ͨ�������·�Ӧ���������ƣ���ȼ�������ɹ������ƣ���A����
B��4.6 g Na��O2��ȫ��Ӧ������7 g����ʱ����Ӧ������Ϊ2.4g�����ݻ�ѧ����ʽ��������ж���ȫ����Ӧ�ǵ���0.2mol����B��ȷ��
C���ƺ�ˮ��������̼��Ӧ��Na�Ż�ʱ������ˮ��𣬿���ϸɳ���������ֹ�����������������̼ˮ�ȽӴ���Ӧ����C��ȷ��
D���ƺ�ˮ��Ӧ�����������ƺ��������������ƺ�����ͭ��Ӧ����������ͭ������������NaͶ�뵽CuS04��Һ�У����г���������������ų�����D��ȷ��
��ѡA��
���������⿼���������ʵķ���Ӧ�ã���Ӧ�����Ͳ�����жϣ����������ʵķ���Ӧ���ǽ���ؼ�����Ŀ�ϼ�
�����Ѷȣ�һ��
5��ѡ���� Ϊ�˷�ֹ���������ж��������ý���ij������ˮ��Һ��ë����ס���ӣ������������˲���
A.��������
B.����
C.NH3
D.����
�ο��𰸣�B
���������
�����Ѷȣ���