微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g) ==CH4(g)+HC
 CH(g)+H2(g)?△H1="156.6" kJ/mol
CH(g)+H2(g)?△H1="156.6" kJ/mol
CH3CH
 CH2(g)=CH4(g)+HC
CH2(g)=CH4(g)+HC
 ?CH(g )?△H2="32.4" kJ/mol
?CH(g )?△H2="32.4" kJ/mol
则相同条件下,反应C3H8(g) ==CH3CH ?CH2(g)+H2(g)的△H=?kJ/mol。
?CH2(g)+H2(g)的△H=?kJ/mol。
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池总反应方程式为?;放电时CO32-移向电池的?(填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3-+H+的平衡常数K1=?。(已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=?。(已知10-5.60=2.5×10-6)
(4)常温下,0.1 mol/LNaHCO3溶液的pH大于8,则溶液中c(H2CO3)?c(CO32-)(填“>”、“=”或“<”),原因是?
?(用离子方程式和必要的文字说明)。
参考答案:(1)124.2 (2分)
(2)C3H8+5O2=3CO2+4H2O (2分)?负(1分)
(3)4.2×10-7 mol/L(2分)
(4)> (1分) HCO3-+H2O CO32-+H3O+(或HCO3-
CO32-+H3O+(或HCO3- CO32-+H+)、
CO32-+H+)、
HCO3-+H2O H2CO3+OH-,HCO3-的水解程度大于电离程度 (3分)
H2CO3+OH-,HCO3-的水解程度大于电离程度 (3分)
本题解析:(1)根据盖斯定律可得:?H=?H1-?H2="156.6" kJ?mol?1-32.4 kJ?mol?1=124.2kJ?mol?1。
(2)燃料电池的总反应方程式可根据燃烧反应的方程式书写:C3H8+5O2=3CO2+4H2O;原电池放电时阴离子向负极移动。
(3)根据pH可得c(H+)=10-5.6mol/L? H2CO3 = HCO3? + H+
平衡浓度(mol?L?1) 1.5×10-5?10-5.6?10-5.6
K=(10-5.6 mol?L?1×10-5.6 mol?L?1)÷1.5×10-5 mol?L?1=4.2×10-7 mol?L?1。
(4)NaHCO3溶液存在两个平衡,HCO3?的电离:HCO3- CO32-+H+和HCO3?的水解:HCO3-+H2O
CO32-+H+和HCO3?的水解:HCO3-+H2O H2CO3+OH-,因为NaHCO3溶液的pH大于8,所以HCO3?的水解程度大于电离程度,c(H2CO3)>c(CO32-)。
H2CO3+OH-,因为NaHCO3溶液的pH大于8,所以HCO3?的水解程度大于电离程度,c(H2CO3)>c(CO32-)。
本题难度:一般
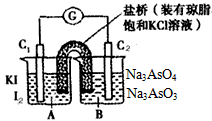
2、选择题 已知反应AsO43- +2I- +2H+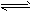 AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2 均为石墨电极),分别进行下述操作:
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2 均为石墨电极),分别进行下述操作:
Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液结果发现电流计指针均发生偏转。
据此,下列判断正确的是
[? ]
A.操作I过程中,C1为正极
B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液
C.操作I过程中,C2棒上发生的反应为:AsO43-+2H+ +2e-=AsO33-+H2O
D.操作Ⅱ过程中,C1棒上发生的反应为:2I- =I2 +2e-
参考答案:C
本题解析:
本题难度:一般
3、填空题 下图是铜锌原电池装置。其电池的总反应是:Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s)。若该电池中两电极的总质量为303g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为298g。
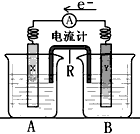
请回答以下问题
(1)R的作用是使两个烧杯中的溶液连成通路,R名称是_________。R中的阳离子移向___________(填A或B)中的溶液。
(2)电极Y的材料是_______。
(3)X为原电池的__________极,其电极反应式是_____________________ 。
(4)产生铜的质量为___________;转移的电子的物质的量为__________。
(5)高铁酸盐在能源环保领域有广泛用途。我国学者提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如图所示。
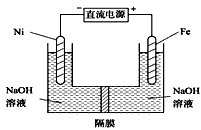
① Fe电极作_________极 (填“阴”或“阳”); ②Ni电极的电极反应式为:___________________。
参考答案:(1)盐桥;A
(2)Zn
(3)正;Cu2++2e-==Cu
(4)128克;4mol
(5)①阳;②2H++2e-==H2(或2H2O+2e-==H2+2OH-)
本题解析:
本题难度:一般
4、选择题 利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,下图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图。上述电池工作时,有关说法正确的是
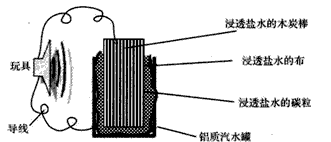
[? ]
A.铝罐将逐渐被腐蚀
B.碳粒和炭棒上发生的反应为:O2+4e-==2O2-
C.炭棒应与玩具电机的负极相连
D.该电池工作一段时间后炭棒和炭粒的质量会减轻
参考答案:A
本题解析:
本题难度:一般
5、判断题 (6分)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
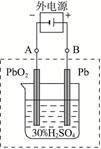
铅蓄电池示意图
Pb+PbO2+4H++2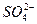
 2PbSO4+2H2O
2PbSO4+2H2O
请完成下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是
____________________________________________________;电解液中H2SO4的浓度将变_________________;当外电路通过1 mol电子时,理论上负极板的质量增加
_________________g。
(2)在完全放电耗尽PbO2和Pb时,若按右图连接,电解一段时间后,则在A电极上生成
_____________________、B电极上生成_____________________,此时铅蓄电池的正负极的极性将__________________________________。
参考答案:(1)PbO2+2e-+4H++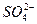 ====PbSO4+2H2O?小? 48
====PbSO4+2H2O?小? 48
(2)Pb? PbO2?对换
本题解析:在反应过程中,由于消耗H+,故反应液的c(H+)将降低。完全放电后再按图连接,则形成电解池,A极为阴极,B极为阳极,由于阳极生成PbO2,则去掉外电源后,铅蓄电池的正负极将与原来相反。
本题难度:简单