��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ͼ��ʾװ���У��ס��������ձ��ֱ�����ʢ��200mL����ʳ��ˮ��������AgNO3��Һ��a��b��c��d�ĸ��缫��Ϊʯī�缫����ͨ��Դ������һ��ʱ��������d�缫����������2.16g���ݴ˻ش����⣺
��1����Դ��N��Ϊ______����
��2���缫b�Ϸ����ĵ缫��ӦΪ______��
��3���缫c�����ɵ������ڱ�״̬�µ������______��
��4������Һ��pHΪ______������Һ�����Ϊ200mL����
��5�����ڱ��ձ���ʵ�����ı������һ��п����������ҺΪ______��e�缫�IJ����ǣ�______��f�缫�ĵ缫��ӦʽΪ______��

�ο��𰸣���1���������d�缫����������2.16g����d�缫����Ag++e-=Ag������d�缫Ϊ������NΪ��Դ�ĸ������ʴ�Ϊ������
��2�����ʳ��ˮ��bΪ����������2H++2e?=H2�����ʴ�Ϊ��2H++2e?=H2����
��3��d�缫����Ag++e-=Ag��c������4OH--4e-=2H2O+O2�����ɵ����غ��֪4Ag��O2��������������Ϊ2.16g108g/mol��14��22.4L/mol=0.112L���ʴ�Ϊ��0.112L��
��4���ɵ����غ��֪2NaOH��2e-��2Ag��n��NaOH��=n��Ag��=0.02mol����c��NaOH��=0.02mol0.2L=0.1mol/L������pH=13���ʴ�Ϊ��13��
��5�����ձ���ʵ�����ı������һ��п����������ҺΪZnCl2��eΪZn��f�缫Ϊ��������缫��ӦʽΪZn2++2e-=Zn���ʴ�Ϊ��ZnCl2��Zn��Zn2++2e-=Zn��
���������
�����Ѷȣ�һ��
2������� ����װ��ܷ����ԭ��أ����ж�����������
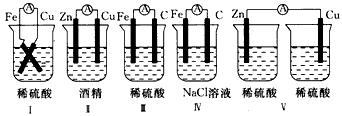
______________________________________
�ο��𰸣�I�ܣ�FeΪ������CuΪ����
����
���ܣ�Fe Ϊ������CΪ����
IV�ܣ�FeΪ������CΪ����
V����
���������
�����Ѷȣ�һ��
3������� �ס������ص缫������ͼ��ʾ���밴Ҫ��ش��������⣺
��1���������о�ΪCu��NO3��2��Һ����Ӧһ��ʱ���
���к�ɫ�����������Ǽ׳��е�______��������̼�����ҳ��е�______��������������
���ҳ��������Ϸ����ĵ缫��Ӧ����ʽ��______��
��2���������о�Ϊ����NaCl��Һ��
��д���ҳ����ܷ�Ӧ�Ļ�ѧ����ʽ______��
�ڼ׳���̼���ϵ缫��Ӧ����ʽ��______���ҳ�̼���ϵ缫��Ӧ����______����������Ӧ����ԭ��Ӧ����
�ο��𰸣���û����ӵ�Դ��������ԭ��أ�����������̼��������������ӵ�Դ�������ǵ��أ����ݵ��ӵ������жϣ�����������̼��������
��1���ټ׳��е�?����������ԭ��Ӧ���н���������������̼����
�ҳ��е�����������ԭ��Ӧ���н���������������������
�ʴ�Ϊ��̼������
���ҳ��������Ϸ���������Ӧ�����������ӵķŵ�����������������ӵķŵ�����������������������ʧ��������������ˮ���ʴ�Ϊ��4OH--4e-�TO2��+2H2O
��2�����Ȼ�����Һ�д��ڵ������ǣ������ӡ����������ӡ������ӡ������ӣ������ӵķŵ������������������ӣ������ӵķŵ��������������ӣ����Ը÷�Ӧ�����������������������������ƣ�
�ʴ�Ϊ��2H2O+2NaCl??���?.?2NaOH+H2��+Cl2��
����������Һ�У�����һ��������������ʱ�ᷢ��������ʴ����������ʧ���ӣ�������������ˮ�õ����������������ӣ��ҳ���̼���������������Ϸ���������Ӧ��
�ʴ�Ϊ��O2+4e-+2H2O�T4OH-��������Ӧ��
���������
�����Ѷȣ�һ��
4������� ��10�֣���ͼ��һ����ѧ���̵�ʾ��ͼ��
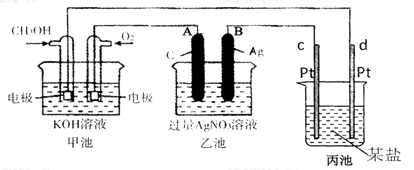
��1��ͼ���ҳ��� װ�á�
��2��c��Pt���缫�������� ��
��3��д��ͨ��CH3OH�ĵ缫�ĵ缫��Ӧʽ�� ��
��4���ҳ��з�Ӧ�����ӷ���ʽΪ ��
��5�����ҳ���B��Ag��������������5��40gʱ���׳�������������O2 mL����״���£�����ʱ����ij�缫����1.6gij����������е�ij����Һ������ ������ţ�
A��MgSO4
B��CuSO4
C��NaCl
D��CuCl2