微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 金属冶炼与处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是________。
a. Fe2O3? b.NaCl? c.Cu2S? d.Al2O3
(2)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,该反应的还原剂是________。当1 mol O2发生反应时,还原剂所失电子的物质的量为________mol。向CuSO4溶液中加入镁条时有气体生成,该气体是________。
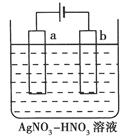
(3)右图为电解精炼银的示意图,________(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体产生,则生成该气体的电极反应式为________。
(4)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用是________。
参考答案:(1)b、d (2)Cu2S 4 H2 (3)a NO3―+2H++e-=NO2+H2O (4)做电解质溶液(或导电)
本题解析:结合氧化还原反应规律及原电池、电解池知识分析相关问题。
(1)电解法常用于冶炼非常活泼的金属,如K、Ca、Na、Mg、Al等,显然b、d项正确。工业上以Fe2O3、Cu2S为原料,采用热还原法冶炼金属Fe、Cu。
(2)该反应中,Cu元素由+1价变为+2价,S元素由-2价变为+6价,O元素由0价变为-2价,则O2为氧化剂,Cu2S为还原剂。1 mol O2发生反应时,得到4 mol电子,则还原剂Cu2S失去4 mol电子。CuSO4溶液中由于Cu2+发生水解而显酸性,加入镁条时,Mg与H+反应放出H2。
(3)电解精炼银时,用含杂质的粗银作阳极,用纯银作阴极,含Ag+的电解质溶液做电解液。图中b极与电源的负极相连,则b极为阴极,NO3―在阴极放电生成红棕色的NO2,电极反应式为NO3―+2H++e-=NO2+H2O。
(4)银器浸于铝质容器里的食盐水中并与铝接触,形成原电池,Al作负极被氧化成Al3+,银器表面的Ag2S作正极,被还原为金属Ag。食盐水为电解质溶液,起导电作用。
点拨:知识:金属的冶炼;氧化还原反应;电解精炼银;原电池原理的应用。能力:考查考生对教材基础知识的掌握及迁移应用能力、简单计算能力。试题难度:中等。
本题难度:一般
2、填空题 (4分)配平氧化还原反应方程式。
(1) ?NH3+ ?NO2― ?N2+ ?H2O
(2) 氧化产物与还原产物的质量比为 ?。
参考答案:(4分)(1)8 6 14 12?(2)4:3
本题解析:本题考查氧化还原反应方程式的配平
(1)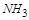 中
中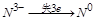 ,
,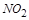 中
中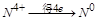 ,得失电子数的最小公倍数为
,得失电子数的最小公倍数为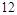 ,
,
在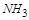 前配系数
前配系数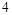 ,在
,在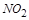 前配系数3,则
前配系数3,则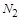 前配系数为
前配系数为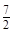 ,再配平
,再配平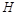 ,在
,在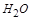 前配
前配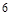 ;
;
即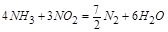
此方程式的两端同乘以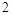 得
得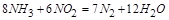
(2) 在反应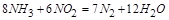 中,
中,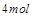
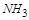 被氧化成
被氧化成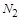 ,
,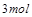
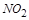 被还原
被还原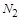 ,产物均为
,产物均为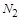 ,因而氧化产物与还原产物的质量比为
,因而氧化产物与还原产物的质量比为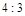 .
.
本题难度:简单
3、计算题 (10分)
用KMnO4氧化密度为1.19g/cm3,溶质的质量分数为36.5%的盐酸。反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥法标出上述反应中电子得失数目、化合价变化,并指出氧化剂和还原剂。
(2)求所用盐酸的物质的量浓度。
(3)15.8gKMnO4能使多少克HCl发生上述反应?产生的Cl2在标准状况下的体积为多少?
参考答案:(共10分)
(1)

氧化剂:KMnO4?还原剂:HCl?
(2)解:
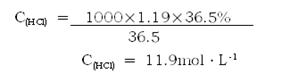
(3)设15.8gKMnO4能同xgHCl发生反应,生成标准状况下yLCl2。
2KMnO4?+ 16HCl =" 2KCl" + 2MnCl2 + 5Cl2↑ + 8H2O
2×158 g? 16×36.5 g?5×22.4 L
15.8 g? x g?y L ?

本题解析:
试题分析 :

氧化剂:KMnO4?(化合价降低 )?还原剂:HCl (化合价升高)
由c=1000ρw/M得:

设15.8gKMnO4能同xgHCl发生反应,生成标准状况下yLCl2。
2KMnO4?+ 16HCl =" 2KCl" + 2MnCl2 + 5Cl2↑ + 8H2O
2×158 g? 16×36.5 g?5×22.4 L
15.8 g? x g?y L ?

点评: 一、氧化还原反应的特点:氧化剂得电子,化合价降低,具有较强氧化性;还原剂失电子,化合价升高,具有较强还原性;
二、双线桥的表示基本步骤:
1.标变价
明确标出所有发生氧化还原反应的元素的化合价,不变价的元素不标化合价。
2.连双线
将标化合价的同一元素用直线加箭头从反应物指向生成物(注意:箭头的起止一律对准各元素)
3.标得失
①标电子转移或偏离数
明确标出得失电子数,格式为“得/失 发生氧化还原反应原子个数×单位原子得失电子数”
②标化合价变化
一律标出化合价的变化,只有“化合价升高”“化合价降低”这两种写法,不可写为“升价”“降价”等
③标出元素反应类型
一律标出元素所发生的反应,“被氧化”或“被还原”,其余写法均不正确
4.检查得失电子守恒
检查得失电子数是否相等,如不相等则重新分析。
本题难度:一般
4、选择题 下列关于锶(Sr,核电核数为38)的单质(密度为2.50g/cm3),一定错误的是
A.颗粒状的单质锶投入水中,剧烈反应,生成大量的气体并引起气体燃烧和轻微爆炸
B.颗粒状的单质锶与稀硫酸反应,反应现象不如钠和水反应那么剧烈
C.锶在纯氧中点燃可燃烧,燃烧生产的产物投入水中可以放出气体
D.锶在纯净氮气中可以燃烧,燃烧产物投入水中可以放出气体
参考答案:A 。
本题解析:根据同主族元素及其化合物性质的递变规律可以推知,硫酸锶的溶解性应该很小(介于硫酸钙微溶和硫酸钡不溶之间),由于硫酸锶的难溶,因此硫酸与锶反应生成的产物覆盖在锶的表面,阻碍两者反应的进行,减缓了反应速率。因此B的叙述是正确的。而选项A,锶投入水中,反应当然会剧烈进行,但是由于锶的密度比水大,沉于水中,因此不可能看到和钾与水反应的相同的现象(钾浮于水面,反应剧烈,产生的热量将引起气体燃烧和轻微爆炸)
本题难度:简单
5、选择题 一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体V L(标准状况),向反应后的溶液中(存在Cu2+和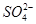 )加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 12.0 g,若上述气体为NO和NO2的混合物,且体积比为1∶1,则V可能为
)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 12.0 g,若上述气体为NO和NO2的混合物,且体积比为1∶1,则V可能为
A.9.0 L
B.13.5 L
C.15.7 L
D.16.8 L
参考答案:A
本题解析:若混合物全是CuS,其物质的量为12/80=0.15 mol,电子转移数0.15 mol×(6+2)=1.2 mol。两者体积相等,设NO x mol,NO2 x mol,3x+x=1.2,计算的x=0.3。气体体积V=0.6 mol×22.4 L・mol-1=13.44 L;若混合物全是Cu2S,其物质的量为0.075 mol,转移电子数0.075 mol×10=0.75 mol,设NO x mol,NO2 x mol,3x+x=0.75,计算得x=0.187 5,气体体积V=0.375 mol×22.4 L・mol-1=8.4 L,因此8.4 L<V<13.44 L。
本题难度:一般