| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《未知》高频考点特训(2017年练习版)(八)
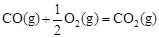 △H2=-283 kJ・mol-1 △H2=-283 kJ・mol-1 △H3=-242 kJ・mol-1 △H3=-242 kJ・mol-1则表示1mol气态甲醇完全燃烧生成CO 2和水蒸气时的热化学方程式为 ; ③在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。请回答: 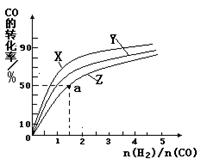 参考答案: 本题解析: 本题难度:困难 3、选择题 将Cu与CuO的混合物20.8g加入到50mL 18.4mol/L浓H2SO4中,加热充分反应至固体物质完全溶解(产生气体全部逸出),冷却后将溶液稀释至1000ml,测得c(H+)=0.84mol/L;若要使稀释后溶液中的Cu2+沉淀完全,应加入6.0mol/L的NaOH溶液的体积为: 参考答案:D 本题解析:由题意可知,Cu与CuO的混合物与硫酸反应硫酸有剩余,向稀释后溶液中加入NaOH使Cu2+沉淀完全,硫酸、硫酸铜都与氢氧化钠反应,此时溶液中溶质为Na2SO4, 本题难度:一般 4、填空题 向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol・L -1HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况)。(已知:Cu2O+2H+=Cu+Cu2++H2O) 参考答案:(1)3Cu2O+ 14H+ + 2NO3-=6Cu2+ +2 NO↑+ 7H2O?(2)16?(3)0.1mol 本题解析:(1)Cu2O跟稀硝酸反应的离子方程式为3Cu2O+ 14H+ + 2NO3-=6Cu2+ +2 NO↑+ 7H2O。(2)n(HNO3)=0.6mol,n(NO)=2.24L÷22.4L/mol=0.1mol.所以n(Cu(NO3)2)=1/2n(NO3-)=0.25mol.所以若将上述混合物用足量的H2加热还原,所得到固体的质量即为Cu的质量。m(Cu)= 0.25mol×64g/mol=16g。(3)若混合物中含0.1 mol Cu,根据方程式3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O可知Cu产生的NO的物质的量为0.2/3mol,则Cu2O与硝酸反应产生的NO的物质的量为0.1mol-2/3×0.1mol=0.1/3mol.在根据3Cu2O+ 14H+ + 2NO3-=6Cu2+ +2 NO↑+ 7H2O可计算出Cu2O的物质的量为0.05mol.所以CuO物质的量为(0.15-0.2/3-0.1/3)mol=0.05mol结合方程式:CuO+H2SO4=CuSO4+H2O; Cu2O+H2SO4="Cu+" Cu SO4+H2O.可知:消耗的H2SO4的物质的量为0.05mol+0.05mol=0.1mol.2O和CuO与硝酸、硫酸反应原理及离子方程式的书写及个组分含量的计算。 本题难度:一般 5、填空题 配平该化学方程式______K37ClO3+______H35Cl-______KCl+______Cl2+______H2O. 参考答案:KClO3中Cl元素的化合价由+5价降低为0价,HCl中Cl元素的化合价由-1价升高到0,根据电子守恒及质量守恒定律来配平,所以其方程式为:1K37ClO3+6H35Cl=1KCl+3Cl2 ↑+3H2O,该反应氯化氢中部分氯元素失电子、部分化合价不变,所以氯化氢体现了酸性和还原性,根据方程式知,转移5mol电子生成3mol氯气,所以若反应中有1.5mol电子发生转移生成Cl2的物质的量=1.5mol×3mol5mol=0.9mol,其平均摩尔质量=0.9mol×2×16(37+35×5)g/mol0.9mol=70.7g/mol,所以其平均相对分子质量为70.7, 本题解析: 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《电解池原理.. | |